
已知:锂离子电池的总反应为LixC+Li1-xCoO2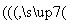 C+LiCoO2
C+LiCoO2
锂硫电池的总反应为2Li+S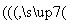 Li2S
Li2S
有关上述两种电池说法正确的是( )
A.锂离子电池放电时,Li+向负极迁移
B.锂硫电池充电时,锂电极发生还原反应
C.理论上两种电池的比能量相同
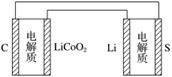
D.下图表示用锂离子电池给锂硫电池充电
科目:高中化学 来源: 题型:
某烃的结构简式为: -C≡C-CH=CH-CH3,有关其结构说法正确的是
-C≡C-CH=CH-CH3,有关其结构说法正确的是
A.所有原子可能在同一平面上 B.所有碳原子可能在同一条直线上
C.所有碳原子可能在同一平面上 D.所有原子可能在同一直线上
查看答案和解析>>
科目:高中化学 来源: 题型:
判断正误,正确的划“√”,错误的划“×”
(1)在原电池中,发生氧化反应的一极一定是负极( )
(2)在原电池中,负极材料的活泼性一定比正极材料强( )
(3)在原电池中,正极本身一定不参与电极反应,负极本身一定要发生氧化反应( )
(4)其他条件均相同,带有“盐桥”的原电池比不带“盐桥”的原电池电流持续时间长( )
查看答案和解析>>
科目:高中化学 来源: 题型:
以甲烷燃料电池为例来分析不同的环境下电极反应式的书写。
(1)酸性介质(如H2SO4)
负极:________________________________________________________________________;
正极:________________________________________________________________________;
总反应式:___________________________________________________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
下图Ⅰ、Ⅱ分别是甲、乙两组同学将反应“AsO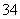 +2I-+2H+??AsO
+2I-+2H+??AsO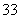 +I2+H2O”设计成的原电池装置,其中C1、C2均为碳棒。甲组向图Ⅰ烧杯中逐滴加入适量浓盐酸;乙组向图ⅡB烧杯中逐滴加入适量40% NaOH溶液。
+I2+H2O”设计成的原电池装置,其中C1、C2均为碳棒。甲组向图Ⅰ烧杯中逐滴加入适量浓盐酸;乙组向图ⅡB烧杯中逐滴加入适量40% NaOH溶液。
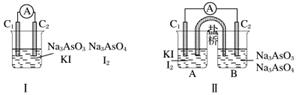
下列叙述中正确的是( )
A.甲组操作时,电流表(A)指针不发生偏转
B.甲组操作时,溶液颜色变浅
C.乙组操作时,C2作正极
D.乙组操作时,C1上发生的电极反应为I2+2e-===2I-
查看答案和解析>>
科目:高中化学 来源: 题型:
银质器皿日久表面会逐渐变黑,这是生成了Ag2S的缘故,根据电化学原理可进行如下处理,在铝质容器中加入食盐溶液,再将变黑的银器浸入该溶液中,一段时间后发现黑色会褪去,下列说法正确的是( )
A.处理过程中银器一直保持恒重
B.银器为正极,Ag2S被还原生成单质银
C.该过程中总反应为2Al+3Ag2S===6Ag+Al2S3
D.黑色褪去的原因是黑色Ag2S转化为白色AgCl
查看答案和解析>>
科目:高中化学 来源: 题型:
锂空气电池作为新一代大容量电池而备受瞩目,其工作原理如图所示。下列有关锂空气电池的说法不正确的是( )
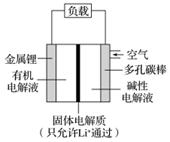
A.随着电极反应的不断进行,正极附近的电解液pH不断升高
B.若把碱性电解液换成固体氧化物电解质,则正极会因为生成Li2O而引起碳孔堵塞,不利于正极空气的吸附
C.放电时,当有22.4 L O2(标准状况下)被还原时,溶液中有4 mol Li+从左槽移动到右槽
D.锂空气电池又称作“锂燃料电池”,其总反应方程式为4Li+O2===2Li2O
查看答案和解析>>
科目:高中化学 来源: 题型:
用图中装置进行实验,实验一段时间后,现象与预测不一致的是
| ①中物质 | ②中物质 |
| |
| A | 浓氨水 | 酚酞试液 | ②中溶液变为红色 |
| B | 浓硝酸 | 淀粉KI溶液 | ②中溶液变为蓝色 |
| C | 浓盐酸 | 浓氨水 | 大烧杯中有白烟 |
| D | 饱和的亚硫酸溶液 | 稀溴水 | ②中无明显变化 |
查看答案和解析>>
科目:高中化学 来源: 题型:
四种元素X、Y、Z、E位于元素周期表的前四周期,已知它们的核电荷数依次增大,Y原子的L层p轨道中有2个电子;Z原子的L电子层中,有三个未成对的电子,且无空轨道;E原子的L层电子数与最外层电子数之比为4∶1,其d轨道中的电子数与最外层电子数之比为5∶1。
(1)XYZ分子中的三个原子除X原子外最外层均为8电子构型,根据电子云重叠方式的不同,该分子中共价键的主要类型有________________。
(2)ZX3是一种常见气体,分子中Z原子的杂化方式是________,该物质易液化,极易溶 于水,其原因是____
于水,其原因是____ ______________________。
______________________。
(3)E元素+2价离子的核外电子排布式为________。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com