
分析 A、B、C、D、E、F为中学化学常见的单质和化合物.常温常压下,A为淡黄色固体,B为最常见的无色无味液体,A与B反应产生使带火星木条复燃的无色无味气体D和E的溶液.判断D为O2,A为Na2O2,B为H2O,D为O2,E为NaOH,C为银白色金属,切开后表面迅速变暗,C与B反应可得到无色气体F和E的溶液,说明C为Na,F为H2,据此分析回答问题.
解答 解:A、B、C、D、E、F为中学化学常见的单质和化合物.常温常压下,A为淡黄色固体,B为最常见的无色无味液体,A与B反应产生使带火星木条复燃的无色无味气体D和E的溶液.判断D为O2,A为Na2O2,B为H2O,D为O2,E为NaOH,C为银白色金属,切开后表面迅速变暗,C与B反应可得到无色气体F和E的溶液,说明C为Na,F为H2,
(1)D的化学式为O2,故答案为:O2;
(2)C单质为Na是活泼金属在空气中被氧气氧化,实验室通常保存在煤油中和空气隔离,故答案为:煤油;
(3)B与C反应是钠和水反应生成氢氧化钠和氢气,反应的离子方程式为2Na+2H2O=2Na++2OH-+H2↑,故答案为:2Na+2H2O=2Na++2OH-+H2↑;
(4)A物质可用于潜水艇中作为氧气的来源,是过氧化钠和呼出的二氧化碳反应生成碳酸钠和氧气,反应的化学方程式为2Na2O2+2CO2=2Na2CO3+O2,
故答案为:过氧化钠和呼出的二氧化碳反应生成碳酸钠和氧气.
点评 本题考查了钠及其化合物性质分析,转化关系的理解应用,主要是物质特征性质的熟练掌握,题目难度不大.


科目:高中化学 来源: 题型:填空题
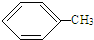 +3HO-NO2$\stackrel{浓硫酸}{→}$
+3HO-NO2$\stackrel{浓硫酸}{→}$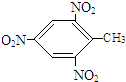 +3H2O.
+3H2O. .
.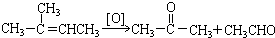
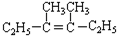 在上述类似条件下发生反应,请写出反应的方程式
在上述类似条件下发生反应,请写出反应的方程式 .
.查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 将煤干馏可以提高能源的利用率 | |
| B. | 甲烷也是一种温室气体,应禁止使用天然气 | |
| C. | 锌-锰干电池是对环境没任何污染的理想电池 | |
| D. | 寻找高效催化剂,使二氧化硅分解产生硅的同时释放能量 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题

| A. | 铜电极上发生反应Cu-2e-=Cu2+ | |
| B. | 工作一段时间后,乙池的c(SO42-)减小 | |
| C. | 电流从铜极经过导线移向锌极 | |
| D. | 电池工作一段时间后,甲池的c(Zn2+)增加 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 手机上用的锂离子电池属于二次电池 | |
| B. | 充电电池可以无限制地反复使用 | |
| C. | 甲醇燃料电池可把化学能转化为电能 | |
| D. | 废旧电池不能乱扔,需回收处理 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | ①③ | B. | ②③ | C. | ④① | D. | ④② |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| X | |||
| Y | Z | W | A |
| T | B |
| A. | X、W、Z元素的原子半径与它们的气态氢化物的热稳定性变化趋势相反 | |
| B. | Y、Z、W、A元素性质均较为活泼,但其中Y、W在自然界中存在游离态的形式,它们的最高价氧化物的水化物的酸性依次递增 | |
| C. | 工业上电解A的钠盐溶液可以得到多种产物,为防止产物互相反应常使用阳离子交换膜,其阴极反应式为:2H2O+2e-═2OH-+H2↑ | |
| D. | 根据元素周期律,可以推测T元素的单质具有半导体特性,T2W3具有氧化性和还原性 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 向铝盐溶液中不断加入偏铝酸钠溶液 | |
| B. | 向盐酸中不断加入偏铝酸钠溶液 | |
| C. | 向氢氧化钠溶液中加铝盐溶液 | |
| D. | 向偏铝酸盐中下断加入盐酸 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 定容时观察液面仰视 | B. | 定容时观察液面俯视 | ||
| C. | 有少量NaOH溶液残留在烧杯中 | D. | 容量瓶中原来有少量蒸馏水 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com