
| T/”ę | 700 | 800 | 830 | 1000 | 1200 |
| K | 0.6 | 0.9 | 1.0 | 1.7 | 2.6 |
·ÖĪö £Ø1£©ÉżøßĪĀ¶Č£¬»ÆŃ§Ę½ŗāĻņĪüČČ·½ĻņŅĘ¶Æ£¬øł¾ŻĪĀ¶Č»Æѧ»ÆŃ§Ę½ŗā³£Źż¹ŲĻµČ·¶Ø·“Ó¦ČČ£»
£Ø2£©ĻČ¼ĘĖćÅضČÉĢ£¬øł¾ŻÅضČÉĢÓė»ÆŃ§Ę½ŗā³£ŹżĻą¶Ō“óŠ”Č·¶Ø·“Ó¦ŹĒ·ń“ļµ½Ę½ŗāדĢ¬£»
£Ø3£©ĻČ¼ĘĖćÅضČÉĢ£¬øł¾ŻÅضČÉĢŗĶ»ÆŃ§Ę½ŗā³£ŹżĻą¶Ō“óŠ”Č·¶Ø·“Ó¦·½Ļņ£¬“Ó¶ųČ·¶ØÕżÄę·“Ó¦ĖŁĀŹĻą¶Ō“󊔣»
£Ø4£©Éč²Ī¼Ó·“Ó¦µÄc£ØCO2£©=xmol/L£¬æŖŹ¼Ź±c£ØCO2£©=2mol/L”¢c£ØH2£©=1mol/L£¬
øĆ·“Ó¦ÖŠCO2£Øg£©+H2£Øg£©?CO£Øg£©+H2O£Øg£©£¬
æŖŹ¼£Ømol/L£©2 1 0 0
·“Ó¦£Ømol/L£©x x x x
Ę½ŗā£Ømol/L£©2-x 1-x x x
»ÆŃ§Ę½ŗā³£ŹżK=$\frac{x£®x}{£Ø2-x£©£®£Ø1-x£©}$=1.0
x=$\frac{2}{3}$£¬
¶žŃõ»ÆĢ¼×Ŗ»ÆĀŹ=$\frac{xmol/L}{2mol/L}$”Į100%£»
ĒāĘų×Ŗ»ÆĀŹ=$\frac{xmol/L}{1mol/L}$”Į100%£»
ČōŌŁ³äČė1mol H2£¬Ę½ŗāÕżĻņŅĘ¶Æ£¬µ«×Ŗ»ÆµÄĒāĘųĪļÖŹµÄĮæŌ¶Ō¶Š”ÓŚ¼ÓČėµÄĒāĘųĪļÖŹµÄĮ森
½ā“š ½ā£ŗ£Ø1£©øł¾Ż±ķÖŠŹż¾ŻÖŖ£¬ÉżøßĪĀ¶ČĘ½ŗā³£ŹżŌö“ó£¬ĖµĆ÷Ę½ŗāÕżĻņŅĘ¶Æ£¬ŌņÕż·“Ó¦ŹĒĪüČČ·“Ó¦£¬¹Ź“š°øĪŖ£ŗĪüČČ£»
£Ø2£©øĆ·“Ó¦ÅضČÉĢ=$\frac{0.01”Į0.03}{0.01”Į0.05}$=0.6£¼1.0£¬ÅضČÉĢŠ”ÓŚĘ½ŗā³£Źż£¬Ć»ÓŠ“ļµ½Ę½ŗāדĢ¬£¬Ę½ŗāÕżĻņŅĘ¶Æ£¬
¹Ź“š°øĪŖ£ŗ·ń£»
£Ø3£©øĆ·“Ó¦ÅضČÉĢ=$\frac{0.01”Į0.03}{0.01”Į0.05}$=0.6£¼0.9£¬ÅضČÉĢŠ”ÓŚĘ½ŗā³£Źż£¬Ę½ŗāÕżĻņÅØ¶Č£¬ŌņÕż·“Ó¦ĖŁĀŹ“óÓŚÄę·“Ó¦ĖŁĀŹ£¬¼“H2OµÄĻūŗÄĖŁĀŹ±ČÉś³ÉĖŁĀŹŠ”£¬¹Ź“š°øĪŖ£ŗŠ”£»
£Ø4£©Éč²Ī¼Ó·“Ó¦µÄc£ØCO2£©=xmol/L£¬æŖŹ¼Ź±c£ØCO2£©=2mol/L”¢c£ØH2£©=1mol/L£¬
øĆ·“Ó¦ÖŠCO2£Øg£©+H2£Øg£©?CO£Øg£©+H2O£Øg£©£¬
æŖŹ¼£Ømol/L£©2 1 0 0
·“Ó¦£Ømol/L£©x x x x
Ę½ŗā£Ømol/L£©2-x 1-x x x
»ÆŃ§Ę½ŗā³£ŹżK=$\frac{x£®x}{£Ø2-x£©£®£Ø1-x£©}$=1.0
x=$\frac{2}{3}$£¬
¶žŃõ»ÆĢ¼×Ŗ»ÆĀŹ=$\frac{xmol/L}{2mol/L}$=$\frac{\frac{2}{3}mol/L}{2mol/L}$=$\frac{1}{3}$£»
ĒāĘų×Ŗ»ÆĀŹ=$\frac{xmol/L}{1mol/L}$=$\frac{\frac{2}{3}mol/L}{1mol/L}$=$\frac{2}{3}$£»
ČōŌŁ³äČė1mol H2£¬Ę½ŗāÕżĻņŅĘ¶Æ£¬µ«×Ŗ»ÆµÄĒāĘųĪļÖŹµÄĮæŌ¶Ō¶Š”ÓŚ¼ÓČėµÄĒāĘųĪļÖŹµÄĮ棬ĖłŅŌĒāĘų×Ŗ»ÆĀŹ¼õŠ”£¬
¹Ź“š°øĪŖ£ŗ$\frac{1}{3}$£»$\frac{2}{3}$£»¼õŠ”£®
µćĘĄ ±¾Ģāæ¼²é»ÆŃ§Ę½ŗā¼ĘĖć£¬ĪŖøßĘµæ¼µć£¬²ąÖŲæ¼²éѧɜ·ÖĪö¼ĘĖćÄÜĮ¦£¬ÕżČ·ĄūÓĆ»ÆŃ§Ę½ŗā³£ŹżÓėÅضČÉĢ¹ŲĻµ½ųŠŠ¼ĘĖćŹĒ½ā±¾Ģā¹Ų¼ü£¬»įøł¾ŻÅضČÉĢÓė»ÆŃ§Ę½ŗā³£ŹżĻą¶Ō“óŠ”Č·¶Ø·“Ó¦·½Ļņ”¢ÕżÄę·“Ó¦ĖŁĀŹĻą¶Ō“󊔣¬ĢāÄæÄŃ¶Č²»“ó£®



| Äź¼¶ | øßÖŠæĪ³Ģ | Äź¼¶ | ³õÖŠæĪ³Ģ |
| øßŅ» | øßŅ»Ćā·ŃæĪ³ĢĶĘ¼ö£” | ³õŅ» | ³õŅ»Ćā·ŃæĪ³ĢĶĘ¼ö£” |
| ø߶ž | ø߶žĆā·ŃæĪ³ĢĶĘ¼ö£” | ³õ¶ž | ³õ¶žĆā·ŃæĪ³ĢĶĘ¼ö£” |
| øßČż | øßČżĆā·ŃæĪ³ĢĶĘ¼ö£” | ³õČż | ³õČżĆā·ŃæĪ³ĢĶĘ¼ö£” |
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗŃ”ŌńĢā
| A£® | ÄĘ | B£® | Ģ¼ | C£® | µŖ | D£® | Įņ |
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗŃ”ŌńĢā
| A£® | Fe3+”¢Ba2+”¢NO3-”¢Cl- | B£® | K+”¢Na+”¢OH-”¢NO3- | ||
| C£® | H+”¢Ag+”¢Cl-”¢SO42- | D£® | Cu2+”¢Ca2+”¢SO42-”¢OH- |
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ½ā“šĢā

²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗŃ”ŌńĢā
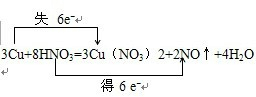
 ČēĶ¼æÉÄę·“Ó¦A+2B?2C+3DµÄ»Æѧ·“Ó¦ĖŁĀŹÓė»ÆŃ§Ę½ŗāĖęĶā½ēĢõ¼žøıä£ØĻČ½µĪĀŗó¼ÓŃ¹£©¶ų±ä»ÆµÄĒéæö£¬ÓÉ“ĖæÉĶʶĻ£Ø””””£©
ČēĶ¼æÉÄę·“Ó¦A+2B?2C+3DµÄ»Æѧ·“Ó¦ĖŁĀŹÓė»ÆŃ§Ę½ŗāĖęĶā½ēĢõ¼žøıä£ØĻČ½µĪĀŗó¼ÓŃ¹£©¶ų±ä»ÆµÄĒéæö£¬ÓÉ“ĖæÉĶʶĻ£Ø””””£©| A£® | Õż·“Ó¦ŹĒĪüČČ·“Ó¦ | B£® | ČōA”¢BŹĒĘųĢ壬ŌņDŹĒŅŗĢå»ņ¹ĢĢå | ||
| C£® | øıäĪļÖŹÅØ¶Č£¬Ę½ŗā²»»įŅĘ¶Æ | D£® | A”¢B”¢C”¢D¾łĪŖĘųĢå |
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗŃ”ŌńĢā
| A£® | +99.7kJ•mol-1 | B£® | +29.7kJ•mol-1 | C£® | -20.6kJ•mol-1 | D£® | -241.8kJ•mol-1 |
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ½ā“šĢā
 Fe£ØSCN£©3£®
Fe£ØSCN£©3£®²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗĢīæÕĢā
 £®
£®²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗŃ”ŌńĢā
| A£® | ¹¤ŅµŗĻ³É°±ÖŠ£¬½«°±ĘųŅŗ»Æ·ÖĄėŅŌĢįøß°±Ęų²śĀŹ | |
| B£® | æŖĘōĘ”¾ĘĘæŗó£¬ĘæÖŠĀķÉĻ·ŗĘš“óĮæÅŻÄ | |
| C£® | ŹµŃéŹŅÖŠ³£ÓĆÅű„ŗĶŹ³ŃĪĖ®µÄ·½·ØŹÕ¼ÆĀČĘų | |
| D£® | Į½Ö§ŹŌ¹ÜÖŠ·Ö±š¼ÓČėµČĢå»ż5%µÄH3O2ČÜŅŗ£¬ŌŚĘäÖŠŅ»Ö§ŹŌ¹ÜÖŠ¼ÓČė2”«3µĪFeCl3ČÜŅŗ£¬øĆŹŌ¹ÜÖŠ²śÉśĘųÅŻæģ |
²éæ““š°øŗĶ½āĪö>>
°Ł¶ČÖĀŠÅ - Į·Ļ°²įĮŠ±ķ - ŹŌĢāĮŠ±ķ
ŗž±±Ź”»„ĮŖĶųĪ„·ØŗĶ²»Į¼ŠÅĻ¢¾Ł±ØĘ½ĢØ | ĶųÉĻÓŠŗ¦ŠÅĻ¢¾Ł±Ø×ØĒų | µēŠÅÕ©Ę¾Ł±Ø×ØĒų | É꥜Ź·ŠéĪŽÖ÷ŅåÓŠŗ¦ŠÅĻ¢¾Ł±Ø×ØĒų | ÉęĘóĒÖČؾŁ±Ø×ØĒų
Ī„·ØŗĶ²»Į¼ŠÅĻ¢¾Ł±Øµē»°£ŗ027-86699610 ¾Ł±ØÓŹĻä£ŗ58377363@163.com