
| A. | 天然气隔绝空气高温分解生成炭黑和氢气 | |
| B. | 石油分馏得到汽油、煤油和柴油 | |
| C. | 石油裂解得到乙烯、丙烯、丁二烯 | |
| D. | 煤干馏生成焦炭、煤焦油、焦炉气和粗氨水 |
分析 A.天然气的主要成分为甲烷,甲烷燃烧是甲烷和氧气反应生成二氧化碳和水;
B.分馏的原理,是利用液体混合物中各成分的不同沸点,进行逐一先汽化后冷却液化,分离成相对纯净物质的过程;
C.油裂解是将石油中大分子的烃发生化学反应生成小分子的烃;
D.煤的干馏是将煤隔绝空气加强热,生成焦炭、煤焦油、焦炉气和粗氨水.
解答 解:A.天然气的主要成分为甲烷,甲烷燃烧是甲烷和氧气反应生成二氧化碳和水,显然属于化学变化,故A错误;
B.分馏的原理,是利用液体混合物中各成分的不同沸点,进行逐一先汽化后冷却液化,分离成相对纯净物质的过程,只是将原来的物质分离,没有新物质生成,是物理变化.石油就是由沸点不同的汽油、煤油、柴油等混合而成,通过分馏将它们分离,是物理变化,故B正确;
C.石油裂解是将石油中大分子的烃发生化学反应生成小分子的烃,得到乙烯、丙烯、丁二烯,是化学变化,故C错误;
D.煤的干馏是将煤隔绝空气加强热,生成焦炭、煤焦油、焦炉气和粗氨水,是化学变化,故D错误;
故选B.
点评 本题考查物理变化与化学变化的区别与联系,难度不大,解答时要分析变化过程中是否有新物质生成,这里的新物质是指和变化前的物质是不同种的物质,若没有新物质生成属于物理变化,若有新物质生成属于化学变化.


科目:高中化学 来源: 题型:选择题
| A. | 碳酸镁 | B. | 氢氧化铝 | C. | 碳酸钙 | D. | 氢氧化钠 |
查看答案和解析>>
科目:高中化学 来源: 题型:填空题
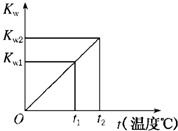 若t1=25℃,则Kw1=10-14;若t2=100℃时,Kw2=10-12,则此时0.05mol•L-1的Ba (OH)2溶液的pH=11.
若t1=25℃,则Kw1=10-14;若t2=100℃时,Kw2=10-12,则此时0.05mol•L-1的Ba (OH)2溶液的pH=11.查看答案和解析>>
科目:高中化学 来源: 题型:解答题
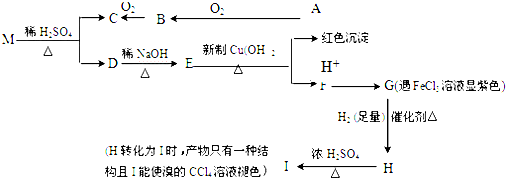
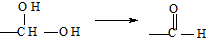
 ;②H→I:
;②H→I: .
. .
.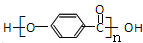 .
. 等.(任写一种)
等.(任写一种)查看答案和解析>>
科目:高中化学 来源: 题型:多选题
| A. | O3与CO2的结构相似 | |
| B. | 硫粉不溶于水,易溶于酒精,难溶于CS2中 | |
| C. | Be(OH)2是两性氢氧化物 | |
| D. | 在相同条件下,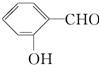 的沸点高于 的沸点高于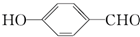 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 检验SO42-:加入BaCl2溶液出现白色沉淀,再加足量稀盐酸沉淀不溶解 | |
| B. | 检验Cl-:加入AgNO3溶液出现白色沉淀 | |
| C. | 检验Na+:将干净的铂丝蘸取少量溶液在酒精灯上灼烧,观察火焰呈浅紫色 | |
| D. | 检验NH4+:滴入浓NaOH溶液后,加热,用湿润红色石蕊试纸检验产生气体发现变蓝 |
查看答案和解析>>
科目:高中化学 来源: 题型:多选题
| A. | 115.75mL | B. | 134.48mL | C. | 143.75mL | D. | 156.8mL |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com