
| A. | 常温常压下,1mol氦气含有4nA个质子 | |
| B. | 1molNa2O2与足量CO2充分反应转移了2nA个电子 | |
| C. | 含49gH2SO4的硫酸溶液中含有nA个氢原子 | |
| D. | 标准状况下,22.4LHCHO含有nA个分子 |
分析 A.氦气是单原子分子,1mol氦气含有1molHe原子,含2mol质子;
B.1mol过氧化钠完全反应生成0.5mol氧气,过氧化钠中氧元素的化合价为-1价;
C.硫酸溶液中,硫酸和水分子中都含有H原子,漏掉了水分子中的氢原子;
D.标况下,甲醛为气体,可以使用标况下的气体摩尔体积计算.
解答 解:A.1mol氦气含有1molHe原子,含2mol质子,含有2nA个质子,故A错误;
B.1mol过氧化钠与二氧化碳完全反应生成0.5mol氧气,转移了1mol电子,转移了2nA个电子,故B错误;
C.49gH2SO4的物质的量为:$\frac{49g}{98g/mol}$=0.5mol,0.5mol硫酸中含有1mol氢原子,溶液中的水分子也含有H原子,则溶液中含有的H原子数大于nA,故C错误;
D.标况下,甲醛为气体,22.4L甲醛的物质的量为1mol,含有nA个甲醛分子,故D正确;
故选D.
点评 本题考查了阿伏伽德罗常数的计算与判断,题目难度中等,明确物质的量与阿伏伽德罗常数、摩尔质量等物理量之间的关系为解答关键,A、C为易错点,注意稀有气体为氮原子分子、硫酸溶液中的水分子也含有H原子.


科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 采用“静电除尘”、“燃煤固硫”、“汽车尾气催化净化”可提高空气质量 | |
| B. | 酸性氧化物均能与水反应生成对应的酸,如CO2、SiO2、SO3 | |
| C. | 石油化工中的裂化、裂解过程都是通过化学反应来获得气态烯烃 | |
| D. | 乙醇、过氧化氢、次氯酸钠等均通过氧化作用达到杀菌消毒的目的 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
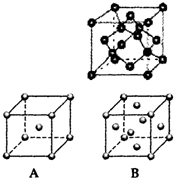 现有A、B、C、D、E、F、G原子序数依次增大的七种元素,它们位于元素周期表的前四周期.B元素含有3个能级,且每个能级所含的电子数相同;D的原子核外有8个运动状态不同的电子;在这七种元素中E元素原子半径最大,A原子半径最小;F元素与G元素处于同一周期相邻的族,它们的原子序数相差3,且F元素的基态原子有4个未成对电子.请回答下列问题:
现有A、B、C、D、E、F、G原子序数依次增大的七种元素,它们位于元素周期表的前四周期.B元素含有3个能级,且每个能级所含的电子数相同;D的原子核外有8个运动状态不同的电子;在这七种元素中E元素原子半径最大,A原子半径最小;F元素与G元素处于同一周期相邻的族,它们的原子序数相差3,且F元素的基态原子有4个未成对电子.请回答下列问题:查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 1 mol Cu和足量的硫反应,转移的电子数为nA | |
| B. | 标准状况下,22.4 L氯仿中含有的分子数为nA | |
| C. | 25℃时,pH=13的Ba(OH)2溶液中含有的OH-数目为0.1nA | |
| D. | 53.5g NH4Cl中含有的分子数为NA |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
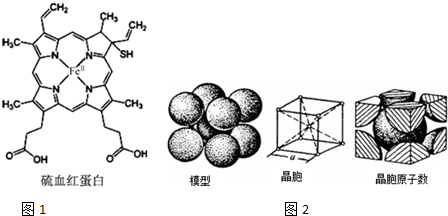
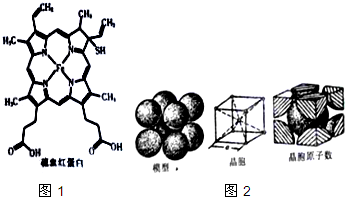 血红蛋白是高等生物体内负责运载氧的一种蛋白质(缩写为HB或HCB).与正常血红蛋白相比,硫血红蛋白不能与氧结合,因此失去携带氧的能力.如图1所示为硫血红蛋白的结构.请回答下列问题:
血红蛋白是高等生物体内负责运载氧的一种蛋白质(缩写为HB或HCB).与正常血红蛋白相比,硫血红蛋白不能与氧结合,因此失去携带氧的能力.如图1所示为硫血红蛋白的结构.请回答下列问题:查看答案和解析>>
科目:高中化学 来源: 题型:选择题
 判断下列说法中不正确的是( )
判断下列说法中不正确的是( )| A. | 乙物质为甲醇 | |
| B. | 该反应为取代反应 | |
| C. | 甲与乙都能与金属钠反应产生氢气 | |
| D. | 甲、乙、丙都能与溴的四氯化碳溶液发生加成反应 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| 选项 | 甲组 | 乙组 |
| A | Al(OH)3、稀盐酸 | NaOH溶液、氨水 |
| B | O2、N2 | H2、Mg |
| C | Cu、NaOH溶液 | FeCl3溶液、稀硝酸 |
| D | SiO2、Cl2 | HF、H2SO3 |
| A. | A | B. | B | C. | C | D. | D |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com