
化学学习中,推理是一种重要的学习方法,下列推论正确的是
A.由“BF3和SO3互为等电子体”,可推知二者均为非极性分子
B.由“同主族元素性质相似,CO2为直线形分子”,可推知SiO2为直线形分子
C.由“SiH4的熔沸点比CH4高”,可推知PH3的熔沸点比NH3高
D.由“C、N、O三种元素的电负性C<N<O”,可推知第一电离能C<N<O
科目:高中化学 来源: 题型:单选题
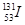 是常规核裂变产物之一,可以通过测定大气或水中
是常规核裂变产物之一,可以通过测定大气或水中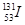 的含量变化来检测核电站是否发生放射性物质泄漏。下列有关
的含量变化来检测核电站是否发生放射性物质泄漏。下列有关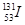 的叙述中错误的是( )
的叙述中错误的是( )
A.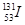 的化学性质与 的化学性质与 相同 相同 | B.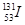 的原子序数为53 的原子序数为53 |
C.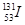 的原子核外电子数为78 的原子核外电子数为78 | D.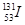 的原子核内中子数多于质子数 的原子核内中子数多于质子数 |
查看答案和解析>>
科目:高中化学 来源: 题型:单选题
A、B、C为三种短周期元素,A、B同周期,A、C的最低价离子分别为A2-、C-,B2+与C-
C具有相同的电子层结构,下列叙述一定不正确的是
A.离子半径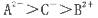
B.它们的原子半径C>B>A
C.它们的原于序数A>B>C
D.原子最外层上的电子数C>A>B
查看答案和解析>>
科目:高中化学 来源: 题型:单选题
短周期元素W、X、Y、Z的原子序数依次增大,W与Y原子的最外层电子数之和为X原子的最外层电子数的2倍,Z原子的最外层电子数等于其最内层电子数,X、Y、Z的简单离子的电子层结构相同,W的单质是空气中体积分数最大的气体。下列说法正确的是
| A.元素Y的气态氢化物比W的稳定 |
| B.元素Y的最高正价与负价绝对值的和等于8 |
| C.化合物XY2与ZY2分子中的化学键类型相同 |
| D.原子半径的大小顺序:r(W)>r(X)>r(Y)>r(Z) |
查看答案和解析>>
科目:高中化学 来源: 题型:单选题
电子层数相同的三种元素X、Y、Z,它们最高价氧化物对应水化物的酸性由强到弱顺序为:HXO4>H2YO4>H3ZO4,下列判断错误的是
| A.原子半径 X>Y>Z | B.气态氢化物稳定性X>Y>Z |
| C.元素原子得电子能力X>Y>Z | D.单质与氢气反应难易X>Y>Z |
查看答案和解析>>
科目:高中化学 来源: 题型:单选题
下列说法正确的是
| A.阴阳离子通过静电吸引形成离子键 |
| B.HF、HCl、HBr、HI的热稳定性和还原性均依次减弱 |
| C.第三周期非金属元素含氧酸的酸性从左到右依次增强 |
| D.元素周期律是元素原子核外电子排布周期性变化的结果 |
查看答案和解析>>
科目:高中化学 来源: 题型:单选题
元素周期表是一座开放的“元素大厦”,“元素大厦”尚未客满。若发现119号元素,请在“元素大厦”中安排好它的“房间”
| A.第七周期0族 | B.第六周期第ⅡA族 |
| C.第八周期第ⅠA族 | D.第七周期第ⅦA族 |
查看答案和解析>>
科目:高中化学 来源: 题型:单选题
A、B、C三种短周期元素在元素周期表中的相对位置如图所示,已知A、C可分别与B形成化合物X和Y,A与B的质子数之和为C的质子数,现有以下说法,其中判断正确的组合是( )
①B与C均存在同素异形体;②X的种类比Y的多③沸点:A的氢化物小于C的氢化物;④C的最高价氧化物对应水化物能与A的氢化物形成三种盐
A.①②③④ B.②③ C.①②④ D.①④
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com