
 A”¢B”¢C”¢D”¢EŹĒŌŖĖŲÖÜĘŚ±ķÖŠŌ×ÓŠņŹżŅĄ“ĪµŻŌöµÄĒ°ĖÄÖÜĘŚŌŖĖŲ£®AŌ×Ó×īĶā²ćµē×ÓŹżĪŖÄŚ²ćµē×ÓŹżµÄ3±¶£»BµÄŃęÉ«·“Ó¦³Ź»ĘÉ«£»CµÄĒā»ÆĪļŹĒŅ»ÖÖĒæĖį£¬ĘäÅØČÜŅŗæÉÓėA”¢EµÄ»ÆŗĻĪļ·“Ӧɜ³ÉCµÄµ„ÖŹ£»DŹĒŅ»ÖÖ½šŹōŌŖĖŲ£¬Ę仳Ģ¬Ō×ÓÖŠÓŠ6øöĪ“³É¶Ōµē×Ó£®Ēė»Ų“šĻĀĮŠĪŹĢā£ŗ
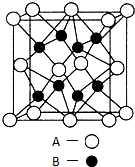
A”¢B”¢C”¢D”¢EŹĒŌŖĖŲÖÜĘŚ±ķÖŠŌ×ÓŠņŹżŅĄ“ĪµŻŌöµÄĒ°ĖÄÖÜĘŚŌŖĖŲ£®AŌ×Ó×īĶā²ćµē×ÓŹżĪŖÄŚ²ćµē×ÓŹżµÄ3±¶£»BµÄŃęÉ«·“Ó¦³Ź»ĘÉ«£»CµÄĒā»ÆĪļŹĒŅ»ÖÖĒæĖį£¬ĘäÅØČÜŅŗæÉÓėA”¢EµÄ»ÆŗĻĪļ·“Ӧɜ³ÉCµÄµ„ÖŹ£»DŹĒŅ»ÖÖ½šŹōŌŖĖŲ£¬Ę仳Ģ¬Ō×ÓÖŠÓŠ6øöĪ“³É¶Ōµē×Ó£®Ēė»Ų“šĻĀĮŠĪŹĢā£ŗ·ÖĪö A”¢B”¢C”¢D”¢EŹĒŌŖĖŲÖÜĘŚ±ķÖŠŌ×ÓŠņŹżŅĄ“ĪµŻŌöµÄĒ°ĖÄÖÜĘŚŌŖĖŲ£®AŌ×Ó×īĶā²ćµē×ÓŹżĪŖÄŚ²ćµē×ÓŹżµÄ3±¶£¬Ō×ÓÖ»ÄÜÓŠ2øöµē×Ó²ć£¬×īĶā²ćµē×ÓŹżĪŖ6£¬ŌņAĪŖOŌŖĖŲ£»BµÄŃęÉ«·“Ó¦³Ź»ĘÉ«£¬ŌņBĪŖNa£»CµÄĒā»ÆĪļŹĒŅ»ÖÖĒæĖį£¬ŌņCĪŖCl£»ĘäÅØČÜŅŗæÉÓėA”¢EµÄ»ÆŗĻĪļ·“Ӧɜ³ÉCµÄµ„ÖŹ£¬Ó¦ŹĒ¶žŃõ»ÆĆĢÓėÅØŃĪĖį·“Ӧɜ³ÉĀČĘų£¬æÉÖŖEĪŖMnŌŖĖŲ£»DŹĒŅ»ÖÖ½šŹōŌŖĖŲ£¬Ę仳Ģ¬Ō×ÓÖŠÓŠ6øöĪ“³É¶Ōµē×Ó£¬“¦ÓŚµŚĖÄÖÜĘŚ£¬ĶāĪ§µē×ÓÅŲ¼ĪŖ3d54s1£¬ŌņDĪŖCr£¬¾Ż“Ė½ā“š£®
½ā“š ½ā£ŗA”¢B”¢C”¢D”¢EŹĒŌŖĖŲÖÜĘŚ±ķÖŠŌ×ÓŠņŹżŅĄ“ĪµŻŌöµÄĒ°ĖÄÖÜĘŚŌŖĖŲ£®AŌ×Ó×īĶā²ćµē×ÓŹżĪŖÄŚ²ćµē×ÓŹżµÄ3±¶£¬Ō×ÓÖ»ÄÜÓŠ2øöµē×Ó²ć£¬×īĶā²ćµē×ÓŹżĪŖ6£¬ŌņAĪŖOŌŖĖŲ£»BµÄŃęÉ«·“Ó¦³Ź»ĘÉ«£¬ŌņBĪŖNa£»CµÄĒā»ÆĪļŹĒŅ»ÖÖĒæĖį£¬ŌņCĪŖCl£»ĘäÅØČÜŅŗæÉÓėA”¢EµÄ»ÆŗĻĪļ·“Ӧɜ³ÉCµÄµ„ÖŹ£¬Ó¦ŹĒ¶žŃõ»ÆĆĢÓėÅØŃĪĖį·“Ӧɜ³ÉĀČĘų£¬æÉÖŖEĪŖMnŌŖĖŲ£»DŹĒŅ»ÖÖ½šŹōŌŖĖŲ£¬Ę仳Ģ¬Ō×ÓÖŠÓŠ6øöĪ“³É¶Ōµē×Ó£¬“¦ÓŚµŚĖÄÖÜĘŚ£¬ĶāĪ§µē×ÓÅŲ¼ĪŖ3d54s1£¬ŌņDĪŖCr£®
£Ø1£©DĪŖCr£¬Ę仳Ģ¬Ō×ÓÖŠÓŠ6øöĪ“³É¶Ōµē×Ó£¬“¦ÓŚµŚĖÄÖÜĘŚ£¬»łĢ¬Ō×Ó¼Ū²ćµē×ÓÅŲ¼Ź½ĪŖ3d54s1£¬
¹Ź“š°øĪŖ£ŗ3d54s1£»
£Ø2£©CĪŖCl£¬ĘäÉĻŅ»ÖÜĘŚĶ¬×åŌŖĖŲµÄĒā»ÆĪļĪŖHF£¬HF·Ö×Ó¼ä“ęŌŚĒā¼ü£¬¶ųHCl·Ö×Ó¼äĪŽĒā¼ü£¬¹ŹHClµÄ·ŠµćµĶÓŚHF£¬
¹Ź“š°øĪŖ£ŗHF·Ö×Ó¼ä“ęŌŚĒā¼ü£¬¶ųHCl·Ö×Ó¼äĪŽĒā¼ü£»
£Ø3£©AĪŖOŌŖĖŲ”¢CĪŖClŌŖĖŲ£¬¶žÕߊĪ³ÉµÄŃõ»ÆĪļÖŠOŌŖĖŲ±ķĻÖøŗ»ÆŗĻ¼Ū£¬¶Ō¼üŗĻµē×ÓĪüŅżĮ¦øü“󣬹ŹµēøŗŠŌ“óŠ”Ė³ŠņŹĒO£¾Cl£¬ClµÄ×īøß¼Ūŗ¬ŃõĖįøłĪŖClO4-£¬ClŌ×Ó¼Ū²ćµē×Ó¶ŌŹżĪŖ4+$\frac{7+1-2”Į4}{2}$=4£¬Ć»ÓŠ¹Ā¶Ōµē×Ó£¬¹ŹĘäæռ乹ŠĶĪŖÕżĖÄĆęĢ壬ĘäClŌ×ÓµÄŌÓ»ÆĄąŠĶĪŖsp3Ōӻƣ¬
¹Ź“š°øĪŖ£ŗO£¾Cl£»ÕżĖÄĆęĢ壻sp3£»
£Ø4£©¾§°ūÖŠNaŌ×ÓŹżÄæĪŖ8£¬OŌ×ÓŹżÄæĪŖ8”Į$\frac{1}{8}$+6”Į$\frac{1}{2}$=4£¬Na”¢OŌ×ÓŹżÄæÖ®±ČĪŖ8£ŗ4=2£ŗ1£¬¹ŹøĆ¾§°ūµÄ»ÆѧŹ½ĪŖNa2O£¬ŅŌÉĻĆęĆęŠÄÖŠAĄė×ÓŃŠ¾æ£¬ÓėÖ®ĻąĮŚµÄBĄė×ÓÓŠ8øö£¬ĮķĶā4øöĪ»ÓŚÉĻĆę¾§°ūÄŚ²æ£¬¹ŹAĄė×ÓµÄÅäĪ»ŹżĪŖ8£¬øĆ¾§ĢåŹōÓŚĄė×Ó¾§Ģ壬
¹Ź“š°øĪŖ£ŗNa2O£»8£»Ąė×Ó¾§Ģ壻
£Ø5£©¾§°ūµÄ±ß³¤ĪŖa pm£¬Ōņ¾§°ūµÄĢå»żĪŖ£Øa”Į10-10£©3cm3£¬¾§°ūÖŠNaŌ×ÓŹżÄæĪŖ8£¬OĄė×ÓŹżÄæĪŖ8”Į$\frac{1}{8}$+6”Į$\frac{1}{2}$=4£¬ĖłŅŌ¾§°ūµÄĆܶČĪŖ$\frac{\frac{23”Į8+16”Į4}{{N}_{A}}}{£Øa”Į1{0}^{-10}£©^{3}}$g/cm3=$\frac{4”Į62}{£Øa”Į1{0}^{-10}£©^{3}{N}_{A}}$g/cm3£¬
¹Ź“š°øĪŖ£ŗ$\frac{4”Į62}{£Øa”Į1{0}^{-10}£©^{3}{N}_{A}}$£®
µćĘĄ ±¾ĢāŹĒ¶ŌĪļÖŹ½į¹¹µÄ漲飬Éę¼°µēøŗŠŌ”¢ŗĖĶāµē×ÓÅŲ¼”¢Ī¢Į£½į¹¹”¢ŌӻƹģµĄ”¢¾§°ū¼ĘĖćµČ£¬ŅŖѧ»įÓĆ¾łĢƷؽųŠŠ¾§°ūµÄ¼ĘĖć£¬ĢāÄæÄѶČÖŠµČ£®



| Äź¼¶ | øßÖŠæĪ³Ģ | Äź¼¶ | ³õÖŠæĪ³Ģ |
| øßŅ» | øßŅ»Ćā·ŃæĪ³ĢĶĘ¼ö£” | ³õŅ» | ³õŅ»Ćā·ŃæĪ³ĢĶĘ¼ö£” |
| ø߶ž | ø߶žĆā·ŃæĪ³ĢĶĘ¼ö£” | ³õ¶ž | ³õ¶žĆā·ŃæĪ³ĢĶĘ¼ö£” |
| øßČż | øßČżĆā·ŃæĪ³ĢĶĘ¼ö£” | ³õČż | ³õČżĆā·ŃæĪ³ĢĶĘ¼ö£” |
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗŃ”ŌńĢā
| A£® | ÓĆ½šŹōÄĘæÉĒų·ÖŅŅ“¼ŗĶŅŅĆŃ | |
| B£® | ÓĆøßĆĢĖį¼ŲĖįŠŌČÜŅŗæÉĒų·Ö¼ŗĶéŗĶ3-¼ŗĻ© | |
| C£® | ÓĆĖ®æÉĒų·Ö±½ŗĶäå±½ | |
| D£® | ÓĆäåĖ®»ņĖįŠŌøßĆĢĖį¼ŲČÜŅŗæÉŅŌ¼ų±š1-¼ŗĻ©ŗĶŅŅČ© |
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗŃ”ŌńĢā
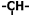 £©£¬²¢ĒŅŅŅĻ©»łŗĶ“Ī¼×»łÖ®¼ä±ŲŠėĶعżŃĒ¼×»łĻąĮ¬£¬µ±øĆĢžŗ¬ÓŠµ„»·½į¹¹ŹĒ·Ö×ÓÖŠµÄŅŅĻ©»łŗĶŃĒ¼×»łµÄøöŹżŅĄ“ĪĪŖ£Ø””””£©
£©£¬²¢ĒŅŅŅĻ©»łŗĶ“Ī¼×»łÖ®¼ä±ŲŠėĶعżŃĒ¼×»łĻąĮ¬£¬µ±øĆĢžŗ¬ÓŠµ„»·½į¹¹ŹĒ·Ö×ÓÖŠµÄŅŅĻ©»łŗĶŃĒ¼×»łµÄøöŹżŅĄ“ĪĪŖ£Ø””””£©| A£® | 2øö£¬3øö | B£® | 5øö£¬3øö | C£® | 4øö£¬6øö | D£® | 3øö£¬6øö |
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ½ā“šĢā
 £©ŹĒŅ»ÖÖÕņĶ“ŗĶĀé×ķŅ©Īļ£¬æÉÓÉ»ÆŗĻĪļB£Ø
£©ŹĒŅ»ÖÖÕņĶ“ŗĶĀé×ķŅ©Īļ£¬æÉÓÉ»ÆŗĻĪļB£Ø £©ĶعżŅŌĻĀĀ·ĻßŗĻ³ÉµĆµ½£®
£©ĶعżŅŌĻĀĀ·ĻßŗĻ³ÉµĆµ½£®
 £®
£® +HBr+CH3Br£®
+HBr+CH3Br£® µČ£®
µČ£® ĖłŹ¾£©µÄŗĻ³ÉĀ·ĻßĮ÷³ĢĶ¼£ØĪŽ»śŹŌ¼ĮČĪŃ”£©£®
ĖłŹ¾£©µÄŗĻ³ÉĀ·ĻßĮ÷³ĢĶ¼£ØĪŽ»śŹŌ¼ĮČĪŃ”£©£®
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ½ā“šĢā
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗŃ”ŌńĢā
| A£® | ÓÉ${\;}_{1}^{2}$HŗĶ${\;}_{8}^{18}$OĖł×é³ÉµÄ11gĖ®ÖŠĖłŗ¬ÖŠ×ÓŹżĪŖ6NA | |
| B£® | H2OŗĶD2O»„³ĘĪŖĶ¬ĖŲŅģŠĪĢ壬ĒŅĮ½ÕߵĻÆѧŠŌÖŹĻąĖĘ | |
| C£® | ${\;}_{8}^{18}$O2ŗĶ${\;}_{8}^{16}$O3»„³ĘĪŖĶ¬Ī»ĖŲ | |
| D£® | ½šøÕŹÆŗĶŹÆÄ«»„ĪŖĶ¬ĖŲŅģŠĪĢ壬Į½ÕßÖ®¼äµÄ×Ŗ»ÆŹōÓŚĪļĄķ±ä»Æ |
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ½ā“šĢā
| ŹµŃé ²½Öč | ŹµŃé²Ł×÷ | Ō¤ĘŚĻÖĻó¼°½įĀŪ £Ø²½Öč1Ö»Š“ĻÖĻó£© |
| 1 | ŌŚA”¢BĮ½Ö§½ą¾»µÄŹŌ¹ÜÖŠø÷¼ÓČė1mL 2%µÄAgNO3ČÜŅŗ£¬Č»ŗó±ßÕńµ“ŹŌ¹Ü±ßÖšµĪµĪČė2%Ļ”°±Ė®£¬ ÖĮ³ĮµķĒ”ŗĆČܽā£¬“ĖŹ±ÖʵĆpH¾łŌ¼ĪŖ8µÄŅų°±ČÜŅŗ£® | ĻČÉś³É°×É«³Įµķ£¬ŗó³ĮµķČܽā£® |
| 2 | ĶłA”¢BŹŌ¹Ü¼ÓČė3µĪŅŅČ©£¬Č»ŗóŌŚAŹŌ¹ÜÖŠ¼Ó1µĪNaOHČÜŅŗ£»Õńµ“ŗó½«Į½Ö§ŹŌ¹Ü·ÅŌŚČČĖ®Ō”ÖŠĪĀČČ£® | ČōAŹŌ¹Ü±ČBŹŌ¹Ü³öĻÖµÄŅų¾µŹ±¼ä¶Ģ”¢¹āĮĮ£¬ŌņŌņČÜŅŗpH“󣬷“Ó¦ĖŁĀŹæģ£» ČōAŹŌ¹Ü±ČBŹŌ¹Ü³öĻÖµÄŅų¾µŹ±¼ä³¤£¬ŌņŌņČÜŅŗpH“󣬷“Ó¦ĖŁĀŹĀż£® |
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ½ā“šĢā
| ·“Ó¦Īļ | “߻ƼĮ | ĪĀ¶Č | |
| ¢Ł | 10mL10% H2O2ČÜŅŗ | ĪŽ | 25”ę |
| ¢Ś | 10mL20% H2O2ČÜŅŗ | ĪŽ | 25”ę |
| ¢Ū | 10mL20% H2O2ČÜŅŗ | ĪŽ | 40”ę |
| ¢Ü | 10mL20% H2O2ČÜŅŗ | 1”«2µĪ0.1mol/LFeCl3ČÜŅŗ | 40”ę |

²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ½ā“šĢā
²éæ““š°øŗĶ½āĪö>>
°Ł¶ČÖĀŠÅ - Į·Ļ°²įĮŠ±ķ - ŹŌĢāĮŠ±ķ
ŗž±±Ź”»„ĮŖĶųĪ„·ØŗĶ²»Į¼ŠÅĻ¢¾Ł±ØĘ½ĢØ | ĶųÉĻÓŠŗ¦ŠÅĻ¢¾Ł±Ø×ØĒų | µēŠÅÕ©Ę¾Ł±Ø×ØĒų | É꥜Ź·ŠéĪŽÖ÷ŅåÓŠŗ¦ŠÅĻ¢¾Ł±Ø×ØĒų | ÉęĘóĒÖČؾŁ±Ø×ØĒų
Ī„·ØŗĶ²»Į¼ŠÅĻ¢¾Ł±Øµē»°£ŗ027-86699610 ¾Ł±ØÓŹĻä£ŗ58377363@163.com