
工业上常用可逆反应SO2+O2 2SO3 △H<0,制备硫酸,下列说法正确的是
2SO3 △H<0,制备硫酸,下列说法正确的是
A.增大压强,平衡向逆反应方向移动
B.升高温度,平衡向正反应方向移动
C.当v(SO2): v(O2): v(SO3)=2:1:2时,反应达到平衡状态
D.当单位时间内生成2 mol SO2的同时生成2 mol SO3,说明该反应达到平衡状态
科目:高中化学 来源: 题型:
A元素原子的M层上有6个电子。B元素与A元素原子核外电子层数相同,B元素原子的最外层上只有1个电子。
(1)A、B元素形成的化合物的名称是________。
(2)A离子的结构示意图为________________________________________________________________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
乙醇是生活中常见的有机物,能进行如下图所示的多种反应,A、C都是有机物。
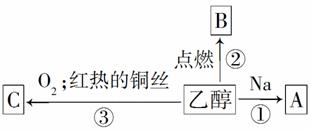
写出下列反应的化学方程式。
反应①:________________________________________________________________________;
反应②:________________________________________________________________________;
反应③:________________________________________________________________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
在元素周期表短周期元素中,A元素原子的最外层电子数是其电子层数的3倍;B元素的单质与A元素的单质化合生成化合物B2A2淡黄色固体;C元素的阳离子与A元素的阴离子电子层结构相同,0.1 mol C单质与足量盐酸反应,生成的H2在标况下体积为3.36 L;D元素与C元素同周期,D是该周期中非金属性最弱的非金属元素。
(1)各元素的符号是A________、B________、C________、D________。
(2)B元素的单质与A元素的单质化合生成化合物B2A2的化学方程式为____________________________________________。
(3)C的最高价氧化物对应水化物与NaOH溶液反应的化学方程式为________________________。
(4)D的原子结构示意图为________;气态氢化物分子式为________。
(5)物质的量相同的C和D分别与足量的强碱溶液反应生成气体的物质的量之比是________。
查看答案和解析>>
科目:高中化学 来源: 题型:
X、Y、Z和W代表原子序数依次增大的四种短周期元素,它们满足以下条件:
①元素周期表中Z与Y相邻,Z与W也相邻;
②Y、Z和W三种元素的原子最外层电子数之和为17。
请填空:
(1)Y、Z和W三种元素是否位于同一周期(填“是”或“否”):________,理由是______________________________。
(2)Y是________,Z是________,W是________。
(3)X、Y、Z和W可组成一化合物,其原子个数之比为8:2:4:1。写出该化合物的名称及化学式______________,____________。
查看答案和解析>>
科目:高中化学 来源: 题型:
臭氧是理想的烟气脱硝试剂,其脱硝反应为:2NO2(g)+O3(g) N2O5(g)+O2(g),
N2O5(g)+O2(g),
若反应在恒容密闭容器中进行,下列对该反应相关图像作出的判断正确的是( )
| A | B | C | D |
|
|
|
|
|
| 升高温度,平衡常数减小 | 0~3s内,反应速率为: v(NO2)=0.2mol·L-1 | t1时仅加入催化剂, 平衡正向移动 | 达平衡时,仅改变x, 则x为c(O2) |
查看答案和解析>>
科目:高中化学 来源: 题型:
(1)对于下列6种溶液:A.NH4Cl溶液 B.NaCl溶液 C.Na2S溶液
D.NaHCO3溶液 E.Na2CO3溶液 F.AlCl3溶液 , 其中(填写序号)
① 溶液呈酸性的是 ; ② 加热蒸干能得到原溶质固体的是 ;
③ 能用作泡沫灭火剂的是 ,两溶液混合后的离子方程式为 。
(2)下列事实能说明醋酸是弱酸的是
① 醋酸不易腐蚀衣服。 ② 0.1mol.L-1的CH3COONa溶液的pH>7。
③ 进行中和滴定时,等体积等物质的量浓度的H2SO4溶液比等体积等物质的量浓度的CH3COOH溶液消耗的NaOH溶液多。
④.0.1mol.L-1的CH3COOH溶液的pH约为2.9。
查看答案和解析>>
科目:高中化学 来源: 题型:
汕头市工商局查获400g袋装中老年补钙营养奶粉1401包。这种奶粉被鉴定为所含亚硝酸钠残留量高出正常值7.8倍,长期食用可能致癌。NaNO2有像食盐一样的咸味。已知NaNO2能发生如下反应:2NaNO2 + 4HI = 2NO + I2 + 2NaI + 2H2O 。
(1)上述反应中氧化剂是 ,若有0.75mol的还原剂被氧化,则被还原的氧化剂是 mol
(2)根据上述反应,可以用试纸和生活中常见的物质进行实验,以鉴别NaNO2和NaCl,可选用的物质有:
①自来水 ②碘化钾淀粉试纸 ③淀粉 ④白糖 ⑤食醋 ⑥白酒。进行实验时,必须选用的物质有 (填序号)。
(3)某厂废切削液中,含2% ~ 5%的NaNO2 ,直接排放会造成污染,下列试剂
(填序号)能使NaNO2 转化为不引起二次污染的N2。
①NaCl ②NH4Cl ③H2O2 ④浓硫酸
查看答案和解析>>
科目:高中化学 来源: 题型:
钢铁很容易生锈而被腐蚀,每年因腐蚀而损失的钢铁占世界钢铁年产量的四分之一。
(1)钢铁腐蚀主要是吸氧腐蚀,该腐蚀过程中的电极反应式为:__________________________________________________________
_________________________________________________________。
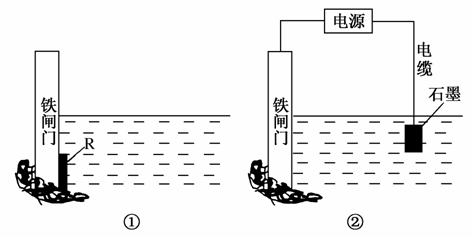
(2)为了降低某水库的铁闸门被腐蚀的速率,可以采用图①所示的方案,其中焊接在铁闸门上的固体材料R可以采用________。
A.铜 B.钠
C.锌 D.石墨
(3)图②所示的方案也可以降低铁闸门的腐蚀速率,其中铁闸门应该连接在直流电源的__________极。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com