
| A. | 仅含有碳、氢元素的有机物叫烃 | B. | 甲烷是最简单的有机物 | ||
| C. | 乙烷、丙烷均不存在同分异构体 | D. | 含碳元素的物质都是有机物 |
分析 A.烃是仅由碳和氢两种元素组成的有机化合物;
B.最简单的有机物是甲烷;
C.烷烃中碳原子数目≤3的烷烃不存在同分异构体现象;
D.含碳元素的物质不都是有机物,如二氧化碳、碳酸钙中都含有碳元素,但是这些物质的性质和无机物相似,把它们归入无机物.
解答 解:A.烃的定义为仅含有碳、氢元素的有机物,故A正确;
B.甲烷是最简单的有机物,故B正确;
C.CH4、C2H6、C3H8都无同分异构体,从丁烷开始才出现同分异构体,C4H10既可表示正丁烷,也可表示异丁烷,故C正确;
D.有机物是指含有碳元素的化合物.无机物是指不含有碳元素的化合物.一氧化碳、二氧化碳、碳酸盐等物质中虽然含有碳元素,但是这些物质的性质和无机物相似,把它们归入无机物,故D错误;
故选D.
点评 本题看考查了烃类物质的元素组成和性质,题目难度不大,注意烷烃同分异构体.


科目:高中化学 来源: 题型:选择题
| A. | NH4CO3 $\frac{\underline{\;\;△\;\;}}{\;}$NH3↑+H2O↑+CO2↑ | B. | 2Na2O2+2 H2O═4NaOH+O2↑ | ||
| C. | H2O+Cl2?HCl+HClO | D. | NH3+SO2+H2O═NH4HSO3 |
查看答案和解析>>
科目:高中化学 来源: 题型:填空题
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
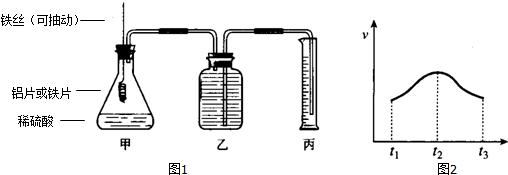
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 侯氏制碱法的工艺过程中应用了物质溶解度的差异 | |
| B. | 可用蘸浓硝酸的玻璃棒检验氨气是否已收集满 | |
| C. | 碘是人体必须微量元素,所以要多吃富含高碘酸的食物 | |
| D. | 黑火药由硫磺、硝石、木炭三种物质按一定比例混合制成 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
 已知反应:X(g)+2Y(g)?2Z(g),将X和Y气体按体积比1:2混合于一密闭容器中,并加压到3×107Pa时达到平衡状态,此时反应物、生成物的物质的量之比为6:1,则如右图所示,此时反应对应的温度为( )
已知反应:X(g)+2Y(g)?2Z(g),将X和Y气体按体积比1:2混合于一密闭容器中,并加压到3×107Pa时达到平衡状态,此时反应物、生成物的物质的量之比为6:1,则如右图所示,此时反应对应的温度为( )| A. | 100℃ | B. | 200℃ | C. | 300℃ | D. | 400℃ |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:填空题
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com