
 新非凡教辅冲刺100分系列答案
新非凡教辅冲刺100分系列答案科目:高中化学 来源: 题型:选择题

| A. | 该电池放电时,图中电极a是正极,c是负极 | |
| B. | 该电池放电时,水性电解质pH不变 | |
| C. | 当给该锂-空气电池充电时,c极应接电源的负极 | |
| D. | 当给该锂-空气电池充电时,b极的电极反应式为4OH--4e-=2H2O+O2↑ |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:填空题
| 同位素 | 同位素的质量分数 | 原子百分比 |
| 103A | 103 | 20% |
| 105A | 105 | 80% |
查看答案和解析>>
科目:高中化学 来源: 题型:填空题
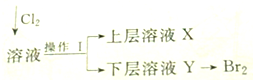 实验室用含有Ca2+、Mg2+、Cl-、SO42-、Br-等离子的溶液进行有关实验.已知:Cl2+2Br-=Br2+2Cl-.
实验室用含有Ca2+、Mg2+、Cl-、SO42-、Br-等离子的溶液进行有关实验.已知:Cl2+2Br-=Br2+2Cl-.查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 1mol任何物质都含有约6.02×1023个原子 | |
| B. | 0.012kg 12C约含有6.02×1023个碳原子 | |
| C. | 使用物质的量时,应指明粒子的种类 | |
| D. | 1mol H2的质量是2g |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 10g 甲烷所含有的分子数目为NA | |
| B. | 4g 氦气所含有的原子数目为2NA | |
| C. | 1mol 铝原子含有的电子数目为13NA | |
| D. | 电解水若产生2g 氢气,则产生的氧气分子数目为NA |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com