
| 温度/℃ | 700 | 800 | 830 | 1000 | 1200 |
| 平衡常数 | 1.7 | 1.1 | 1.0 | 0.6 | 0.4 |
分析 (1)平衡常数是平衡时生成物浓度幂之积比上反应物浓度幂之积;温度越高平衡常数越小,所以正反应是放热反应;
(2)根据△c=v△t计算△c(A),A的起始浓度-△c(A)=6s时c(A);
根据△n=△cV计算△n(A),再根据方程式计算C的物质的量;
(3)设平衡时A的浓度变化量为x,利用三段式表示平衡时各组分的平衡浓度,代入平衡常数列方程计算x的值,再根据转化率定义计算;保持温度、容器不变,再向密闭容器中充入0.20mol的A和0.80mol的B,相当于给原平衡体系加压,所以此时A的转化率不变;体积不变,充入1mol氩气,反应混合物各组分的浓度不变,变化不移动,A的转化率不变;
(4)根据化学平衡状态的特征解答,当反应达到平衡状态时,正逆反应速率相等,各物质的浓度、百分含量不变,以及由此衍生的一些量也不发生变化,解题时要注意,选择判断的物理量,随着反应的进行发生变化,当该物理量由变化到定值时,说明可逆反应到达平衡状态;
(5)同一反应在相同温度下,正、逆反应方向的平衡常数互为倒数.
解答 解:(1)已知A(g)+B(g)?C(g)+D(g)反应,平衡常数K=$\frac{c(C)•c(D)}{c(A)•c(B)}$;由表可知温度越高平衡常数越小,所以△H<0,故答案为:K=$\frac{c(C)•c(D)}{c(A)•c(B)}$;<;
(2)反应初始6s内A的平均反应速率v(A)=0.002mol•L-1•s-1,则6s内△c(A)=0.002mol•L-1•s-1×6s=0.012mol/L,A的起始浓度为$\frac{0.2mol}{5L}$=0.04mol/L,故6s时时c(A)=0.04mol/L-0.012mol/L=0.028mol/L,
故6s内△n(A)=0.012mol/L×5L=0.06mol,由方程式可知n(C)=△n(A)=0.06mol,故答案为:0.028;0.06;
(3)设平衡时A的浓度变化量为x,则:
A(g)+B(g)?C(g)+D(g)
开始(mol/L):0.04 0.16 0 0
变化(mol/L):x x x x
平衡(mol/L):0.04-x 0.16-x x x
故$\frac{{x}^{2}}{(0.04-x)(0.16-x)}$=1,解得x=0.032
所以平衡时A的转化率为$\frac{0.032mol/L}{0.04mol/L}$×100%=80%,
保持温度、容器不变,再向密闭容器中充入0.20mol的A和0.80mol的B,相当于给原平衡体系加压,所以此时A的转化率不变,仍为80%,
体积不变,充入1mol氩气,反应混合物各组分的浓度不变,变化不移动,A的转化率不变为80%,
故答案为:80%;80%;不变;
(4)a.该反应前后气体的物质的量不变,压强始终不变,故压强不随时间改变,不能说明到达平衡,故a错误,
b.混合气体的总质量不变,容器的容积不变,故混合气体的密度始终不变,故气体的密度不随时间改变,不能说明到达平衡,故b错误,
c.可逆反应到达平衡时,各组分的浓度不发生变化,故c(A)不随时间改变,说明到达平衡,故c正确,
d.单位时间里生成C和D的物质的量相等,都表示正反应速率,反应始终按1:1生成C、D的物质的量,不能说明到达平衡,故d错误,
e.单位时间内生成amolA等效于生成amolB的同时消耗amolB,达平衡状态,故e正确;
故答案为:ce;
(5)同一反应在相同温度下,正、逆反应方向的平衡常数互为倒数,故1200℃时反应C(g)+D(g)?A(g)+B(g)的平衡常数的值为$\frac{1}{0.4}$=2.5,
故答案为:2.5.
点评 本题考查化学平衡计算、平衡常数计算、化学反应速率、平衡状态判断,难度中等,注意化学平衡状态判断,选择判断的物理量,随着反应的进行发生变化,当该物理量由变化到定值时,说明可逆反应到达平衡状态.


科目:高中化学 来源: 题型:选择题
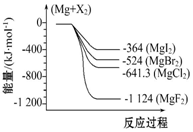 如图是金属镁和卤素反应的能量变化图(反应物和生成物均为298K时的稳定状态).下列选项中不正确的是( )
如图是金属镁和卤素反应的能量变化图(反应物和生成物均为298K时的稳定状态).下列选项中不正确的是( )| A. | Mg与F2反应放热最多 | |
| B. | MgF2(s)+Br2(l)═MgBr2(s)+F2(g)吸热 | |
| C. | MgBr2与Cl2反应放热 | |
| D. | 化合物的热稳定顺序:MgI2>MgBr2>MgCl2>MgF2 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 苯中含有少量甲苯 | B. | 乙醇中含有少量乙酸 | ||
| C. | 溴苯中含有少量苯 | D. | 乙酸乙酯中含有少量乙酸 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 反应C(s)+H2O(g)═CO(g)+H2(g)的△H>0,△S>0 | |
| B. | 铅酸蓄电池放电时,负极质量减少,正极质量增加 | |
| C. | 向Na2S溶液中加入少量NaOH固体后,溶液中c(Na+)/c(S2- )减少 | |
| D. | 向平衡体系CH3COOH+C2H5OH?CH3COOC2H5+H2O中,加少量浓硫酸,乙酸转化率不变 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
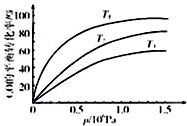 铁及其化合物在日常生活、生产中应用广泛,研究铁及其化合物的应用意义重大.回答下列问题:
铁及其化合物在日常生活、生产中应用广泛,研究铁及其化合物的应用意义重大.回答下列问题:| 温度 | 250℃ | 600℃ | 1000℃ | 2000℃ |
| 主要成分 | Fe2O3 | Fe3O4 | FeO | Fe |
| t/min | 0 | 10 | 20 | 30 | 40 | 50 |
| x(CO) | 0.25 | 0.23 | 0.214 | 0.202 | 0.193 | 0.193 |
查看答案和解析>>
科目:高中化学 来源: 题型:实验题
| 选用试剂 | 实验现象 | |
| 方案 | ①d或b | ②溶液变成血红色或下层的四氯化碳溶液依然无色 |
查看答案和解析>>
科目:高中化学 来源: 题型:推断题
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
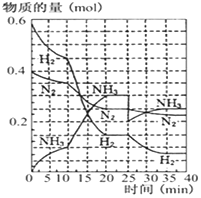 德国人发明了合成氨反应,其原理为:N2(g)+3H2(g)?2NH3(g);已知298K时,△H=-92.4kJ•mol-1,在500℃,20Mpa时,将氮气和氢气通入到体积为2升的密闭容器中,反应过程中各种物质的量变化如右图所示.
德国人发明了合成氨反应,其原理为:N2(g)+3H2(g)?2NH3(g);已知298K时,△H=-92.4kJ•mol-1,在500℃,20Mpa时,将氮气和氢气通入到体积为2升的密闭容器中,反应过程中各种物质的量变化如右图所示.查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com