
A、 |
B、 |
C、 |
D、 |


 挑战100单元检测试卷系列答案
挑战100单元检测试卷系列答案科目:高中化学 来源: 题型:

| 烃 | CH4 | CH3CH3 | CH3(CH2)2CH3 | 硝基苯酚 |  |  | 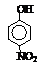 |
| 沸点/℃ | -164 | -88.6 | -0.5 | 熔点/℃ | 45 | 96 | 114 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、含有离子键的化合物一定是离子化合物 |
| B、含有共价键的化合物一定是共价化合物 |
| C、共价化合物中一定含有极性共价键,肯定不含离子键 |
| D、离子化合物一定含有离子键,可能含有共价键. |
查看答案和解析>>
科目:高中化学 来源: 题型:
| 选项 | 实验操作 | 现象 | 结论 | ||
| A | ①向溶液中通入CO2②继续通入CO2浑浊至过量 | ①溶液变浑浊②浑浊不消失 | 原溶液一定是NaAlO2溶液 | ||
| B | ①想溶液中加入KSCN溶液②滴入一定量盐酸 | ①溶液无明显现象②溶液变为血红色 | 原溶液中可能含有Fe2+NO
| ||
| C | 用洁净帕丝蘸取少量溶液进行焰色反应 | 火焰呈黄色 | 原溶液一定是钠盐溶液 | ||
| D | 溶液中加入盐酸 | 产生的气体使澄清石灰水变浑浊 | 原溶液中一定含有CO
|
| A、A | B、B | C、C | D、D |
查看答案和解析>>
科目:高中化学 来源: 题型:
A、
| ||
B、
| ||
C、
| ||
D、
|
查看答案和解析>>
科目:高中化学 来源: 题型:

| A、将集有氨气的试管倒扣于水槽中,液体迅速充满试管,说明氨气极易溶于水 |
| B、将pH=11的氨水稀释1000倍,测得pH>8,说明NH3?H2O为弱碱 |
| C、加热NH4HCO3固体,观察到固体逐渐减少,试管口有液滴产生,说明NH4HCO3受热不稳定 |
| D、将红热的Pt丝伸入右图所示的锥形瓶中,瓶口出现少量红棕色气体,说明氨气的氧化产物为NO2 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| 酸 | 电离常数 |
| 碳酸 | Ki1=4×10-7 Ki2=5.6×10-11 |
| 亚硫酸 | Ki1=1.54×10-2 Ki2=1.02×10-7 |
| A、SO32-、HCO3- |
| B、HSO3-、CO32- |
| C、SO32-、CO32- |
| D、HSO3-、HCO3- |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com