
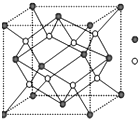
 A-IĪŖŌ×ÓŠņŹżµŻŌöµÄĒ°4ÖÜĘŚµÄŌŖĖŲ£¬ŅŃÖŖAŌ×ÓµÄ×īĶā²ćµē×ÓŹĒ“ĪĶā²ćµē×ÓŹżµÄ2±¶£¬DĪŖÖÜĘŚ±ķÖŠµēøŗŠŌ×ī“óµÄŌŖĖŲ£¬FÓėCĪ»ÓŚĶ¬Ņ»Ö÷×壬EÓėGŌŚÖÜĘŚ±ķµÄĪ»ÖĆŹĒÉĻĻĀĻąĮ¬£¬Į½ŌŖĖŲĖłŌŚÖ÷×åÖŠĖłÓŠŌŖĖŲ¶¼ŹĒ½šŹō£¬HĪŖÓ¦ÓĆ×ī¹ć·ŗµÄ½šŹō£»I“¦ÓŚÖÜĘŚ±ķÖŠµÄµŚ¶žø±×壮Ēė»Ų“šĻĀĮŠĪŹĢā£ŗ£ØŅŌĻĀĪŹĢāÖŠµÄĖłÓŠŌ×Ó¶¼±ŲŠėŌŚÉĻŹöŌŖĖŲÖŠŃ°ÕŅ£©
A-IĪŖŌ×ÓŠņŹżµŻŌöµÄĒ°4ÖÜĘŚµÄŌŖĖŲ£¬ŅŃÖŖAŌ×ÓµÄ×īĶā²ćµē×ÓŹĒ“ĪĶā²ćµē×ÓŹżµÄ2±¶£¬DĪŖÖÜĘŚ±ķÖŠµēøŗŠŌ×ī“óµÄŌŖĖŲ£¬FÓėCĪ»ÓŚĶ¬Ņ»Ö÷×壬EÓėGŌŚÖÜĘŚ±ķµÄĪ»ÖĆŹĒÉĻĻĀĻąĮ¬£¬Į½ŌŖĖŲĖłŌŚÖ÷×åÖŠĖłÓŠŌŖĖŲ¶¼ŹĒ½šŹō£¬HĪŖÓ¦ÓĆ×ī¹ć·ŗµÄ½šŹō£»I“¦ÓŚÖÜĘŚ±ķÖŠµÄµŚ¶žø±×壮Ēė»Ų“šĻĀĮŠĪŹĢā£ŗ£ØŅŌĻĀĪŹĢāÖŠµÄĖłÓŠŌ×Ó¶¼±ŲŠėŌŚÉĻŹöŌŖĖŲÖŠŃ°ÕŅ£©·ÖĪö A-IĪŖŌ×ÓŠņŹżµŻŌöµÄĒ°4ÖÜĘŚµÄŌŖĖŲ£¬ŅŃÖŖAŌ×ÓµÄ×īĶā²ćµē×ÓŹĒ“ĪĶā²ćµē×ÓŹżµÄ2±¶£¬ŌņAŌ×ÓÖ»ÄÜÓŠ2øöµē×Ó²ć£¬×īĶā²ćµē×ÓŹżĪŖ4£¬ŌņAĪŖĢ¼ŌŖĖŲ£»DĪŖÖÜĘŚ±ķÖŠµēøŗŠŌ×ī“óµÄŌŖĖŲ£¬ŌņDĪŖ·śŌŖĖŲ£»HĪŖÓ¦ÓĆ×ī¹ć·ŗµÄ½šŹō£¬ŌņHĪŖFe£»I“¦ÓŚÖÜĘŚ±ķÖŠµÄµŚ¶žø±×壬ŌņIĪŖZn£®EÓėGŌŚÖÜĘŚ±ķµÄĪ»ÖĆŹĒÉĻĻĀĻąĮ¬£¬Į½ŌŖĖŲĖłŌŚÖ÷×åÖŠĖłÓŠŌŖĖŲ¶¼ŹĒ½šŹō£¬½įŗĻŌ×ÓŠņŹżæÉÖŖ£¬“¦ÓŚ¢ņA×壬EĪŖMg”¢GĪŖCa£»½įŗĻŌ×ÓŠņŹżæÉÖŖ£¬BĪŖNŌŖĖŲ”¢CĪŖOŌŖĖŲ£»FÓėCĪ»ÓŚĶ¬Ņ»Ö÷×壬FµÄŌ×ÓŠņŹżŠ”ÓŚCa£¬ŌņFĪŖSŌŖĖŲ£¬¾Ż“Ė½ā“š£®
½ā“š ½ā£ŗA-IĪŖŌ×ÓŠņŹżµŻŌöµÄĒ°4ÖÜĘŚµÄŌŖĖŲ£¬ŅŃÖŖAŌ×ÓµÄ×īĶā²ćµē×ÓŹĒ“ĪĶā²ćµē×ÓŹżµÄ2±¶£¬ŌņAŌ×ÓÖ»ÄÜÓŠ2øöµē×Ó²ć£¬×īĶā²ćµē×ÓŹżĪŖ4£¬ŌņAĪŖĢ¼ŌŖĖŲ£»DĪŖÖÜĘŚ±ķÖŠµēøŗŠŌ×ī“óµÄŌŖĖŲ£¬ŌņDĪŖ·śŌŖĖŲ£»HĪŖÓ¦ÓĆ×ī¹ć·ŗµÄ½šŹō£¬ŌņHĪŖFe£»I“¦ÓŚÖÜĘŚ±ķÖŠµÄµŚ¶žø±×壬ŌņIĪŖZn£®EÓėGŌŚÖÜĘŚ±ķµÄĪ»ÖĆŹĒÉĻĻĀĻąĮ¬£¬Į½ŌŖĖŲĖłŌŚÖ÷×åÖŠĖłÓŠŌŖĖŲ¶¼ŹĒ½šŹō£¬½įŗĻŌ×ÓŠņŹżæÉÖŖ£¬“¦ÓŚ¢ņA×壬EĪŖMg”¢GĪŖCa£»½įŗĻŌ×ÓŠņŹżæÉÖŖ£¬BĪŖNŌŖĖŲ”¢CĪŖOŌŖĖŲ£»FÓėCĪ»ÓŚĶ¬Ņ»Ö÷×壬FµÄŌ×ÓŠņŹżŠ”ÓŚCa£¬ŌņFĪŖSŌŖĖŲ£¬
£Ø1£©Bµ„ÖŹĪŖN2£¬·Ö×ÓÖŠŠĪ³ÉN”ŌNČż¼ü£¬ŗ¬ÓŠ1øö¦Ņ¼ü”¢2øö¦Š¼ü£¬¦ŅÓė¦Š¼üŹżÄæ±ČĪŖ1£ŗ2£»Ķ¬ÖÜĘŚĖęŌ×ÓŠņŹżŌö“óµŚŅ»µēĄėÄܳŹŌö“óĒ÷ŹĘ£¬µ«NŌŖĖŲ2pÄܼ¶ĪŖ°ėĀśĪȶØדĢ¬£¬ÄÜĮæ½ĻµĶ£¬µŚŅ»µēĄėÄÜøßÓŚŃõŌŖĖŲ£¬¹ŹN”¢O”¢FµŚŅ»µēĄėÄÜÓÉŠ”µ½“óµÄĖ³ŠņĪŖO£¼N£¼F£¬
¹Ź“š°øĪŖ£ŗ1£ŗ2£»O£¼N£¼F£»
£Ø2£©HĪŖFeŌŖĖŲ£¬Ō×ӵļŪ²ćµē×ÓÅŲ¼Ź½ĪŖ3d64s2£¬Fe3+Ąė×ÓæÉŅŌÓėÉĻŹöŌŖĖŲÖŠµÄČżÖÖŠĪ³ÉµÄijŅõĄė×ÓÉś³ÉŃŖŗģÉ«ĀēŗĻĪļ£¬øĆŅõĄė×ÓĪŖSCN-£¬ÓÖÓėA-IŌŖĖŲÖŠµÄijŠ©Ō×ÓŠĪ³ÉµÄ·Ö×Ó»„ĪŖµČµē×ÓĢ壬µČµē×ÓĢåŗ¬ÓŠĻąĶ¬µÄŌ×ÓŹżÄæÓė¼Ūµē×Ó×ÜŹż£¬øĆ·Ö×ÓĪŖCO2µČ£¬¼Ūµē×Ó×ÜŹżĻąĶ¬µÄµČµē×ÓĢåæÕ¼ä½į¹¹ĻąĖĘ£¬¹ŹSCN-ÓėCO2µÄæÕ¼ä½į¹¹ĻąĖĘĪŖÖ±ĻߊĶ£¬
¹Ź“š°øĪŖ£ŗ3d64s2£»CO2µČ£»Ö±ĻߊĶ£»
£Ø3£©FÓėCaæÉŅŌŠĪ³ÉCaF2£¬Ę侧°ūÖŠŗŚÉ«ĒņŹżÄæ=8”Į$\frac{1}{8}$+6”Į$\frac{1}{2}$=4£¬°×É«ĒņŹżÄæ=8£¬¹ŹŗŚÉ«Ēņ“ś±ķCaŌŖĖŲ£¬Óɾ§°ū½į¹¹æÉÖŖ£¬Ó¦øĆFŌ×ÓÖÜĪ§ÓŠ4øöCaŌ×Ó£¬¼“FŌ×ÓÅäĪ»ŹżĪŖ4£¬ŌņøĆCaŌ×ÓŌŚøĆ¾§°ūÖŠµÄÅäĪ»ŹżĪŖ8£¬
¹Ź“š°øĪŖ£ŗCa£»8£»
£Ø4£©Čō½«ÉĻŹö¾§°ūŌ²Č¦¶ŌÓ¦µÄŌ×ÓĖłŌŚÉĻĻĀĮ½²ćĘ½ĆęŌ×Ó£¬°“Į½ĢõĻą»„“¹Ö±µÄ¶Ō½ĒĻßÉĻø÷Č„µōøĆŌ×Ó2øö£Ø¹²Č„µō4øö£©£¬ŌņŌ²Č¦ŹżÄæĪŖ4£¬ŗŚÉ«ĒņŹżÄæ=8”Į$\frac{1}{8}$+6”Į$\frac{1}{2}$=4£¬¾§°ūÖŠŌ×ÓŹżÄæĪŖ1£ŗ1£¬²¢½«Š”µćŗĶŌ²Č¦¶ŌÓ¦µÄŌŖĖŲøüøÄĪŖĮķĶāĮ½ÖÖŌŖĖŲ£¬·ūŗĻZnSµÄĮ¢·½½į¹¹£¬ŌņÕāøö¾§°ū»ÆѧŹ½ĪŖZnS£¬
ČōŌŁ½«ĮōĻĀµÄĖłÓŠŌ×Ó»»³ÉĮķĶāŅ»ÖÖŠĀŌŖĖŲµÄŌ×Ó£¬Ōņ³ÉĪŖĮķĶāŅ»ÖÖ¾§°ū£¬Óɾ§°ū½į¹¹£ØĄąĖĘ½šøÕŹÆ½į¹¹£©æÉÖŖ£¬ĆæøöŌ×ÓÖÜĪ§Į¬½Ó4øöŌ×Ó£¬ŠĪ³ÉÕżĖÄĆęĢåŠĶ£¬øĆ¾§°ūÖŠ³É¼üŌ×Ó¼ü½ĒĪŖ109”ć28”䣬
¹Ź“š°øĪŖ£ŗZnS£»109”ć28”䣻
£Ø5£©ŅŃÖŖ£¬Sµ„ÖŹ¾§ĢåµÄŌ×ӶѻżĪŖABABŠĶ£¬ĪŖĮł·½×īĆܶѻż£¬¾§°ūČēĶ¼£ŗ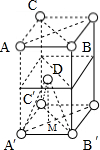 £¬
£¬
D”¢C”䔢A”䔢B”ä±Ė“ĖŌ×ÓĻąĮŚ£¬¹¹³ÉÕżĖÄĆęĢå½į¹¹£¬¾§°ūµÄø߶ČĪŖøĆÕżĖÄĆęĢåøßµÄ2±¶£¬Čē¹ūFµÄŌ×Ó°ė¾¶ĪŖR£¬ŌņDA”䳤ĪŖ2R£¬ÕżĖÄĆęĢåµÄøßDM£¬MĪŖÕżČż½ĒŠĪA”äB”äC”äµÄÖŠŠÄ£¬ŌņA”äMµÄ³¤ĪŖ $\frac{2}{3}$”Į£Ø2R”Į$\frac{\sqrt{3}}{2}$ £©=$\frac{2\sqrt{3}R}{3}$£¬ŌņDMµÄ³¤=$\sqrt{£Ø{2R£©}^{2}-£Ø\frac{2\sqrt{3}R}{3}£©^{2}}$=$\frac{2\sqrt{6}R}{3}$£¬¹Ź¾§°ūµÄø߶Č=2”Į$\frac{2\sqrt{6}R}{3}$=$\frac{4\sqrt{6}R}{3}$£»
S£Ø”÷A”äB”äC”䣩=$\frac{1}{2}$”Į2R”Į2R”Įsin60”ć=$\sqrt{3}$R2£¬¹Źµ×ĆęĆ껿ĪŖ2 $\sqrt{3}$R2£¬¾§°ūµÄĢå»ż=2 $\sqrt{3}$R2”Į$\frac{4\sqrt{6}R}{3}$=8 $\sqrt{2}$R3£¬¾§°ūÖŠŗ¬ÓŠŌ×ÓŹżÄæĪŖ1+8”Į$\frac{1}{8}$=2£¬¹ŹŌ×Ó×ÜĢå»ż=2”Į$\frac{4}{3}$”Į¦ŠR3£¬¹Ź¾§°ūæÕ¼äĄūÓĆĀŹ=$\frac{2”Į\frac{4}{3}¦Š{R}^{3}}{8\sqrt{2}{R}^{3}}$”Į100%=74.05%£»
Čē¹ūFµ„ÖŹµÄĦ¶ūÖŹĮæĪŖM£¬¾§°ūµÄÖŹĮæ=$\frac{2M}{N{\;}_{A}}$£¬¾§°ūĄā³¤ĪŖa£¬ŌņS£Ø”÷A”äB”äC”䣩=$\frac{1}{2}$”Įa”Įa”Įsin60”ć=$\frac{1}{2}$ a2sin60”ć£¬¹Źµ×ĆęĆ껿ĪŖa2sin60”ć£¬¾§°ūø߶ČĪŖc£¬Ōņ¾§°ūĢå»ż=ca2sin60”ć£¬¹Ź¾§ĢåĆܶČ=$\frac{\frac{2M}{N{\;}_{A}}}{ca{\;}^{2}sin60”ć}$=$\frac{2M}{N{\;}_{A}ca{\;}^{2}sin60”ć}$£¬
¹Ź“š°øĪŖ£ŗ74.05%£» $\frac{2M}{N{\;}_{A}ca{\;}^{2}sin60”ć}$£» $\frac{4\sqrt{6}R}{3}$£®
µćĘĄ ±¾Ģāæ¼²éĪļÖŹ½į¹¹ÓėŠŌÖŹ£¬Éę¼°ŗĖĶāµē×ÓÅŲ¼”¢µēĄėÄÜ”¢¾§°ū½į¹¹Óė¼ĘĖćµČ£¬ĢāÄæ¼ĘĖćĮæ“󣬶ŌѧɜµÄæÕ¼äĻėĻóÓėŹżŃ§¼ĘĖćÓŠ½ĻøßµÄŅŖĒ󣬣Ø4£©£Ø5£©ĪŖŅדķµć”¢ÄŃµć£¬Ąķ½ā¾§°ū½į¹¹ŹĒ¹Ų¼ü£¬ÄŃ¶Č½Ļ“ó£®


 ĢģĢģĻņÉĻŅ»±¾ŗĆ¾ķĻµĮŠ“š°ø
ĢģĢģĻņÉĻŅ»±¾ŗĆ¾ķĻµĮŠ“š°ø Š”ѧɜ10·ÖÖÓÓ¦ÓĆĢāĻµĮŠ“š°ø
Š”ѧɜ10·ÖÖÓÓ¦ÓĆĢāĻµĮŠ“š°ø
| Äź¼¶ | øßÖŠæĪ³Ģ | Äź¼¶ | ³õÖŠæĪ³Ģ |
| øßŅ» | øßŅ»Ćā·ŃæĪ³ĢĶĘ¼ö£” | ³õŅ» | ³õŅ»Ćā·ŃæĪ³ĢĶĘ¼ö£” |
| ø߶ž | ø߶žĆā·ŃæĪ³ĢĶĘ¼ö£” | ³õ¶ž | ³õ¶žĆā·ŃæĪ³ĢĶĘ¼ö£” |
| øßČż | øßČżĆā·ŃæĪ³ĢĶĘ¼ö£” | ³õČż | ³õČżĆā·ŃæĪ³ĢĶĘ¼ö£” |
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ½ā“šĢā
| Ąė×Ó | Cu2+ | H+ | Cl- | SO42- |
| ÅØ¶Č£Øc/mol•L-1£© | 0.5 | 2 | 2 | 0.5 |
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ½ā“šĢā
 ŅŃÖŖŹŅĪĀĻĀ£¬Ä³Š©ČõĖįµÄµēĄė³£ŹżČēĻĀ£ŗ
ŅŃÖŖŹŅĪĀĻĀ£¬Ä³Š©ČõĖįµÄµēĄė³£ŹżČēĻĀ£ŗ| CH3COOH | H2CO3 | HClO | |
| µēĄėĘ½ŗā³£Źż | 1.7”Į10-5 | Ka1=4.2£®”Į10-7 Ka2=5.6£®”Į10-11 | 3”Į10-8 |
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗŃ”ŌńĢā
| A£® | ĮņĖįĢś | B£® | ĮņĖįĶ | C£® | ĮņĖį | D£® | ĮņĖįŃĒĢś |
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ½ā“šĢā
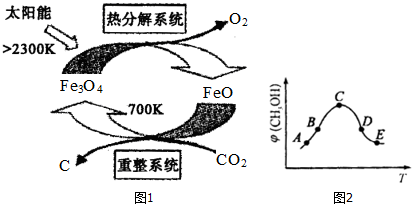
| ČŻĘ÷ | ¼× | ŅŅ |
| ·“Ó¦ĪļĶ¶ČėĮæ | 1molCO2”¢3molH2 | a molCO2”¢b molH2”¢c molCH3OH£Øg£©”¢c molH2O£Øg£© |
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗŃ”ŌńĢā
| A£® | NaHCO3 µÄĖ®ČÜŅŗ£ŗNaHCO3ØTNa++H++CO32- | |
| B£® | ČŪȌדĢ¬µÄNaHSO4£ŗNaHSO4ØTNa++HSO4- | |
| C£® | HFµÄĖ®ČÜŅŗ£ŗHFØTH++F- | |
| D£® | H2S µÄĖ®ČÜŅŗ£ŗH2S?2H++S2- |
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ½ā“šĢā
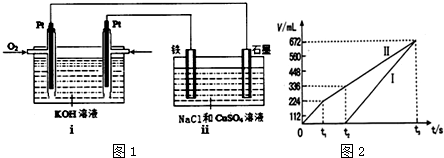
| »ÆŗĻĪļ | ¼× | ŅŅ | ±ū | ¶” |
| ×é³ÉŌŖĖŲ | B”¢C | A”¢C | A”¢D | C”¢D |
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ½ā“šĢā
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗŃ”ŌńĢā
| ŹµŃéÄæµÄ | ŹµŃé²Ł×÷ | |
| A | ³ĘČ”2.0gNaOH¹ĢĢå | ĻČŌŚĶŠÅĢÉĻø÷·ÅŅ»ÕÅĀĖÖ½£¬Č»ŗóŌŚÓŅÅĢÉĻĢķ¼Ó2gķĄĀė£¬×óÅĢÉĻĢķ¼ÓNaOH¹ĢĢå |
| B | ÖʱøFe£ØOH£©3½ŗĢå | ĻņĀČ»ÆĢś±„ŗĶČÜŅŗÖŠÖšµĪ¼ÓČėÉŁĮæNaOHČÜŅŗ£¬¼ÓČČÖó·ŠÖĮŅŗĢå±äĪŖŗģŗÖÉ« |
| C | Ö¤Ć÷Ģ¼ĖįµÄĖįŠŌĒæÓŚ¹čĖį | CO2ĶØČėNa2SiO3ČÜŅŗÖŠ£¬Īö³ö¹čĖį½ŗĢå |
| D | ŻĶČ”µāĖ®ÖŠµÄµā | ½«µāĖ®µ¹Čė·ÖŅŗĀ©¶·£¬Č»ŗóŌŁ×¢Čė¾Ę¾«£¬Õńµ“£¬¾²ÖĆ·Ö²ćŗó£¬ĻĀ²ćŅŗĢå“ÓĻĀæŚ·Å³ö£¬ÉĻ²ćŅŗĢå“ÓÉĻæŚµ¹³ö |
| A£® | A | B£® | B | C£® | C | D£® | D |
²éæ““š°øŗĶ½āĪö>>
°Ł¶ČÖĀŠÅ - Į·Ļ°²įĮŠ±ķ - ŹŌĢāĮŠ±ķ
ŗž±±Ź”»„ĮŖĶųĪ„·ØŗĶ²»Į¼ŠÅĻ¢¾Ł±ØĘ½ĢØ | ĶųÉĻÓŠŗ¦ŠÅĻ¢¾Ł±Ø×ØĒų | µēŠÅÕ©Ę¾Ł±Ø×ØĒų | É꥜Ź·ŠéĪŽÖ÷ŅåÓŠŗ¦ŠÅĻ¢¾Ł±Ø×ØĒų | ÉęĘóĒÖČؾŁ±Ø×ØĒų
Ī„·ØŗĶ²»Į¼ŠÅĻ¢¾Ł±Øµē»°£ŗ027-86699610 ¾Ł±ØÓŹĻä£ŗ58377363@163.com