

| A£® | ĻõĖįļ§”¢Ēč»ÆÄĘ”¢µēŹÆŗĶ½šŹōÄĘ¾łŹōÓŚµē½āÖŹ | |
| B£® | CN-ÖŠCŌŖĖŲĻŌ+2¼Ū£¬NŌŖĖŲĻŌ-3¼Ū£¬Ōņ·Ē½šŹōŠŌN£¾C | |
| C£® | Ēč»ÆÄĘŹĒŅ»ÖÖÖŲŅŖµÄ»Æ¹¤ŌĮĻ£¬Ņ²ŹĒ¾ē¶¾Ī£ĻÕĘ·£¬Ę¤·ōÉĖæŚ½Ó“„”¢ĪüČė”¢ĶĢŹ³Ī¢ĮææÉÖŠ¶¾ĖĄĶö | |
| D£® | µēŹÆŹōÓŚĪ£»ÆĘ·ÖŠµÄÓöŹŖŅ×Č¼¹ĢĢ壬ŠčĢłÉĻÓŅĶ¼±źÖ¾£¬Ęä×Å»šŹ±²»ÄÜÓĆĖ®Ćš»š |
·ÖĪö A£®½šŹōµ„ÖŹ£¬¼Č²»ŹĒµē½āÖŹŅ²²»ŹĒ·Ēµē½āÖŹ£»
B£®·Ē½šŹōŠŌĒæµÄ£¬ŌŚ»ÆŗĻĪļÖŠĻŌŹ¾øŗ¼Ū£»
C£®Ēč»ÆÄĘŹĒŅ»ÖÖÓŠ¶¾µÄ»ÆŗĻĪļ£»
D£®µēŹÆÓėĖ®·“Ӧɜ³ÉŅŅČ²£¬¾Ż“Ė½ā“š¼“æÉ£®
½ā“š ½ā£ŗA£®NaŹĒ½šŹōµ„ÖŹ£¬¼Č²»ŹĒµē½āÖŹŅ²²»ŹĒ·Ēµē½āÖŹ£¬µē½āÖŹ±ŲŠėŹĒ»ÆŗĻĪļ£¬¹ŹA“ķĪó£»
B£®ÓÉÓŚNµÄ·Ē½šŹōŠŌĒæÓŚC£¬ĖłŅŌŌŚĒčĒāøłÖŠNĻŌŹ¾øŗ»ÆŗĻ¼Ū£¬¹ŹBÕżČ·£»
C£®Ēč»ÆÄĘŹĒŅ»ÖÖ¾ē¶¾µÄ»ÆŗĻĪļ£¬²»Äܽӓ„æŚ±Ē”¢Ę¤·ōµČ£¬¹ŹCÕżČ·£»
D£®µēŹÆŹĒÖĘČ”ŅŅČ²µÄ»ÆŗĻĪļ£¬ÓėĖ®·“Ó¦£¬¹ŹµēŹÆ×Å»š²»ÄÜÓĆĖ®ĘĖĆš£¬¹ŹDÕżČ·£¬¹ŹŃ”A£®
µćĘĄ ±¾ĢāÖ÷ŅŖæ¼²éµÄŹĒµē½āÖŹµÄøÅÄī”¢·Ē½šŹōŠŌĒæČõµÄ±Č½ĻµČ£¬ÄŃ¶Č²»“ó£¬ŹōÓŚ³£æ¼Ģā£®



| Äź¼¶ | øßÖŠæĪ³Ģ | Äź¼¶ | ³õÖŠæĪ³Ģ |
| øßŅ» | øßŅ»Ćā·ŃæĪ³ĢĶĘ¼ö£” | ³õŅ» | ³õŅ»Ćā·ŃæĪ³ĢĶĘ¼ö£” |
| ø߶ž | ø߶žĆā·ŃæĪ³ĢĶĘ¼ö£” | ³õ¶ž | ³õ¶žĆā·ŃæĪ³ĢĶĘ¼ö£” |
| øßČż | øßČżĆā·ŃæĪ³ĢĶĘ¼ö£” | ³õČż | ³õČżĆā·ŃæĪ³ĢĶĘ¼ö£” |
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗŃ”ŌńĢā
| A£® | ¼īŠŌ£ŗAl£ØOH£©3”¢Mg£ØOH£©2”¢NaOH | B£® | ĖįŠŌ£ŗHClO4”¢H2SO4”¢H3PO4 | ||
| C£® | »¹ŌŠŌ£ŗHCl”¢HBr”¢HI | D£® | Ō×Ó°ė¾¶£ŗS”¢Na”¢O |
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗŃ”ŌńĢā
| A£® | ¹żŃõ»ÆÄʵē×ÓŹ½£ŗ | |
| B£® | ÖŹ×ÓŹż35”¢ÖŠ×ÓŹż45µÄäåŌ×Ó£ŗ${\;}_{35}^{80}$Br | |
| C£® | ĮņĄė×Ó½į¹¹Ź¾ŅāĶ¼£ŗ | |
| D£® | HClOµÄ½į¹¹Ź½£ŗH-Cl-O |
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ½ā“šĢā

²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ½ā“šĢā
 £®
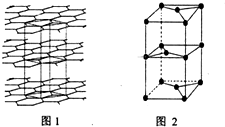
£®
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗŃ”ŌńĢā
| X | Y | ĻÖĻó | ×°ÖĆ | |
| A | ĀČĖ® | ŹÆČļ | ČÜŅŗĻȱäŗģŗóĶŹÉ« | 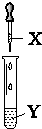 |
| B | °±Ė® | AgNO3ČÜŅŗ | ĻČ²śÉś³ĮµķŗóÖš½„Čܽā | |
| C | NaOHČÜŅŗ | AlCl3ČÜŅŗ | ²śÉś°×É«³ĮµķĒŅ²»ĻūŹ§ | |
| D | Ė«ŃõĖ® | ĖįŠŌµķ·ŪKIČÜŅŗ | ČÜŅŗ±äĄ¶É« |
| A£® | A | B£® | B | C£® | C | D£® | D |
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗŃ”ŌńĢā
| A£® | Å©×÷ĪļŹÕ»ńŗ󣬾ĶµŲ·ŁÉÕ½ÕøŃ£¬Ōö¼ÓĶĮČĄÖŠ¼Ų·Źŗ¬Įæ | |
| B£® | ¹¤Ņµ·ĻĖ®æɾ¹ż”°ŌŁÉś”±“¦Ąķ£¬ÓĆÓŚ³ĒŹŠµĄĀ·±£½ą”¢ÅēČŖŗĶ½½»ØÓĆĖ® | |
| C£® | ¹čµ„ÖŹ³£×÷ĪŖÖʱø¹āµ¼ĻĖĪ¬µÄÖ÷ŅŖ²ÄĮĻ | |
| D£® | ĢŌĆ×Ė®ÖŠŗ¬ÓŠµķ·ŪæÉŅŌÖ±½Ó¼ģ²ā¼ÓµāŃĪÖŠŹĒ·ńŗ¬ÓŠµāŌŖĖŲ |
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ½ā“šĢā
 £®
£®²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ½ā“šĢā

²éæ““š°øŗĶ½āĪö>>
°Ł¶ČÖĀŠÅ - Į·Ļ°²įĮŠ±ķ - ŹŌĢāĮŠ±ķ
ŗž±±Ź”»„ĮŖĶųĪ„·ØŗĶ²»Į¼ŠÅĻ¢¾Ł±ØĘ½ĢØ | ĶųÉĻÓŠŗ¦ŠÅĻ¢¾Ł±Ø×ØĒų | µēŠÅÕ©Ę¾Ł±Ø×ØĒų | É꥜Ź·ŠéĪŽÖ÷ŅåÓŠŗ¦ŠÅĻ¢¾Ł±Ø×ØĒų | ÉęĘóĒÖČؾŁ±Ø×ØĒų
Ī„·ØŗĶ²»Į¼ŠÅĻ¢¾Ł±Øµē»°£ŗ027-86699610 ¾Ł±ØÓŹĻä£ŗ58377363@163.com