
【题目】COP、FeS2、NiS2等物质对电化学氢析出反应有良好的催化活性和稳定性。请回答下列问题:
(1)基态Co原子价层电子的电子排布图(轨道表达式)为________________,基态P原子的电子占据最高能级的电子云轮廓图为________形。
(2)PH3的沸点________(填“高于”或“低于”)NH3,原因是______________。
(3)PH3分子的空间结构为__________,其中存在的共价键类型为_________________,P原子的杂化方式为______________________
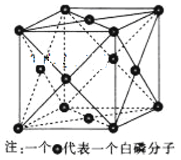
(4)下图为白磷(P4)的晶胞示意图,晶胞的边长为a nm,设阿伏加德罗常数的数值为NA,其晶体密度的计算表达式为______g·cm-3。
【答案】![]() 哑铃形或纺锤形 低于 NH3分子间存在氢键,PH3不存在分子间氢键 三角锥形 σ键或极性共价键 sp3
哑铃形或纺锤形 低于 NH3分子间存在氢键,PH3不存在分子间氢键 三角锥形 σ键或极性共价键 sp3 ![]()
【解析】
(1)Co为过渡元素,价电子包括最外层电子和次外层d能级电子,基态Co原子价层电子的电子排布图为![]() ;基态P原子电子排布式为[Ne]3s23p3,电子占据最高能级的电子云轮廓图为哑铃形或纺锤形;
;基态P原子电子排布式为[Ne]3s23p3,电子占据最高能级的电子云轮廓图为哑铃形或纺锤形;
(2)NH3分子间存在氢键,PH3不存在分子间氢键,因此NH3的沸点高于PH3;
(3)PH3中心原子P有3个σ键,孤电子对数为(5-3×1)/2=1,PH3空间构型为三角锥形;存在的共价键类型为σ键或极性共价键;P原子的杂化类型为sp3;
(4)晶胞中白磷分子位于顶点和面心,个数为8×1/8+6×1/2=4,晶胞的质量为4×31×4/NAg,晶胞的体积为(a×10-7)3cm3,根据密度的定义,ρ=![]() g/cm3;
g/cm3;


科目:高中化学 来源: 题型:
【题目】以电石渣[主要成分Ca(OH)2,含Fe2O3、MgO和SiO2等杂质]为原料制备纳米碳酸钙的一种工艺流程如下:


(1)“浸渍”时,NH4Cl和Ca(OH)2反应的化学方程式为________________________________________。
(2)“浸渍”时,一定时间内Ca2+浸取率随温度变化如图所示。Ca2+浸取率随温度升高而上升的两个原因是_________________________________________;__________________________________________。
(3) “碳化”时,一般采用低温工艺,对应的离子方程式为___________________________。
(4)滤液Ⅱ中,可循环利用的溶质的化学式为___________________________________。
(5)“洗涤”时,检验是否洗净的方法是________________________________________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】快乐是什么?精神病学专家通过实验发现:在大脑的相应部位—“奖赏中心”,给予柔和的电击,便会处于似乎极度快乐的状态。人们已经将“奖赏中心”各部分的脑电图绘制出来,并认为,在各区域之间传递信息的化学物质是多巴胺,所以“奖赏中心”又称为多巴胺系统。多巴胺结构如下图:
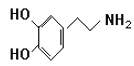
(1)多巴胺分子式:______________________。
(2)试判断多巴胺能发生的化学反应___________。
A.加成 B.取代 C.氧化 D.水解
(3)写出与多巴胺互为同分异构体且属于1、3、5三取代苯并且苯环上直接连有一个羟基和一个氨基且分别能与钠和氢氧化钠反应,消耗钠与氢氧化钠的物质的量之比为2:1的所有物质的结构简式:__________________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】I.反应A(g)+B(g)![]() C(g)+D(g)过程中的能量变化如图所示,回答下列问题。
C(g)+D(g)过程中的能量变化如图所示,回答下列问题。

(1)该反应是_____________反应(填“吸热”或“放热”)。
(2)下列表述能作为反应达到化学平衡状态的标志是(________)
A.反应速率v(A)∶v(B)∶v(C)∶v(D) =1∶1∶1∶1
B.各组分的质量分数不再改变
C.混合气体的平均相对分子质量不再改变
II.某温度时,在一个2L的密闭容器中,X、Y、Z三种气态物质的物质的量随时间的变化曲线如图所示。根据图中数据,试填写下列空白:

(1)从开始至2min,Z的平均反应速率为________________;
(2)向其中充入1 mol He(g)(He不参加反应),化学反应速率____________(填“加快”“减慢”或“不变”)。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列说法不正确的是( )
A. 温度升高,正逆反应速率都增大
B. 化学反应的速率和限度均可通过改变化学反应条件而改变
C. 可逆反应只是代表少数反应
D. 化学反应达到平衡状态时,正反应速率与逆反应速率相等
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列事实与平衡移动原理无关的是
A. 向含酚酞的Na2CO3溶液中滴加BaCl2溶液,红色变浅
B. 加热MgCl2·6H2O固体最终得到Mg(OH)Cl
C. 将FeS2矿石粉碎更有利于焙烧制备SO2气体
D. NO2气体经过冷凝和加压成无色液体
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】将反应Cu(s)+2Ag+(aq)===Cu2+(aq)+2Ag(s)设计成原电池,某一时刻的电子流向及电流计(G)指针偏转方向如图所示,下列有关叙述正确的是( )

A、KNO3盐桥中的K+移向Cu(NO3)2溶液
B、Cu作负极,发生还原反应
C、电子由AgNO3溶液通过盐桥移向Cu(NO3)2溶液
D、工作一段时间后,AgNO3溶液中c(Ag+)减小
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】用所学知识回答下列问题:
(1)已知常温下,Ksp[Mg(OH)2]=5× ![]() ,若某溶液常温下刚 析出Mg(OH)2固体时,c(Mg2+)=5×
,若某溶液常温下刚 析出Mg(OH)2固体时,c(Mg2+)=5× ![]() mol/L,则此时溶液的pH=______。
mol/L,则此时溶液的pH=______。
(2)已知CH3COONH4溶液呈中性,又知CH3COOH溶液加到NaHCO3溶液中有气体放出,试推断常温下NH4HCO3溶液的pH______7(填“>”、“<”或“=”)。
(3)25℃时,pH=11的KOH溶液中,由水电离出的c(OH-)=_______mol/L。
(4)25℃时,pH=11的K2CO3溶液中,由水电离出的c(OH-)=_______mol/L。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】化学是材料、能源、环境、信息等现代科学技术的重要基础。下列说法不正确的是
A. 制造矢量发动机使用含铼(Re)合金材料,合金是纯净物
B. “人造太阳”的核燃料是氘、氚,12H、13H互为同位素
C. 在人体中检测出了“微塑料”,说明白色污染危害严重
D. 制造芯片的工艺中,用氢氟酸腐蚀硅是化学变化
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com