
���ݻ�Ϊ1 L���ܱ������У��������·�Ӧ�� A(g)��2B(g) 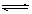 C(g)��D(g)���ڲ�ͬ�¶��£�D�����ʵ���n(D)��ʱ��t�Ĺ�ϵ��ͼ��
C(g)��D(g)���ڲ�ͬ�¶��£�D�����ʵ���n(D)��ʱ��t�Ĺ�ϵ��ͼ��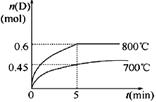
��ش��������⣺
��1��700��ʱ��0��5min�ڣ���B��ʾ��ƽ����Ӧ����Ϊ_______��
��2�����жϷ�Ӧ�ﵽ��ѧƽ��״̬��������__________��
A��������ѹǿ���� B�����������c(A)����
C��v��(B)��2v��(D) D��c(A)��c(C)
��3�����������1.0 mol A��2.2 mol B������ͼ�����ݼ���800��ʱ��ƽ�ⳣ��K��___ _______���÷�ӦΪ__________��Ӧ(����ȡ����ȡ�)��
��4�� 800��ʱ��ijʱ�̲����ϵ�����ʵ���Ũ�����£�c(A)��0.06 mol/L��c(B)��0.50 mol/L��c(C)��0.20 mol/L��c(D)��0.018 mol/L�����ʱ�÷�Ӧ______ ____(�����������С��������淽����С�����ƽ��״̬��)��
��1��0.18 mol/(L��min) ��2��ABC ��3��0.9 ����
��4�������������
���������������1��700��ʱ��0-5min�ڣ�D��ƽ����ѧ��Ӧ����v(D)����n/(V?��t)=0.45mol/(1L��5min)
=0.09mol/(L?min)��ͬһ��Ӧ�У������ʵķ�Ӧ����֮�ȵ��ڼ�����֮�ȣ�����v��B����v��D��=2��1��
��v��B��=0.18mol?L-1?min-1��
��2���÷�Ӧ�Ƿ�Ӧǰ�����������С�ķ�Ӧ����Ӧ�ﵽƽ��״̬ʱ�����淴Ӧ������ȣ�ƽ��ʱ�������ʵ����ʵ�����Ũ�ȵȲ��ٷ����仯�����ԣ�
A���÷�Ӧ�Ƿ�Ӧǰ�����������С�ķ�Ӧ����ѹǿ����ʱ�������ʵ�Ũ�Ȳ��ٷ����仯����A��ȷ��
B����Ӧ�ﵽƽ��״̬ʱ�����淴Ӧ������ȣ�ƽ��ʱ�������ʵ����ʵ�����Ũ�ȵȲ��ٷ����仯��B��ȷ��
C��v����B��=2v�棨D��������֮�ȵ��ڻ�ѧ������֮�ȣ���Ӧ��ƽ��״̬����C��ȷ��
D�����۷�Ӧ�Ƿ�ﵽƽ��״̬��c��A��=c��C�������Բ�����Ϊ�ж�ƽ��״̬�����ݣ���D����
��3�� A��g��+2B��g��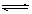 C��g��+D��g��
C��g��+D��g��
��ʼ(mol/L) 1.0 2.2 0 0
��Ӧ(mol/L) 0.6 1.2 0.6 0.6
ƽ��(mol/L) 0.4 1.0 0.6 0.6
��ѧƽ�ⳣ��K=(0.6mol/L��0.6mol/L)/[0.4mol/L��(1.0mol/L)2 ]=0.9��mol?L-1��-1��
����ͼ��֪�������¶�D�ĺ������٣�����ƽ�����淴Ӧ�����ƶ���������Ӧ�����ȷ�Ӧ��
��4��A��B��C��D�����ʵ�Ũ�ȷֱ�Ϊc(A)��0.06 mol/L��c(B)��0.50 mol/L��c(C)��0.20 mol/L��c(D)��0.018 mol/L��Ũ����QC="(0.2" mol/L��0.018 mol/L)/[0.06 mol/L��(0.5 mol/L)2 ]=0.24��mol?L-1��-1��0.9��mol?L-1��-1�����Է�Ӧ������Ӧ������С�
���㣺���⿼����ǻ�ѧƽ���־���жϡ���Ӧ���ʵļ��㡢ƽ�ⳣ���ļ���ȡ�


 ��������һ���þ�ϵ�д�
��������һ���þ�ϵ�д� Сѧ��10����Ӧ����ϵ�д�
Сѧ��10����Ӧ����ϵ�д�
| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
�״���������10��һ25���ļ״�����������ԭ�ϡ����Ӽ��ϳɵ����ͳ���ȼ�ϣ��ɴﵽ�������͵����ܺ�ָ�ꡣ�״���һ�ֿ�������Դ�����й㷺�Ŀ�����Ӧ��ǰ����
��ҵ�Ϻϳɼ״�һ��������з�Ӧ��CO��g��+2 H2��g�� CH3 OH��g�� ��H="a" kJ/mol��
CH3 OH��g�� ��H="a" kJ/mol��
�±��Ǹ÷�Ӧ�ڲ�ͬ�¶��µĻ�ѧƽ�ⳣ����K����
| �¶�/0C | 250 | 310 | 350 |
| K | 2.041 | 0.250 | 0.012 |
| Ũ��mol/L ʱ��/min | c(CO) | c(H2) | c(CH3OH) |
| 0 | 0.8 | 1.6 | 0 |
| 2 | 0.6 | 1.2 | 0.2 |
| 4 | 0.3 | 0.6 | 0.5 |
| 6 | 0.3 | 0.6 | 0.5 |
 CH3 OH��g����H="a" kJ/mol�����º����·�Ӧ��ͬʱ��ֱ�����ϵ��CO�İٷֺ����ֱ�Ϊw1��w2����֪T1<T2����
CH3 OH��g����H="a" kJ/mol�����º����·�Ӧ��ͬʱ��ֱ�����ϵ��CO�İٷֺ����ֱ�Ϊw1��w2����֪T1<T2�����鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
��ҵ��һ���ں����ܱ������в������з�Ӧ�ϳɼ״���
CO(g)��2H2(g)  CH3OH(g)+Q
CH3OH(g)+Q
��1�����жϷ�Ӧ�ﵽƽ��״̬��������(����ĸ��ţ���ͬ)________��
| A������CH3OH������������CO��������� | B�����������ܶȲ��� |
| C����������ƽ����Է����������� | D��CH3OH��CO��H2��Ũ�ȶ����ٷ����仯 |
| �¶� | 250�� | 300�� | 350�� |
| K | 2.041 | 0.270 | 0.012 |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
t��ʱ����3 mol A��1 mol B����ͨ�����Ϊ2L���ܱ�������(�ݻ�����)���������·�Ӧ��3A(g)+B(g) xC(g)��2minʱ��Ӧ�ﵽƽ��״̬(�¶Ȳ���)��ʣ����0.8 mol B�������C��Ũ��Ϊ0.4 mol��L������д���пհף�
xC(g)��2minʱ��Ӧ�ﵽƽ��״̬(�¶Ȳ���)��ʣ����0.8 mol B�������C��Ũ��Ϊ0.4 mol��L������д���пհף�
��1���ӿ�ʼ��Ӧ���ﵽƽ��״̬������C��ƽ����Ӧ����Ϊ ��
��2��x�� ��
��3������ԭƽ��������������ٳ���a mol C����t��ʱ�ﵽ�µ�ƽ�⣬��ʱB�����ʵ���Ϊn(B)��
mol��
��4�����������Ӧ����ͬ�¶Ⱥ������н��У���ʹ��Ӧ�ﵽƽ��ʱC�����ʵ���������ԭƽ����ȣ���ʼ������������ʵ����ʵ���n(A)��n(B)��n(C)֮��Ӧ������Ĺ�ϵʽΪ ��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
��1����������Ĵ������Ĺ�����ͼ��ʾ������a��c�����Ļ�ѧ����ʽ�ɱ�ʾΪ��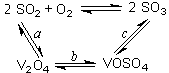
SO2+V2O5 SO3+ V2O4
SO3+ V2O4
4VOSO4+O2 2V2O5+4SO3��
2V2O5+4SO3��
�÷�Ӧ�Ĵ����� ��д��ѧʽ��
��2�� 550 ��ʱ��SO2ת��ΪSO3��ƽ��ת���ʣ���������ϵ��ѹǿ��p���Ĺ�ϵ��ͼ��ʾ����2��0 mol SO2��1��0 mol O2����5 ���ܱ������У���Ӧ��ƽ�����ϵ��ѹǿΪ0��10 M Pa���Լ��㷴Ӧ2SO3 2SO2+O2��550 ��ʱ��ƽ�ⳣ��K= ��
2SO2+O2��550 ��ʱ��ƽ�ⳣ��K= ��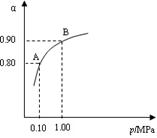
��3��550 ��ʱ����2��0 mol SO2��1��0 mol O2����5 ���ܱ������У���Ӧ ��ƽ������д�ʩ����ʹn(SO3)/n(SO2)�������
A�������¶�
B������He(g)��ʹ��ϵ��ѹǿ����
C���ٳ���2 mol SO2��1 mol O2
D���ٳ���1 mol SO2��1 mol O2
��4��ά���¶Ȳ���������ʹ֮�������·�Ӧ��2SO2��O2 2SO3������ֻ�ܱ�����A��B��A������һ�������ƶ��Ļ�����ʹ�����ڱ��ֺ�ѹ��B�����ܱ��ֺ��ݡ���ʼʱ�������������зֱ��������ʵ����������Ϊ2��1��SO2��O2�Ļ�����壬��ʹA��B�ݻ���ȣ�����ͼ��ʾ����
2SO3������ֻ�ܱ�����A��B��A������һ�������ƶ��Ļ�����ʹ�����ڱ��ֺ�ѹ��B�����ܱ��ֺ��ݡ���ʼʱ�������������зֱ��������ʵ����������Ϊ2��1��SO2��O2�Ļ�����壬��ʹA��B�ݻ���ȣ�����ͼ��ʾ����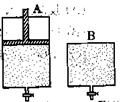
����д���пո�
A�����ﵽƽ��ʱ�����ʱ���B����__________������̻�����ƽ��ʱA������SO2��ת���ʱ�B����_______��������С�������ﵽ����ƽ���������������ͨ������ʵ�����ԭ��Ӧ���壬�ﵽƽ��ʱ��A�����Ļ��������SO3���������_________�����������С�����䡱����ͬ����B�����Ļ��������SO3���������_________��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
��ij�¶��£�����㶨���ܱ������м���2 molN2��4 molH2���������·�Ӧ��
N2(g)+3H2(g) 2NH3(g)����H����92.4 kJ/mol���ﵽƽ��ʱ���ų�����46.2 kJ����
2NH3(g)����H����92.4 kJ/mol���ﵽƽ��ʱ���ų�����46.2 kJ����
��1���ﵽƽ��ʱ��N2��ת����Ϊ_______________, NH3���������Ϊ ��
��2������������м���a mol N2��b mol H2��c mol NH3����a��b��c��Ϊ����������ͬ�����´ﵽƽ��ʱ��������и���ֵ����ʵ���������ƽ����ͬ��a��b��cȡֵ���������һ�������� , ��
��3����ѧ�ҷ�����ʹNH3ֱ������ȼ�ϵ�صķ�������װ���ò������缫������������Һ�У�һ���缫ͨ���������һ�缫ͨ��NH3�������ܷ�ӦʽΪ��4NH3+3O2��2N2+6H2O���������ҺӦ���� ������������������ԡ� �������ԡ� ���ԡ� ����д�������ĵ缫��Ӧ����ʽ������������������ ��������
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
��ͼ��ʾ��B�л����������ɻ�����A��B�о���1mol X��1mol Y����ʼʱ��V(A)��V(B)��a L���ر�K����ͬ�¶��£���������ͬʱ������Ӧ��2X(g)��2Y(g) Z(g)��2W(g) ��H��0���ﵽƽ�⣨��ʱ��V(B)��0.8a L��
Z(g)��2W(g) ��H��0���ﵽƽ�⣨��ʱ��V(B)��0.8a L��
��1���ﵽƽ�������ʱ�䣺A B�����>������<������=������ͬ��
��2��W�İٷֺ�����A B��
��3��B��X��ת����Ϊ ��
��4����K�����´�ƽ�⣨��ʱ��B�����Ϊ L���ú�a��ʽ�ӱ�ʾ����ͨ��������Բ��ƣ���
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
�跴Ӧ��Fe(s)+CO2(g) FeO(s)+CO(g)��H=Q1��ƽ�ⳣ��ΪK1��
FeO(s)+CO(g)��H=Q1��ƽ�ⳣ��ΪK1��
��Ӧ��Fe(s)+H2O(g) FeO(s)+H2(g)��H=Q2��ƽ�ⳣ��ΪK2���ڲ�ͬ�¶��£�K1��K2��ֵ���£�
FeO(s)+H2(g)��H=Q2��ƽ�ⳣ��ΪK2���ڲ�ͬ�¶��£�K1��K2��ֵ���£�
| �¶�(T) | K1 | K2 |
| 973 | 1��47 | 2��38 |
| 1173 | 2��15 | 1��67 |
 CO(g)+H2O(g)��H=Q3
CO(g)+H2O(g)��H=Q3�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
��֪A(g)+B(g)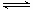 2 C(g)��Ӧ��ƽ�ⳣ�����¶ȵĹ�ϵ���£�
2 C(g)��Ӧ��ƽ�ⳣ�����¶ȵĹ�ϵ���£�
| �¶�/ �� | 700 | 800 | 830 | 1000 | 1200 |
| ƽ�ⳣ�� | 1��70 | 1��10 | 1��00 | 0��60 | 0��40 |
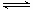 A(g)+B(g)��ƽ�ⳣ����ֵΪ ��
A(g)+B(g)��ƽ�ⳣ����ֵΪ ���鿴�𰸺ͽ���>>
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com