
【题目】表为元素周期表的一部分,请回答有关问题:
ⅠA | ⅡA | ⅢA | ⅣA | ⅤA | ⅥA | ⅦA | 0 | |
2 | ① | ② | ||||||
3 | ③ | ④ | ⑤ | ⑥ | ⑦ | ⑧ | ||
4 | ⑨ |
(1)表中最活泼的金属是___________,非金属性最强的元素是____________。(填写元素符号,下同)
(2)表中能形成两性氢氧化物的元素是_______________,分别写出该元素的氢氧化物与⑥、⑨最高价氧化物对应水化物反应的化学方程式:___________、___________。
(3)⑨最高价氧化物对应水化物的电子式______________。
(4)利用下图装置来验证同主族元素非金属性的变化规律:
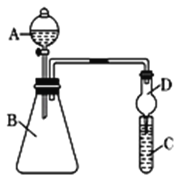
要证明非金属性:C>Si,在A中加盐酸,B中加CaCO3,C中加Na2SiO3溶液,应在B、D之间增加一个盛有足量____(选填下列字母:A 浓盐酸 、B 浓NaOH溶液、C 饱和Na2CO3溶液 、D 饱和NaHCO3溶液)的洗气装置.改进后C中发生反应的化学方程式是_____.
【答案】K F Al 2Al(OH)3+3H2SO4═Al2(SO4)3+6H2O Al(OH)3+KOH═KAlO2+2H2O; ![]() D Na2SiO3+CO2+H2O═H2SiO3↓+Na2CO3
D Na2SiO3+CO2+H2O═H2SiO3↓+Na2CO3
【解析】
本题是对元素周期表和元素周期律的综合考查。根据各元素在表中的位置可知①‐⑨分别为:C、F、Mg、Al、Si、S、Cl、Ar、K,金属性最强的元素位于左下角,非金属性最强的元素位于右上角,非金属性的强弱可通过最高价含氧酸的酸性比较,利用强制弱的原理,通过实验验证。
(1)根据各元素位置,⑨位于左下角,②位于右上角,故最活泼的金属是K,非金属性最强的是F;
(2)能形成两性氢氧化物的元素是Al,其氢氧化物为Al(OH)3,⑥、⑨最高价氧化物对应水化物分别为H2SO4、KOH,反应的化学方程式分别为:2Al(OH)3+3H2SO4═Al2(SO4)3+6H2O、Al(OH)3+KOH═KAlO2+2H2O;
(3)⑨最高价氧化物对应水化物为KOH,其电子式![]() ;
;
(4)要证明非金属性:C>Si,可通过比较酸性H2CO3>H2SiO3,利用强酸制弱酸的原理进行验证,如图B中产生的CO2通入C中,Na2SiO3+CO2+H2O═H2SiO3↓+Na2CO3,得到H2SiO3白色沉淀,结论得到验证,但由于盐酸具有挥发性,可能通过导管进入C中,干扰实验,故需除去HCl,最合适的试剂为饱和NaHCO3溶液,选D。


科目:高中化学 来源: 题型:
【题目】氟他胺G是一种可用于治疗肿瘤的药物。实验室由芳香烃A制备G的合成路线如下:
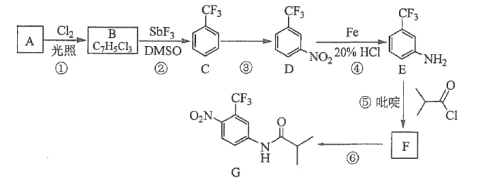
回答下列问题:
(1)A的结构简式为______,B的官能团名称:_____,C的化学名称是______。
(2)③的反应试剂和反应条件分别是_____,该反应的类型是__________。
(3)⑤的反应方程式为____________。
(4)G的分子式为__________。
(5)H是G的同分异构体,其苯环上的取代基与G的相同但位置不同,则H可能的结构有______种。
(6)4-甲氧基乙酰苯胺(![]() )是重要的精细化工中间体,写出由苯甲醚(
)是重要的精细化工中间体,写出由苯甲醚(![]() )制备4-甲氧基乙酰苯胺的合成路线_________(其他试剂任选)。
)制备4-甲氧基乙酰苯胺的合成路线_________(其他试剂任选)。
合成路线示例:![]()
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】如图装置(I)为一种可充电电池的示意图,其中的离子交换膜只允许K+通过,该电池放电、充电的化学方程式为:2K2S2+KI3![]() K2S4+3KI。装置(II)为电解池的示意图。当闭合开关K时,电极X附近溶液先变红。则闭合K时,下列说法正确的是( )
K2S4+3KI。装置(II)为电解池的示意图。当闭合开关K时,电极X附近溶液先变红。则闭合K时,下列说法正确的是( )
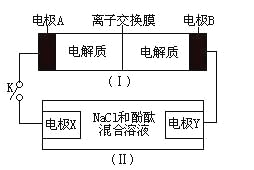
A.K+从右到左通过离子交换膜
B.电极A上发生的反应为:3I--2e-=I3-
C.电极X上发生的反应为:2Cl--2e-=C12↑
D.当有0.1molK+通过离子交换膜,X电极上产生1.12L气体(标准状况)
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】(1)如图的氮循环是生态系统物质循环的重要部分,人类活动加剧了氮循环中的物质转化。
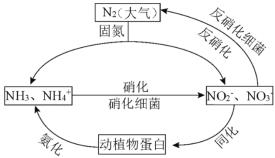
①下列说法正确的是_______(填字母序号)
A.固氮过程中,N2只做氧化剂
B.硝化过程需要有氧化剂参与
C.反硝化过程有助于弥补人工固氮对氮循环造成的影响
D.同化、氨化过程中,实现了氮元素在无机物和有机物之间的转化
②反硝化过程中,CH3OH可作为反应的还原剂,1mol还原剂失去6mol电子。请将该反应的离子方程式补充完整:5CH3OH+□NO3—![]() □_______+□_______+□_______+□_______,_____________
□_______+□_______+□_______+□_______,_____________
(2)研究表明,氮氧化物(NOx)和二氧化硫都与大气中雾霾的形成有关。
①已知:SO2生成SO3总反应方程式是2SO2(g)+O2(g)![]() 2SO3(g)ΔH=-196.6kJ/mol
2SO3(g)ΔH=-196.6kJ/mol
此反应可通过如下两步完成:2NO(g)+O2(g)![]() 2NO2(g)ΔH1=-113kJ/mol
2NO2(g)ΔH1=-113kJ/mol
NO2(g)+SO2(g)![]() SO3(g)+NO(g)ΔH2=_______。
SO3(g)+NO(g)ΔH2=_______。
②一定温度下,向2L恒容密闭容器中充入NO2和SO2各1mol,5min达到平衡,此时容器中NO2和NO的浓度之比为1∶3,则NO2的平衡转化率是_______。
(3)砷(As)是第四周期ⅤA族元素,其化合物,有着广泛的用途。
①AsH3的稳定性比NH3的稳定性_______(填“强’’或“弱’’)。用原子结构解释原因_______。
②常将含砷废渣(主要成分为As2S3)制成浆状,通入O2氧化,生成H3AsO4和单质硫。写出发生反应的化学方程式_______。
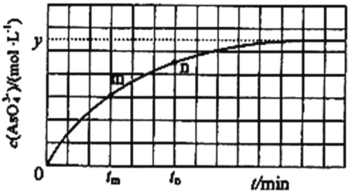
③298K时,将20mL3xmolL-1Na3AsO3、20mL3xmolL-1I2和20mLNaOH溶液混合,发生反应:AsO33-(aq)+I2(aq)+2OH-![]() AsO43-(aq)+2I-(aq)+H2O(l)。溶液中c(AsO43﹣)与反应时间(t)的关系如图所示。若平衡时溶液的pH=14,则该反应的平衡常数K为_______。
AsO43-(aq)+2I-(aq)+H2O(l)。溶液中c(AsO43﹣)与反应时间(t)的关系如图所示。若平衡时溶液的pH=14,则该反应的平衡常数K为_______。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】在一个绝热容积不变的密闭容器中发生N2(g)+3H2(g)![]() 2NH3(g) △H<0。下列各项能说明该反应已经达到反应限度的是( )
2NH3(g) △H<0。下列各项能说明该反应已经达到反应限度的是( )
A.容器内气体的总质量保持不变
B.断裂lmolN≡N键的同时断裂3molH-H键
C.容器中H2的浓度保持不变
D.v(N2):v(H2):v(NH3)=1:3:2
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】1-氯丙烷和2-氯丙烷分别与NaOH乙醇溶液共热的反应,下列有关说法不正确的是( )
A. 产物相同B. 碳氢键断裂的位置相同
C. 反应类型相同D. 1-氯丙烷和2-氯丙烷都能与NaOH水溶液共热的发生反应
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】X、Y、Z三种元素的原子序数依次减小且三者原子序数之和为16,其常见单质在适当条件下可发生如图所示变化,其中B和C均为10电子分子。下列说法不正确的是( )
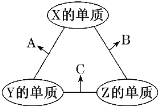
A.X元素位于VIA族B.1 molC中含有3mol共价键
C.A和C在一定条件下能发生氧化还原反应D.X与Y的最高正价大小:X>Y
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】W、X、Y、Z为短周期原子序数依次增大的主族元素,其中W元素形成的单质密度最小,且W与X、Y、Z都能形成共价化合物,Y、W形成的常见化合物溶于水显碱性,Z、W形成的化合物溶于水显酸性。四种元素原子序数之和为30,可形成的某种化合物结构式为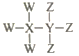 。下列说法正确的是
。下列说法正确的是
A.X为碳元素
B.Y的氧化物对应的水化物是强酸
C.W与Y、Z三种元素形成的化合物中一定不含离子键
D.含Z的某种含氧酸盐可用于物体表面和环境等的杀菌消毒
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】近来有报道,碘代化合物E与化合物G在Cr-Ni催化下可以发生偶联反应,合成一种多官能团的化合物Y,其合成路线如下:
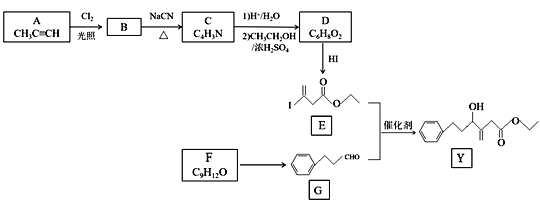
已知:①RCN![]() RCOOH
RCOOH
②RCHO+CH3CHO![]() RCH=CHCHO+H2O
RCH=CHCHO+H2O
回答下列问题:
(1)D的结构简式为________。
(2)下列说法正确的是__________。
A.物质A中最多有5个原子在同一平面内 B.D生成E的反应为取代反应
C.物质G和银氨溶液能发生反应 D.物质Y的分子式为C15H18O3
(3)B为单氯代烃,由B生成C的化学方程式为_________。
(4)写出同时符合下列条件的D的所有同分异构体的结构简式_______。
①具有完全相同的官能团,且不含“—O—C≡C—”;
②核磁共振氢谱显示三种不同化学环境的氢,其峰面积之比为3∶3∶2。
(5)以苯甲醇、乙醛为原料制备F,写出相应的合成路线流程图(无机试剂任用,合成路线流程图示例见本题题干)。________________。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com