
| A. | 用浓盐酸与二氧化锰共热制氯气 | |
| B. | 标准状况下,将1 g铝片投入20 mL 18 mol•L-1硫酸中 | |
| C. | 向100 mL 4 mol•L-1硝酸中加入5.6 g 铁 | |
| D. | 在5×107 Pa、500℃和铁触媒催化的条件下,用氮气和氢气合成氨 |
分析 A.二氧化锰与浓盐酸反应,随反应进行浓盐酸变成稀盐酸,二氧化锰与稀盐酸不反应;
B.18.4mol/L的硫酸为浓硫酸,常温下遇到铁、铝金属发生的钝化,不再继续反应;
C.向100mL4mol/L的硝酸中加入5.6g铁根据反应的量,铁全部反应生成三价铁离子;
D.氮气和氢气生成氨气的反应是可逆反应,存在反应限度,所以不能完全反应.
解答 解:A.MnO2+4HCl(浓)$\frac{\underline{\;\;△\;\;}}{\;}$MnCl2+Cl2↑+2H2O,二氧化锰与越浓盐酸反应,随反应进行,浓盐酸变成稀盐酸,二氧化锰与稀盐酸不反应,盐酸不能完全反应,故A错误;
B.标准状况下,铝片遇浓硫酸发生钝化,阻止反应进行,铝片不能完全反应,故B错误;
C.根据反应Fe+4HNO3=Fe(NO3)3+NO↑+2H2O,0.4mol硝酸氧化0.1mol铁为0.1mol三价铁离子,铁无剩余,故C正确;
D.氮气与氢气在高温、高压催化剂作用下反应生成氨气:N2+3H2?2NH3,该反应是可逆反应,存在反应限度,所以氢气不能完全反应,故D错误;
故选C.
点评 本题考查了元素化合物的性质,注意物质浓度对物质性质的影响、可逆反应特点,变价金属铁与硝酸反应量不同产物不同为该题的难点,题目难度中等.


科目:高中化学 来源:2016-2017学年河南省高一上月考二化学试卷(解析版) 题型:实验题
某课外活动小组进行Fe(OH)3胶体的制备实验并检验其性质。
(1)现有甲、乙、丙三名同学进行Fe(OH)3胶体的制备。
① 甲同学的操作是:取一小烧杯,加入25 mL蒸馏水加热至沸腾,向沸水中逐滴加入1~2 mL FeCl3饱和溶液,继续煮沸至混合液呈红褐色,停止加热。
② 乙直接加热饱和FeCl3溶液。
③ 丙向沸水中滴加饱和FeCl3溶液,为了使反应进行充分,煮沸10分钟。
你认为哪位同学的制备方法更合理: ,可以利用胶体的什么性质来证明有Fe(OH)3胶体生成? 。
(2)Fe(OH)3胶体稳定存在的主要原因是_________________。
A.胶粒直径小于1 nm B.胶粒带正电荷 C.胶粒作布朗运动 D.胶粒能透过滤纸
(3)Fe(OH)3胶体区别于FeCl3溶液最本质的特征是____________。
A.Fe(OH)3胶体粒子的直径在1~100 nm之间 B.Fe(OH)3胶体具有丁达尔效应
C.Fe(OH)3胶体是均一的分散系 D.Fe(OH)3胶体的分散质能透过滤纸
(4)提纯所制Fe(OH)3胶体常用的方法是________,若 向Fe(OH)3胶体中滴入硫酸直到过量,描述此过程的实验现象_______________________。
向Fe(OH)3胶体中滴入硫酸直到过量,描述此过程的实验现象_______________________。
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 液氯、干冰均为纯净物 | |
| B. | NO2、CO、CO2均为酸性氧化物 | |
| C. |  与 与 互为同系物 互为同系物 | |
| D. | 淀粉、纤维素和油脂都属于天然高分子化合物 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 属于羧基类的有2种 | |
| B. | 属于酯类的有3种 | |
| C. | 存在分子中含有六元环的同分异构体 | |
| D. | 分子中可含有两种不同的官能团 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 25℃时,pH=11 NaOH溶液和pH=3 CH3COOH混合,若溶液显酸性,则所得溶液中离子浓度可能为c(CH3COO-)>c(H+)>c(Na+)>c(OH-) | |
| B. | 取c(H+)=0.01mol/L的盐酸和醋酸各100mL,分别稀释2倍后,再分别加入0.03g锌粉,在相同条件下充分反应,醋酸与锌反应的速率大 | |
| C. | 含等物质的量的NaHC2O4和Na2C2O4的溶液中存在:2c(Na+)=3[c(HC2O4-)+c(C2O42-)+c(H2C2O4)] | |
| D. | 25℃时,某溶液中由水电离出的c(H+)=10-amol/L,若a>7时,该溶液pH一定为14-a |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 可用铁作阳极材料 | |
| B. | 电解过程中阳极附近溶液的pH升高 | |
| C. | 阳极反应方程式为:2Cl--2e-═Cl2↑ | |
| D. | 1 mol二价镍全部转化为三价镍时,外电路中通过 了2 mol 电子 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
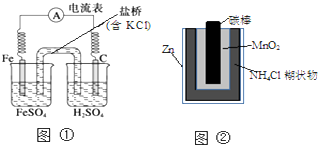
| A. | 图①中正极附近溶液pH降低 | |
| B. | 图②正极反应是2MnO2(s)+H2O(l)+2e-=Mn2O3(s)+2OH-(aq) | |
| C. | 图①中电子由Fe流向石墨,盐桥中的Cl-移向FeSO4溶液 | |
| D. | Zn-MnO2干电池自放电腐蚀主要是由MnO2的氧化作用引起的 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
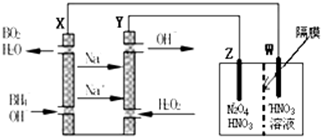
查看答案和解析>>
科目:高中化学 来源: 题型:选择题

| A. | X和Y与电流表连接,Cu极为正极,发生氧化反应 | |
| B. | X和Y与电流表连接,盐桥中的阴离子移向CuSO4溶液 | |
| C. | X和Y分别与电源“-”、“+”极相连,Cu极质量减轻 | |
| D. | X和Y分别与电源“+”、“-”极相连,Zn极电极反应为4OH--4e-═O2↑+2H2O |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com