
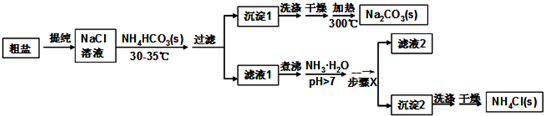
分析 根据题中流程可知,粗盐水提纯后得氯化钠溶液,经蒸发浓缩后,温度控制在30℃~35℃,防止碳酸氢按分解,加入碳酸氢铵,生成沉淀1为碳酸氢钠,滤液1主要为氯化铵,氯化铵溶液中加入氨水,可抑制铵根离子的水解,经过蒸发浓缩、冷却结晶、过滤可得沉淀2为氯化铵固体,经洗涤、干燥得纯净的氯化铵,滤液2中含有少量的氯化铵和碳酸氢钠,
(1)粗盐中含有Ca2+、Mg2+、SO42-等杂质离子,使用的试剂有:①NaOH ②BaCl2③HCl ④Na2CO3,根据前面加入的物质是过量的,在后面加入的物质在除去溶液中原来的杂质外还要将前面加入的试剂杂质除去,据此判断;过滤中用到玻璃棒的作用是引流;
(2)样品中加入适量的氯化钡溶液可判断粗盐中SO42-是否已除尽;
(3)蒸发浓缩时溶液要加热,而NH4HCO3在36℃开始分解,据此答题;
(4)碳酸氢钠受热分解生成碳酸钠、二氧化碳和水;
(5)氨水能抑制铵根离子的水解,同时能使NaHCO3转化为Na2CO3,并补充煮沸时损失的NH3,从氯化铵溶液得到氯化铵固体可以通过蒸发浓缩,冷却结晶,过滤的方法;
(6)由滴定用去的氢氧化钠的物质的量计算出盐酸的物质的量,根据方程式4NH4Cl+6HCHO→(CH2)6N4+4HCl+6H2O,计算出氯化铵的质量,进而计算出样品中氯化铵的质量分数.
解答 解:(1)粗盐中含有Ca2+用Na2CO3除去,Mg2+用NaOH除去,SO42-用BaCl2除去,考虑到除SO42-时,滴加过量的BaCl2,引入的Ba2+也需要用Na2CO3溶液除去,故正确的操作顺序为先滴加过量NaOH溶液,再滴加过量BaCl2溶液,然后滴加过量Na2CO3溶液,过滤后最后滤液里滴加稀盐酸酸化,选项B符合题意;过滤操作中使用玻璃棒起引流作用,
故答案为:B;引流;
(2)判断粗盐中SO42-是否已除尽,实际检验SO42-是否存在,可选择BaCl2溶液来检验,具体操作是:取少量除杂后的样品于试管中,滴加适量氯化钡溶液,若无白色沉淀产生,则含SO42-已除尽,
故答案为:取少量除杂后的样品于试管中,滴加适量氯化钡溶液,若无白色沉淀产生,则含SO42-已除尽;
(3)NH4HCO3很不稳定受热易分解,在加NH4HCO3前加热浓缩NaCl溶液,可避免NH4HCO3的分解,
故答案为:可避免NH4HCO3的分解;
(4)沉淀1是NaHCO3,其受热分解的方程式为:2NaHCO3$\frac{\underline{\;\;△\;\;}}{\;}$Na2CO3+H2O+CO2↑,
故答案为:2NaHCO3$\frac{\underline{\;\;△\;\;}}{\;}$Na2CO3+H2O+CO2↑;
(5)NH4Cl是强酸弱碱盐易水解,且水解生成的HCl有挥发性,NH3•H2O不稳定,易分解放出NH3,故加热过程中添加氨水,可抑制水解,补充挥发的氨,有利于提高NH4Cl的产率和纯度;步骤X的操作目的是从溶液里析出NH4Cl晶体,因此需加热浓缩、冷却结晶并过滤,为提高NH4Cl产品的产率和纯度,需在滤液中加入氨水,理由是:抑制NH4+水解;使NaHCO3转化为Na2CO3 ,步骤X包括的操作有:补充煮沸时损失的NH3蒸发浓缩,冷却结晶,过滤,
故答案为:抑制NH4+水解;使NaHCO3转化为Na2CO3;补充煮沸时损失的NH3蒸发浓缩,冷却结晶,过滤;
(6)采用“甲醛法”测定工业产品中氯化铵的纯度其原理是
4NH4Cl+6HCHO→(CH2)6N4+4HCl+6H2O,再用NaOH溶液滴定,根据原子守恒规律可得关系式:NH4Cl-HCl-NaOH,可知滴定时消耗NaOH的物质的量就是原产品中NH4Cl的物质的量,10mL溶液消耗NaOH的物质的量为0.1mol/L×0.025L=0.00025mol,则样品中NH4Cl的物质的量为0.00025mol×10=0.025mol,质量为0.025mol×53.5g•mol-1=1.3375g,该样品中氯化铵的质量分数=$\frac{1.3375g}{1.5g}$×100%=89.2%,
故答案为:89.2%.
点评 本题考查侯氏制碱法、溶解度、物质的分离提纯、物质含量测定等,题目难度中等,侧重考查学生对流程的分析和基础知识的灵活的应用.


科目:高中化学 来源: 题型:解答题
| 实验步骤 | 预期现象和结论 |
| 步骤1:取少量固体样品于试管中,加入蒸馏水至固体溶解. | 得到无色溶液 |
| 步骤2:向试管中加入过量的BaCl2溶液,静置. | 溶液变浑浊,则证明固体中含有(NH4)2CO3. |
| 步骤3:取步骤2的上层清液于试管中加入少量的Ba(OH)2溶液. | 溶液不变浑浊,则证明固体中不含有NH4HCO3. |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
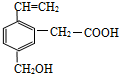 ,关于该有机物的叙述正确的是( )
,关于该有机物的叙述正确的是( )| A. | 不能跟NaOH溶液反应 | |
| B. | 能使溴的四氯化碳溶液褪色,1moL该物质因加成反应消耗溴2mol | |
| C. | 既能与乙酸发生酯化反应,又能与乙醇发生酯化反应 | |
| D. | 在足量的氧气中燃烧1mol该有机物生成H2O 7 mol |
查看答案和解析>>
科目:高中化学 来源: 题型:实验题
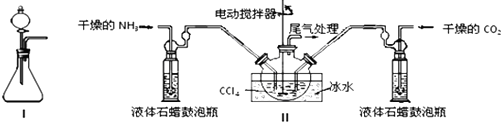
 某实验小组用如图装置制备家用消毒液,并探究其性质.
某实验小组用如图装置制备家用消毒液,并探究其性质.| 操作 | 现象 |
| a.测溶液pH,并向其中滴加2滴酚酞 | pH=13,溶液变红,5min后褪色 |
| b.向其中逐滴加入盐酸 | 溶液逐渐变成黄绿色 |
| 操作 | 现象 |
| 取5mLpH=13NaOH溶液,向其中滴加2滴酚酞 | 溶液变红,30min后褪色 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题

查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | S(g)+O2(g)=SO2(g)+Q3 Q3>297.16 kJ | |
| B. | 单斜硫和正交硫互为同分异构体 | |
| C. | 常温下单斜硫比正交硫稳定 | |
| D. | 单斜硫转化为正交硫的反应是吸热反应 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
 随着工业发展和社会的进步,人们日益关注环境污染问题.
随着工业发展和社会的进步,人们日益关注环境污染问题.查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com