
(6分)以下10种物质:①铝线 ②石墨 ③BaSO4 ④纯硫酸 ⑤金刚石
⑥石灰水 ⑦乙醇 ⑧熔融的KNO3 ⑨NH3 ⑩盐酸
其中(1)能导电的是(填序号,下同)
(2)属于电解质的是
(3)属于非电解质的是
科目:高中化学 来源:2014-2015学年河南省南阳市上学期10月月考高二化学试卷(解析版) 题型:填空题
北京奥运会“祥云”火炬燃料是丙烷(C3H8),亚特兰大奥运会火炬燃料是丙烯(C3H6).
(1)丙烷脱氢可得丙烯. 已知:C3H8(g)═CH4(g)+HC≡CH(g)+H2(g)△H1=156.6kJ?mol﹣1
CH3CH=CH2(g)═CH4(g)+HC≡CH(g)△H2=32.4kJ?mol﹣1则相同条件下,反应C3H8(g)═CH3CH=CH2(g)+H2(g)的△H= kJ?mol﹣1
(2)氢气是一种清洁能源,氢气的制取与储存是氢能源利用领域的研究热点.已知:CH4(g)+H2O(g)=CO(g)+3H2(g)△H=+206.2kJ?mol﹣1CH4(g)+CO2(g)=2CO(g)+2H2(g)△H=+247.4kJ?mol﹣1
2H2S(g)=2H2(g)+S2(g)△H=+169.8kJ?mol﹣1以甲烷为原料制取氢气是工业上常用的制氢方法.CH4(g)与H2O(g)反应生成CO2(g)和H2(g)的热化学方程式为 .
(3)铝是地壳中含量最高的金属元素,其单质及合金在生产生活中的应用日趋广泛.真空碳热还原﹣氯化法可实现由铝矿制备金属铝,其相关的热化学方程式如下:Al2O3(s)+AlCl3(g)+3C(s)=3AlCl(g)+3CO(g)△H=a kJ?mol﹣13AlCl(g)=3Al(l)+AlCl3(g)△H=b kJ?mol﹣1反应Al2O3(s)+3C(s)=2Al(l)+3CO(g)的△H= kJ?mol﹣1(用含a、b的代数式表示).
查看答案和解析>>
科目:高中化学 来源:2014-2015学年河南周口市高二上第一次月考化学(解析版) 题型:选择题
下列事实不能用勒夏特列原理解释的是
A.在硫化氢水溶液中加入碱有利于S2-的生成
B.加入催化剂有利于氨的氧化反应
C.高压有利于合成氨反应
D.向新制氯水中加入碳酸钙有利于次氯酸浓度增大
查看答案和解析>>
科目:高中化学 来源:2014-2015学年河北省高一上学期第二次月考化学试卷(解析版) 题型:选择题
物质分类是化学研究的重要方法之一。化学工作者经常根据物质的组成对物质进行分类研究。近年来发现在金星大气层中存在三氧化二碳。下列物质与它属于同类的是
A.H2、O3 B.H2SO4、H2CO3 C.SO2、NO D.Na2SO4、KClO3
查看答案和解析>>
科目:高中化学 来源:2014-2015学年河北省高一上学期期中化学试卷(解析版) 题型:填空题
(10分)已知铜在常温下能被稀硝酸溶解,其反应的化学方程式如下
3Cu + 8HNO3 == 3Cu(NO3)2 + 2NO↑+ 4H2O
(1)用双线桥法分析上述反应(只需标出电子得失的方向和数目)
3Cu + 8HNO3 == 3Cu(NO3)2 + 2NO↑+ 4H2O
(2)上述反应中氧化剂是 ,氧化产物是 (填化学式)。
(3)若19.2g铜与足量硝酸完全反应,则消耗硝酸为 mol,被还原的硝酸为 mol,生成NO的体积为 L(标准状况) 。
查看答案和解析>>
科目:高中化学 来源:2014-2015学年河北省高一上学期期中化学试卷(解析版) 题型:选择题
下列反应既是离子反应,又是氧化还原反应的是
A.氯化钠溶液中滴入硝酸银溶液
B.铁片置于硫酸铜溶液中
C.铁在氧气中燃烧
D.二氧化碳通入澄清石灰水中
查看答案和解析>>
科目:高中化学 来源:2014-2015学年河北省高一上学期期中化学试卷(解析版) 题型:选择题
下列有关说法正确的是
A.氯化钠溶液均一稳定透明,不是分散系
B.冰水混合物是一种分散系
C.分散系有的是纯净物有的是混合物
D.分散系都是混合物,按分散质和分散剂所处的状态,分散系的组合有9种方式
查看答案和解析>>
科目:高中化学 来源:2014-2015学年河北省高二上学期第三次月考化学试卷(解析版) 题型:填空题
(10分)在80℃时,将0.40 mol的N2O4气体充入2 L已经抽空的固定容积的密闭容器中,发生如下反应:N2O4 2NO2,隔一段时间对该容器内的物质进行分析,得到如下数据:
2NO2,隔一段时间对该容器内的物质进行分析,得到如下数据:
时间/s n/mol | 0 | 20 | 40 | 60 | 80 | 100 |
n(N2O4) | 0.40 | a | 0.20 | c | d | e |
n(NO2) | 0.00 | 0.24 | b | 0.52 | 0.60 | 0.60 |
(1)计算20~40 s内用N2O4表示的平均反应速率为________。
(2)计算在80℃时该反应的平衡常数K=________(请注明单位)。
(3)反应进行至100 s后将反应混合物的温度降低,混合气体的颜色________(填“变浅”、“变深”或“不变”)。
(4)要增大该反应的K值,可采取的措施有________(填序号)。
A.增大N2O4的起始浓度
B.向混合气体中通入NO2
C.使用高效催化剂
D.升高温度
(5)下图是80℃时容器中N2O4物质的量的变化曲线,
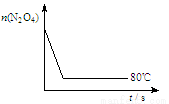
请在该图中补画出该反应在60℃时N2O4物质的量的变化曲线。
查看答案和解析>>
科目:高中化学 来源:2014-2015学年河北省唐山市高二上学期第一次月考化学试卷(解析版) 题型:选择题
高铁酸盐在能源、环境保护等有着广泛的用途,可以用电解法制高铁酸盐(已知高铁酸盐在酸性条件下不稳定),总反应式为Fe+2H2O+2OH- 3H2↑+FeO
3H2↑+FeO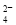 。下列说法正确的是
。下列说法正确的是
A.铁为阳极,H2SO4为电解液
B.铁为阴极,浓NaOH为电解液
C.阳极发生的电极反应为Fe+8OH--6e-===4H2O+FeO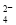
D.铁失去3 mol电子可以在阴极得到33.6 L氢气
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com