
已知:
CH3CH2CH2CH3(g)+6.5O2(g) = 4CO2(g)+5H2O(l) △H =-2878 kJ/mol
(CH3)2CHCH3(g)+6.5O2(g) = 4CO2(g)+5H2O(l) △H =-2869 kJ/mol
下列说法正确的是( )
A.正丁烷的稳定性大于异丁烷
B.异丁烷分子中的碳氢键比正丁烷的多
C.等物质的量的正丁烷能量大于异丁烷能量
D.异丁烷转化为正丁烷的过程是一个放热过程
科目:高中化学 来源: 题型:
已知:2Fe+3Cl2 2FeCl3,下列说法正确的是(设NA为阿伏加德罗常数的值)
2FeCl3,下列说法正确的是(设NA为阿伏加德罗常数的值)
A.氯气是氧化剂,FeCl3是还原剂
B.常温下,与56g Fe反应断裂1.5NA个Cl-Cl键
C.1 L 0.1 mol·L-1 FeCl3溶液中含有0.1NA个Fe3+
D.常温常压下,22.4 L Cl2和足量Fe反应转移3NA个电子
查看答案和解析>>
科目:高中化学 来源: 题型:
现有浓度均为0.1 mol·L-1的下列溶液:①硫酸 ②醋酸 ③氢氧化钠 ④氯化铵
请回答下列问题:
(1)四种溶液中由水电离出的H+浓度由大到小的顺序是(填序号)_____________________ _____________________________________。
(2)将③和④等体积混合后,混合液中各离子浓度由大到小的顺序是__________________________________________________。
(3)已知T ℃,KW=1×10-13,则T ℃________25 ℃(填“>”、“<”或“=”)。在T ℃时将pH=11的NaOH溶液a L与pH=1的硫酸b L混合(忽略混合后溶液体积的变化),若所得混合溶液的pH=10,则a∶b=________。
(4)25 ℃时,有pH=x的盐酸和pH=y的氢氧化钠溶液(x≤6,y≥8),取a L该盐酸与b L该氢氧化钠溶液反应,恰好完全中和,求:
①若x+y=14,则a/b=________(填数据);
②若x+y=13,则a/b=________(填数据);
③若x+y>14,则a/b=________(填表达式);
④该盐酸与该氢氧化钠溶液完全中和,两溶液的pH(x、y)的关系式为________(填表达式)。
查看答案和解析>>
科目:高中化学 来源: 题型:
如图所示,U型管的左端被水和胶塞封闭有甲烷和氯气(体积比为1:4)的混和气体,假定氯气在水中溶解度可以忽略。将封闭有甲烷和氯气的混和气体的装置放置在有光亮的地方,让混和气体缓慢的反应一段时间。
(1)假设甲烷与氯气反应充分,且只产生一种有机物,请写出化学方程式: 。
(2)经过几个小时的反应后,U型管右端的玻璃管中水柱变化是 。
A.升高 B.降低 C.不变 D.无法确定
(3)甲烷通常用来作燃料,其燃烧反应的化学方程式是
。
(4)若用甲烷—氧气构成燃料电池,电解质溶液为KOH溶液,试写出该电池的正极的电极反应式 ;负极的电极反应式 。
查看答案和解析>>
科目:高中化学 来源: 题型:
氢能是一种既高效又清洁的新能源,发展前景良好,用氢作能源的燃料电池汽车倍受青睐。我国拥有完全自主知识产权的氢燃料电池轿车“超越三号”,已达到世界先进水平,并加快向产业化的目标迈进。氢能具有的优点包括( )
①原料来源广;②易燃烧、热值高;③储存方便;④制备工艺廉价易行
A.③④ B.①② C.①③ D.②④
查看答案和解析>>
科目:高中化学 来源: 题型:
在容积不变的密闭容器中进行如下反应:N2+3H2 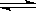 2NH3,若将平衡体系中各物质的浓度都增加到原来的2倍,则产生的结果是( )
2NH3,若将平衡体系中各物质的浓度都增加到原来的2倍,则产生的结果是( )
①平衡不发生移动;②平衡向正反应方向移动;③平衡向逆反应方向移动;
④NH3的质量分数增加;⑤正逆反应速率都增大。
A.①⑤ B.③④ C.②④ D.②④⑤
查看答案和解析>>
科目:高中化学 来源: 题型:
50℃和1.01×105 Pa时,该反应能自发进行:2N2O5(g) = 4NO2(g) + O2(g) △H= +56.76 kJ/mol,其自发进行的原因是( )
A.是吸热反应
B.是放热反应
C.是熵减少的反应
D.熵增大效应大于能量效应
查看答案和解析>>
科目:高中化学 来源: 题型:
工业上制备纯硅反应的热化学方程式如下:SiCl4(g)+2H2(g) Si(s)+4HCl(g);△H=+QkJ/mol(Q>0) 某温度、压强下,将一定量反应物通入密闭容器进行以上反应(此条件下为可逆反应),下列叙述正确的是 ( )
Si(s)+4HCl(g);△H=+QkJ/mol(Q>0) 某温度、压强下,将一定量反应物通入密闭容器进行以上反应(此条件下为可逆反应),下列叙述正确的是 ( )
A. 反应过程中,若增大压强能提高SiCl4的转化率
B. 若反应开始时SiCl4为1mol,则达平衡时,吸收热量为QkJ
C. 升高温度 ,反应重新达平衡后,HCl的体积分数不变
D. 当反应吸收热量为0.025QkJ时,生成的HCl通入100mL 1mol/L的NaOH溶液恰好反应
查看答案和解析>>
科目:高中化学 来源: 题型:
用pH试纸测定无色溶液的pH时,规范的操作是
A.将pH试纸放入溶液中观察其颜色变化,跟标准比色卡比较
B.将溶液倒在pH试纸上,跟标准比色卡比较
C.用干燥的洁净玻璃棒蘸取溶液,滴在pH试纸上,跟标准比色卡比较
D.在试管内放入少量溶液,煮沸,把pH试纸放在管口,观察颜色,跟标准比色卡比
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com