
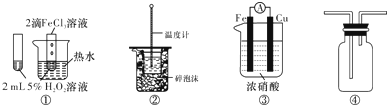
| A. | 图①可验证FeCl3对H2O2分解反应有催化作用 | |
| B. | 图②可用于中和热的测定 | |
| C. | 图③可用于探究铁作负极的原电池原理 | |
| D. | 图④可用于收集NH3 |
分析 A.温度、催化剂均加快反应速率;
B.缺少环形搅拌器,难测定反应最高温度;
C.Fe遇浓硝酸发生钝化,Cu为负极;
D.氨气的密度比空气的密度小.
解答 解:A.滴加FeCl3溶液的试管不要放在热水中,否则温度也会影响速率,不能验证FeCl3对H2O2分解反应有催化作用,故A错误;
B.缺少环形搅拌器,而且小烧杯应该和大烧杯杯口平齐,否则散热较大,数据不准,故B错误;
C.常温下Fe遇浓HNO3钝化,故无法探究,故C错误;
D.氨气利用向下排空气法收集,NH3可从右进,左出,故D正确;
故选D.
点评 本题考查化学实验方案的评价,为高频考点,侧重于学生的分析、实验能力的考查,题目难度不大,注意把握反应速率、中和热测定及物质的性质为解答的关键,学习中注意相关基础知识的积累.


 小学夺冠AB卷系列答案
小学夺冠AB卷系列答案科目:高中化学 来源: 题型:多选题
| A. | 常温常压下,16 g O3中含有质子总数为8NA | |
| B. | 25℃时,1 mL纯水中含有OH-离子数目为10-10 | |
| C. | pH=2的醋酸稀释10倍后,溶液中H+数目大于0.001NA | |
| D. | 1molCl2与足量NaOH溶液反应,转移的电子数为2NA |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 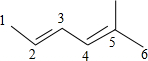 :5-甲基-2,4-己二烯 :5-甲基-2,4-己二烯 | B. |  1,2,3,4-四甲基环己烷 1,2,3,4-四甲基环己烷 | ||
| C. |  :1,3,4-三甲基苯 :1,3,4-三甲基苯 | D. |  :3-甲基-2-乙基戊烷 :3-甲基-2-乙基戊烷 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
| 投料比 CO的体积分数% 温度/℃ | $\frac{n({H}_{2}O)}{n(CO)}$=1 | $\frac{n({H}_{2}O)}{n(CO)}$=3 | $\frac{n({H}_{2}O)}{n(CO)}$=5 |
| 200 250 300 350 | 1.70 2.73 6.00 7.85 | 0.21 0.30 0.84 1.52 | 0.02 0.06 0.43 0.80 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:解答题

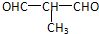 +4Cu(OH)2+2NaOH$\stackrel{△}{→}$NaOOCCH(CH3)COONa+2Cu2O↓+6H2O.
+4Cu(OH)2+2NaOH$\stackrel{△}{→}$NaOOCCH(CH3)COONa+2Cu2O↓+6H2O.查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 将洁厕灵与84消毒液混合使用,能更有效的起到洁具除垢和卫生消毒作用 | |
| B. | 二氧化硫、氮氧化物和可入肺颗粒物是雾霾的主要成分,PM2.5就是指大气中直径小于或等于2.5微米的可入肺颗粒物 | |
| C. | 屠呦呦最早提出用乙醚提取青蒿,其提取物抗疟作用达95%到100%,这种提取原理就是蒸馏,属于物理过程 | |
| D. | 不锈钢具有较强的抗腐蚀性,是因为在钢铁表面镀上了金属铬 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 0.125 | B. | 0.10 | C. | 0.08 | D. | 0.20 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题

查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com