
����Ŀ��ʵ��������������ˮ���������Ҵ��Ʊ�1��2�����������װ����ͼ��ʾ�� 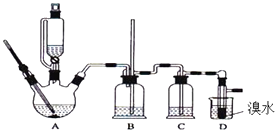
�Ҵ� | 1��2�������� | ���� | |
״̬ | ��ɫҺ�� | ��ɫҺ�� | ��ɫҺ�� |
�ܶ�/gcm��3 | 0.79 | 2.2 | 0.71 |
�е�/�� | 78.5 | 132 | 34.6 |
�۵�/�� | ��130 | 9 | ��116 |
��ش��������⣺
��1��д���Ʊ�1��2��������ķ�Ӧԭ������ʽ����
��2���ڴ��Ʊ�ʵ���У�Ҫ������Ѹ�ٵذѷ�Ӧ�¶����ߵ�170�����ң�����Ҫ��Ŀ����������ţ���
a��������Ӧ b���ӿ췴Ӧ�ٶ�c����ֹ�Ҵ��ӷ� d�����ٸ�������������
��3��װ��B�������� ��
��4����װ��C��Ӧ����������ţ�����Ŀ�������շ�Ӧ�п������ɵ��������壮
a��ˮb��Ũ����c������������Һd������̼��������Һ
��5���жϸ��Ʊ���Ӧ�Ѿ�������������� ��
��6����1��2��������ֲ�Ʒ���ڷ�Һ©���У���ˮ���ã�����Ӧ������ϡ����¡����㣮
��7�������������������������ѣ������ķ�����ȥ��
���𰸡�
��1��CH3CH2OH ![]() CH2=CH2��+H2O��CH2�TCH2+Br2��BrCH2CH2Br
CH2=CH2��+H2O��CH2�TCH2+Br2��BrCH2CH2Br
��2��d
��3���ж�װ���Ƿ����
��4��c
��5��D����ˮ����ɫ��ȫ��ȥ
��6����
��7������
���������⣺��1���Ʊ�1��2��������ķ�Ӧԭ������ʽ��CH3CH2OH ![]() CH2=CH2��+H2O��CH2�TCH2+Br2��BrCH2CH2Br���Դ��ǣ�CH3CH2OH
CH2=CH2��+H2O��CH2�TCH2+Br2��BrCH2CH2Br���Դ��ǣ�CH3CH2OH ![]() CH2=CH2��+H2O�� CH2�TCH2+Br2��BrCH2CH2Br����2���Ҵ���Ũ����140��������£�������������ˮ�������ѣ�����Ѹ�ٵذѷ�Ӧ�¶���ߵ�170�����ң�������ҪĿ���ǣ����ٸ������������ɣ�
CH2=CH2��+H2O�� CH2�TCH2+Br2��BrCH2CH2Br����2���Ҵ���Ũ����140��������£�������������ˮ�������ѣ�����Ѹ�ٵذѷ�Ӧ�¶���ߵ�170�����ң�������ҪĿ���ǣ����ٸ������������ɣ�
���Դ��ǣ�d����3�����D�е����ܷ��������¹ʣ�A�в�������ϩ����ᵼ��װ��B��ѹǿ��������Һ�������������װ��B�г�������E������Ϊ�ж�װ���Ƿ������
���Դ��ǣ��ж�װ���Ƿ��������4��Ũ���������ˮ�ԡ���ˮ�Ժ�ǿ�����ԣ��������Ҵ���CH3CH2OH+4H2SO4��Ũ�� ![]() 4SO2��+CO2��+7H2O+C���������ɵ���������Ϊ������������̼��������̼��ˮ���ܽ��С��������ز������ն�����̼��Ũ����Ȳ������ն�����̼��Ҳ�������ն�����������̼�����������ܺ�����������Һ��Ӧ��SO2+2NaOH=Na2SO3+H2O��CO2+2NaOH�TNa2CO3+H2O��
4SO2��+CO2��+7H2O+C���������ɵ���������Ϊ������������̼��������̼��ˮ���ܽ��С��������ز������ն�����̼��Ũ����Ȳ������ն�����̼��Ҳ�������ն�����������̼�����������ܺ�����������Һ��Ӧ��SO2+2NaOH=Na2SO3+H2O��CO2+2NaOH�TNa2CO3+H2O��
���Դ��ǣ�c����5��Һ��Ϊ����ɫ������1��2����������Ϊ��ɫ������Ӧ����ʱҺ��ȫ��ת��Ϊ1��2���������飬D��Һ���ɺ���ɫ��Ϊ��ɫ
���Դ��ǣ�D����ˮ����ɫ��ȫ��ȥ����6��1��2�����������ˮ�����ܣ�1��2�����������ܶȱ�ˮ�����Լ�ˮ�����ã�����Ӧ���²㣬
���Դ��ǣ��£���7��1��2���������������ѵķе㲻ͬ�����߾�Ϊ�л�����ܣ�������ķ��������Ƿ��룬
���Դ��ǣ�����



| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ���ִ��������Ŵ���ܳ��õ�Ƽӹ��ɵĹ�ͭɫӲ�����죮ȡӲ����Ʒ������ͼ��ʾ��ʵ�飨ÿһ���Լ������������ɴ˿���֪��Ӳ�������Ϊ�� �� 
A.Al��Cu��Mg��Si
B.Al��Mg��Si��Zn
C.Al��Fe��C��Cu
D.Al��Si��Zn��Na
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ�������й����ʵ���������;���ж�Ӧ��ϵ����
A.SO2ˮ��Һ�����ԣ�������Ư��ֽ��B.������۵�ߣ����ư뵼�����
C.Al(OH)3�������ԣ�����������θ�����D.H2O2���л�ԭ�ԣ�����������ɱ��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��A��B�Ľṹ��ʽ��ͼ�� 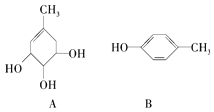
��1��A�����к��еĹ����ŵ���������B�����к��еĹ����ŵ������� ��
��2��A�ܷ�������������Һ��Ӧ��B�ܷ�������������Һ��Ӧ ��
��3��A��һ�������¿ɵõ�B���䷴Ӧ���ͺ������ֱ����� ��
��4��A��B��1mol�ֱ����������ˮ����ȫ��Ӧ�����ĵ���������ʵ����ֱ���mol��mol��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ�����������г����IJ��Ͽ��Խ��кܶ��ѧʵ�飬����������һЩ��ʵ��Ӧ�ü�ֵ��װ��������ͼ����һ���÷Ͼɲ��������Ŀ�����������ߵĵ�ص�ʾ��ͼ��������ع���ʱ���й�˵����ȷ���ǣ� �� 
A.��������ʴ
B.̼����̿���Ϸ����ķ�ӦΪ��O2+4e��=2O2��
C.̿��Ӧ����ߵ���ĸ�������
D.�õ�ع���һ��ʱ���̿����̿�������������
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ����֪�¶�Tʱ��ˮ�����ӻ�����ΪKw�����¶��£���Ũ��Ϊa molL��1��һԪ��HA��Һ��b molL��1��һԪ��BOH��Һ�������ϣ����жϸ���Һһ�������Ե������ǣ� ��
A.�����Һ��PH=7
B.�����Һ�У�C��H+��= ![]() mol?L��1
mol?L��1
C.a=b
D.�����Һ�У�C��H+��+C��B+��=C��OH����+C��A����
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ���ͻ��������Ϻ���ij�ְ�ɫǦ������������ڿ����г�ʱ���ͻ��ɺ�ɫPbS���Ӷ�ʹ�ͻ���ɫ�ʱ䰵������˫��ˮH2O2����ϴ����ɽ�PbS���PbSO4���Ӷ�ʹ�ͻ���ԭ��������ϴ��Ӧ�Ļ�ѧ����ʽΪ PbS+ 4H2O2 = PbSO4 + 4M������ƽ��
��1��������M�Ļ�ѧʽΪ_________________________
��2���ڴ˷�Ӧ�У�PbS�� _____________����H2O2�� _____________��
��3��������ת�Ƶĵ�����Ŀ2molʱ���μӷ�Ӧ��H2O2������Ϊ ___________ ��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��ijϩ���⻯��õ��ı������� ![]() ����ԭϩ�������еĽṹ��ʽ�У� ��
����ԭϩ�������еĽṹ��ʽ�У� ��
A.1��
B.2��
C.3��
D.4��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
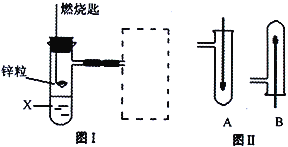
����Ŀ����1��ͼ����ʵ������H2��ԭCuOʵ��ļ���װ�ã����е�ͭ��ȼ�ճ������Թ��������ƶ������߿������ͼ����ѡȡװ�á�ͼ���е�ϸͭ˿һ�˱��������״��ʵ��ʱ�����ھƾ��ƻ����ϼ��ȣ���ں���Ѹ�������Ƶõ�H2�С�
����ͼ���У�X��ҺӦѡ��______��
A��ϡ���� B��Ũ���� C��NaCl��Һ
����ͼ�����߿��У�Ӧѡ��ͼ���е�_______����A��B��װ�á�
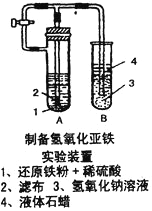
��2��ijѧ�������һ����ȡ������������ʵ�鷽����ʵ��װ�ü�����ͼ,�����ʵ����̣�
����B�Թ��м���NaOH��Һ��������l��2���Ӳ���������2mLҺ��ʯ�������������м�����е�Ŀ���ǣ�_____________________________��
���ھ�֧�Թ�A�м���ϡH2SO4��Һ�������������ۣ�����Ϊʲô����Ҫ����_____________��
�����Ӻõ��ܣ�ͬʱ��˨����������ϡ���ᷴӦƽ��ʱ���رջ�˨����ʱ����A�Թ���_________��������B�Թ���_________��������
�����B�в����������������������������ֵ�������_______________�������仯�Ļ�ѧ����ʽΪ_____________��
��3�����л�������SO2���ʵ�CO2���壬��ѡ���ʵ���ʵ��װ�ã��ռ����������CO2���塣
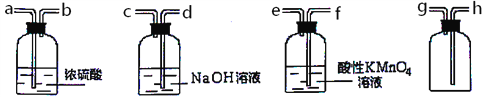
��Ҫ�ﵽʵ��Ŀ�ģ������������ң����ӿ�����˳����ȷ����_______��
A��dcabh B��feabh C��feabg
�ڱ�ʵ���ȥSO2��ԭ��������SO2��________���ʣ�����ţ���
A�������� B��Ư���� C����ԭ�� D������
��SO2�����Ը�����ط�Ӧ�����ӷ���ʽ��__________________��
�鿴�𰸺ͽ���>>
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com