
下列有关实验的叙述正确的是( )
-A.-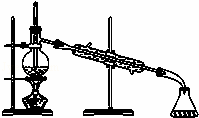
实验室蒸馏石油
-B.-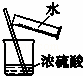
实验室稀释浓硫酸
-C.-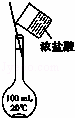
配制100 mL 0.1 mol•L﹣1 的盐酸
-D.-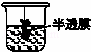
可用于分离或提纯胶体
考点:-化学实验方案的评价.
分析:-A.蒸馏时测定馏分的温度;
B.稀释时,将密度大的液体注入密度小的液体中,便于混合;
C.浓盐酸应在烧杯中稀释、冷却后再转移;
D.胶体不能透过半透膜,而离子可以.
解答:-解:A.蒸馏时测定馏分的温度,则图中温度计的水银球应在烧瓶支管口处,故A错误;
B.稀释时,将密度大的液体注入密度小的液体中,便于混合,则图中应将浓硫酸注入水中,故B错误;
C.浓盐酸应在烧杯中稀释、冷却后再转移,不能将浓盐酸直接注入容量瓶中,故C错误;
D.胶体不能透过半透膜,而离子可以,则图中渗析操作合理,故D正确;
故选D.
点评:-本题考查化学实验方案的评价,为高频考点,涉及实验基本操作、混合物分离提纯等,把握实验基本技能及混合物分离方法为解答的关键,侧重分析与实验能力的考查,题目难度不大.


 学而优衔接教材南京大学出版社系列答案
学而优衔接教材南京大学出版社系列答案 小学课堂作业系列答案
小学课堂作业系列答案 金博士一点全通系列答案
金博士一点全通系列答案科目:高中化学 来源: 题型:
已知1g氢气完全燃烧生成水蒸气时放出热量121kJ,且氧气中1mol O═O键完全断裂时吸收热量496kJ,水蒸气中1mol H﹣O键形成时放出热量463kJ,则氢气中1mol H﹣H键断裂时吸收热量为()
A. 188kJ B. 436 kJ C. 557 kJ D. 920 kJ
查看答案和解析>>
科目:高中化学 来源: 题型:
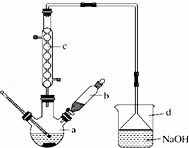
溴苯是一种化工原料,实验室合成溴体的装置示意图及有关数据如下:
苯 溴 溴苯
密度/g•cm﹣3 0.88 3.10 1.50
沸点/℃ 80 59 156
水中溶解度 微溶 微溶 微溶
按下列合成步骤回答问题:
(1)在a中加入15mL无水苯和少量铁屑.在b中小心加入4.0mL液态溴.向a中滴入几滴溴,有白色烟雾产生,是因为生成了 气体.继续滴加至液溴滴完.装置d的作用是 ;
(2)液溴滴完后,经过下列步骤分离提纯:
①向a中加入10mL水,然后过滤除去未反应的铁屑;
②滤液依次用10mL水、8mL 10%的NaOH溶液、10mL水洗涤.NaOH溶液洗涤的作用是 ;
③向分出的粗溴苯中加入少量的无水氯化钙,静置、过滤.加入氯化钙的目的是 ;
(3)经以上分离操作后,粗溴苯中还含有的主要杂质为苯,要进一步提纯,下列操作中必须的是 ;(填入正确选项前的字母)
A.重结晶 B.过滤 C.蒸馏 D.萃取
(4)在该实验中,a的容积最适合的是 .(填入正确选项前的字母)
A.25mL B.50mL C.250mL D.500mL.
查看答案和解析>>
科目:高中化学 来源: 题型:
影响化学反应速率与平衡的因素有多方面,如浓度压强温度催化剂等.下列有关说法不正确的是( )
|
| A. | 其它条件不变时,改变压强能改变气体反应的速率,但不一定改变平衡 |
|
| B. | 增大浓度能加快化学反应速率,原因是增大浓度就增加了反应体系中活化分子的百分数 |
|
| C. | 温度升高使化学反应速率加快的主要原因是增加了反应体系中活化分子的百分数 |
|
| D. | 加入催化剂能降低反应所需的活化能,使反应速率加快,平衡常数增大 |
查看答案和解析>>
科目:高中化学 来源: 题型:
下列说法正确的是( )
-A.-硫酸和磷酸的摩尔质量相等
-B.-摩尔质量越大,物质的质量越大
-C.-HNO3的摩尔质量是63g
-D.-摩尔质量就等于该物质的相对分子质量
查看答案和解析>>
科目:高中化学 来源: 题型:
对1mol•L﹣1的MgCl2溶液的有关叙述中,正确的是( )
-A.-该溶液中Cl﹣浓度为2 mol•L﹣1
-B.-该溶液中Mg2+的物质的量是1 mol
-C.-可使用250 mL容量瓶分两次完成490 mL该浓度的MgCl2溶液的配制
-D.-该溶液可由95g MgCl2•6H2O固体在水中溶解并稀释至1L获得
查看答案和解析>>
科目:高中化学 来源: 题型:
海水是巨大的资源宝库.如图1是从海水中提取食盐和溴的主要流程.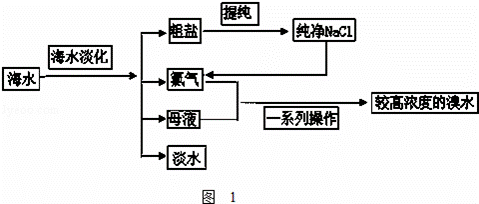
(1)粗盐除含NaCl外,还含有少量MgCl2、CaCl2、Na2SO4以及泥沙等杂质.如图2是粗盐提纯的操作流程.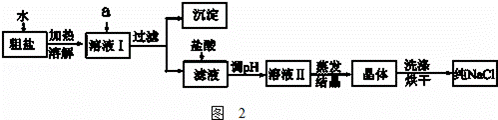
提供的试剂:Na2CO3溶液、K2CO3溶液、NaOH溶液、BaCl2溶液、Ba(NO3)2溶液、饱和NaCl溶液.
①除去溶液I中的MgCl2、CaCl2、Na2SO4,从提供的试剂中选出a所代表的试剂,按滴加顺序依次为:过量的NaOH溶液、 、
②如何证明操作①中NaOH溶液已经过量?
③蒸发过程所用的主要仪器有:铁架台、酒精灯、 ;
某同学欲四氯化碳萃取较高浓度的溴水中的溴,经振荡并在铁架台上静置分层后,
①分离出四氯化碳层的操作: .②分离碘的四氯化碳溶液的操作方法是:
(3)工业上将较高浓度的溴水经进一步处理得到工业溴.某研究性学习小组为了解从工业溴中提纯溴的方法,查阅了有关资料,Br2的沸点为 59℃,微溶于水,有毒性和强腐蚀性.水的沸点为100℃.他们参观生产过程后,设计了如图3装置简图: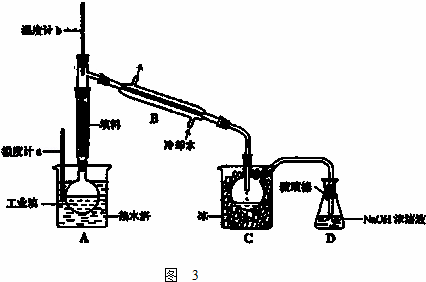
①图中仪器B的名称: .
②用热水浴加热的优点是: .
③实验装置气密性良好,要达到提纯溴的目的,收集溴时温度计应控制的温度为: .
查看答案和解析>>
科目:高中化学 来源: 题型:
下列各溶液中,Na+浓度最大的是( )
|
| A. | 5L 1.2mol•L﹣1的Na2SO4溶液 |
|
| B. | 2L 0.8mol•L﹣1的NaOH溶液 |
|
| C. | 1L 1mol•L﹣1的Na2CO3溶液 |
|
| D. | 4L 0.5mol•L﹣1的NaCl溶液 |
查看答案和解析>>
科目:高中化学 来源: 题型:
(1)同温同压下,同体积的甲烷(CH4)和二氧化碳分子数之比为 ,物质的量之比为 ,原子总数之比为 ,密度之比为 .
(2)在标准状况下,4g H2、11.2L O2、1mol H2O中,所含分子数最多的是 ,含原子数最多的是 ,体积最小的是 .
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com