
����Ŀ����ͼΪԪ�����ڱ���һ���֣������NԪ�ص�λ�ã��ش��������⣺
�� | N | |||||||
�� | �� | �� | �� |
��ش��������⣺
(1)д����4���ڡ����ͬ��Ԫ�ص����ƣ�___________��
(2)�ٵĵ��ʱ���Ϊ��21���͵���Դ�������������������غʹ������������⻯�������ˮ��Ӧ�������������⻯�����ʽΪ___________��д�����⻯����ˮ��Ӧ�Ļ�ѧ����ʽ_____________________��
(3)��(Ga)���ͬ���壬д���ص���������NaOH��Ӧ�Ļ�ѧ����ʽΪ____________��
(4)��Ԫ�صķǽ����ԱȢ�______(����ǿ����������)���о�һ����ѧ��ʵ����˵��_______________________________________________��
(5)NԪ�ش���N2��N4��ͬ�������塣��֪N4Ϊ��������ṹ��N��N����Ϊ167 kJ��mol-1��N��N����Ϊ942 kJ��mol-1��д��N4(g)ת��ΪN2(g)���Ȼ�ѧ����ʽ��______________________________________��
���𰸡�� ![]() LiH+H2O ��H2��+ LiOH Ga2O3 + 2OH- �� 2GaO2-+H2O �� ���ԣ�H2SO4��HClO4(���ȶ��ԣ�H2S��HCl�ȣ���������) N4(g)�� 2N2(g) ��H=-882 kJ��mol-1
LiH+H2O ��H2��+ LiOH Ga2O3 + 2OH- �� 2GaO2-+H2O �� ���ԣ�H2SO4��HClO4(���ȶ��ԣ�H2S��HCl�ȣ���������) N4(g)�� 2N2(g) ��H=-882 kJ��mol-1
��������
����Ԫ�������ڱ��е�λ�ÿ��жϸ�Ԫ��Ϊ��Li��Al��S��Cl��Ar
��1����4�������Arͬ��Ԫ�ص����ƣ�봣�
��2���⻯﮿�����ˮ��Ӧ�������������⻯�����ʽΪ![]() ��
��
��3��ģ���������������ķ�Ӧ��д��Ga2O3 �� OH- ��Ӧ����GaO2-�����ӷ���ʽ��
��4��ͬһ���ڴ����ҷǽ���������ǿ���ɴ����������ˮ��������ǿ������H2���ϵ����Ѽ������⻯���ȶ��Եȶ��Ƚϡ�
��5���÷�Ӧ�ʱ�=��Ӧ�����-��������ܣ��ݴ���д�Ȼ�ѧ����ʽ��
��1����4�������Arͬ��Ԫ�ص����ƣ�봣�
��2���⻯﮵���ʽΪ![]() ���⻯﮿�����ˮ��Ӧ����������������ﮣ���ѧ����ʽ��LiH+H2O��H2��+ LiOH ��
���⻯﮿�����ˮ��Ӧ����������������ﮣ���ѧ����ʽ��LiH+H2O��H2��+ LiOH ��
��3��ģ���������������ķ�Ӧ��д��Ga2O3 �� OH- ��Ӧ����GaO2-�����ӷ���ʽ��Ga2O3 + 2OH- �� 2GaO2-+H2O��
��4��ͬһ���ڴ����ҷǽ���������ǿ��S�ǽ�����С��Cl�����ԣ�H2SO4��HClO4���ȶ��ԣ�H2S��HCl�Ⱦ���˵����
��5���÷�Ӧ�ʱ�=��Ӧ�����-���������=6��167kJ��mol��1-2��942kJ��mol��1=-882kJ��mol��1����÷�Ӧ�Ȼ�ѧ����ʽΪN4��g��=2N2��g����H=-882 kJ��mol��1��


 �����������Ů��ͯ������ϵ�д�
�����������Ů��ͯ������ϵ�д�
| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ�������£����и���������ָ����Һ���ܴ����������(����)
A. 0.1 mol��L��1KI��Һ��Na����K����ClO����OH��
B. 0.1 mol��L��1Fe2(SO4)3��Һ��Cu2����N![]() ��N
��N![]() ��S
��S![]()
C. 0.1 mol��L��1HCl��Һ��Ba2����K����CH3COO����N![]()
D. 0.1 mol��L��1NaOH��Һ��Mg2����Na����S![]() ��HC
��HC![]()
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ������и�����������Һ�Ӵ�ֱ�ӷ�Ӧ�ή�͵�ص�����ת��Ч�ʣ���Ϊ�Էŵ�������ͼ��ʾ�����й��ڸɵ�غ�Ǧ���ص�˵���������

A. �ɵ��Ϊһ���Ե�Դ��Ǧ����Ϊ���ε�Դ
B. �ɵ����MnO2�ķŵ���������KMnO4
C. Ǧ���ش����Էŵ�����
D. Ǧ�����и�����ӦʽΪ��Pb��2e-��SO42-��PbSO4
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ������˵������ȷ���ǣ� ��
A��������H��0�ķ�Ӧ�����Է���Ӧ B���Է����еķ�Ӧһ����Ѹ�ٽ���
C�������������Զ��ۻ���ˮ���������Ĺ��� D��������ؼ��ȷֽ���һ���ؼ�С�Ĺ���
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ���ϳɰ��ķ�ӦΪN2(g)��3H2(g)![]() 2NH3(g)���±���ij�η�ӦʱNH3��Ũ�ȱ仯��
2NH3(g)���±���ij�η�ӦʱNH3��Ũ�ȱ仯��
ʱ��(min) | 0 | 5 | 10 | 15 | 20 | 25 |
c(NH3)(mol��L-1) | 0 | 0.30 | 0.44 | 0.50 | 0.50 | 0.53 |
����˵����ȷ����
A. 0��10 minʱ����H2��ʾ��ƽ����Ӧ����Ϊ0.044mol��L-1��min-1
B. ����ѹǿ�ͽ����¶Ⱦ��ܼӿ�ϳɰ��ķ�Ӧ����
C. ��ͼ����֪���÷�Ӧ��15��20 minʱ���ڻ�ѧƽ��״̬
D. ��Ӧ������������ܶȱ��ֲ��䣬˵���÷�Ӧһ���ﵽƽ��״̬
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��ij�����A������Al2(SO4)3��Al2O3��Fe2O3����һ�������¿�ʵ����ͼ��ʾ�ı仯��

��ش��������⡣
��1��ͼ���漰������Һ������ķ�����__________________��
��2��B��C��D��E 4�����ʵĻ�ѧʽΪ��B_________��C_________��D_________��E_________��
��3������F��NaOH��Һ��Ӧ�����ӷ���ʽΪ__________________________________������E��ϡ���ᷴӦ�����ӷ���ʽΪ__________________________________________����ҺG�����ϡ��ˮ��Ӧ�Ļ�ѧ����ʽΪ______________________________________��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ����CO2���建����ͨ�뵽��KOH��Ba(OH)2��K[Al(OH)4]�Ļ����Һ��ֱ�����������ɳ��������ʵ�������ͨCO2�������ϵ��ͼ��ʾ�����й���������Ӧ�����еĸ�����������ȷ����

A. o��a�η�Ӧ�Ļ�ѧ����ʽ�ǣ�Ba(OH)2 + CO2 = BaCO3��+ H2O
B. b��c�η�Ӧ�����ӷ���ʽ�ǣ�2[Al(OH)4]��+ CO2 = 2Al(OH)3�� +CO32��+ H2O
C. a��b����c��d���������ķ�Ӧ��ͬ
D. d��e�γ����ļ���������̼�ᱵ�������ʧ����
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ����ҵ�Ͽ����÷���м�Ʊ�����Fe3O4����������ͼ��

(1)���Ʊ������У�Ҫ����״����ԭ�Ϸ��顢ĥ�ɷ�ĩ��������________________________
(2)�ںϳɳ�������Fe3O4�����ӷ���ʽΪ__________________________
(3)�������̿�֪���������ĺܿ���ʹ������е�Fe2O3��Fe���ʵ���֮�Ƚӽ�________
(4)ijͬѧ���÷���м����Fe��Fe2O3������ȡFeCl3��6H2O���壬ͬʱ�ⶨ���������������������װ����ͼ���г�װ���ԣ��������Ѽ��飩��
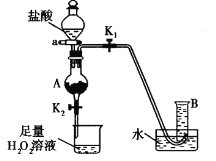
�����������£�
I�����ɼ�K1���رյ��ɼ�K2��������a�������μ����ᡣ
������ʱ���رյ��ɼ�K1���ɼ�K2����A����Һ��ȫ�����ձ���رջ���a��
���ձ�����Һ����Ũ������ȴ�ᾧ�����˺�õ�FeC13��6H2O���塣
��ش�
�� �������С���������������______________���ձ��е�������_________________���������ݲ�������Ӧ�ķ���ʽ��________________��________________���������ӷ�Ӧ��д���ӷ���ʽ��
�������������Ϊm g��ʵ���������B�����õ�������V mL����״��ʱ������ͬѧ�ɴ˼�����˷���м����������������![]() ������ֵ��ʵ����ֵƫ�ͣ���ʵ����̲�������ƫ�͵�ԭ����______________________��
������ֵ��ʵ����ֵƫ�ͣ���ʵ����̲�������ƫ�͵�ԭ����______________________��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ����50mL 0.50 mol/L������50 mL 0.55 mol/L NaOH��Һ����ͼ��ʾ��װ���н����кͷ�Ӧ��ͨ���ⶨ��Ӧ���������ų��������ɼ����к��ȡ��ش��������⣺

��1���۲�ʵ��װ�ã�ͼ����ȱ�ٵ�һ�ֲ�����Ʒ��__________��
��2���ձ���������ֽ����������_________________________��
��3�����ձ��Ͽڲ���Ӳֽ�壬��õ��к�����ֵ __________������ƫ��ƫС����Ӱ��������
��4��ʵ���и���55mL 0.50 mol/L������55mL 0.55 mol/L NaOH��Һ���з�Ӧ��������ʵ����ȣ����ų�������__________ ��������ȡ�����������������к���__________ ��������ȡ������������
��5�����к��Ȳⶨʵ���У�������ͬŨ�Ⱥ�����İ�ˮ����NaOH��Һ����ʵ�飬��õ��к��ȵ���ֵ��____������ƫ��������ƫС������������ԭ����_____________��
�鿴�𰸺ͽ���>>
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com