
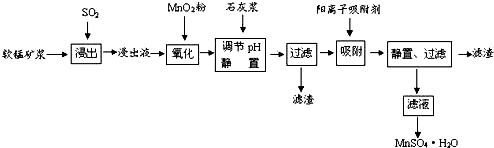

| Ąė×Ó | Ąė×Ó°ė¾¶£Øpm£© | æŖŹ¼³ĮµķŹ±µÄpH | ĶźČ«³ĮµķŹ±µÄpH |
| Fe2+ | 74 | 7.6 | 9.7 |
| Fe3+ | 64 | 2.7 | 3.7 |
| Al3+ | 50 | 3.8 | 4.7 |
| Mn2+ | 80 | 8.3 | 9.8 |
| Pb2+ | 121 | 8.0 | 8.8 |
| Ca2+ | 99 | - | - |
·ÖĪö øßĪĀ±ŗÉÕŗ¬Įņ·ĻŌü²śÉśµÄSO2·ĻĘų£¬ČķĆĢæ󽬵ÄÖ÷ŅŖ³É·ÖŹĒMnO2£¬ĶØČėSO2½ž³öŅŗµÄpH£¼2£¬ĘäÖŠµÄ½šŹōĄė×ÓÖ÷ŅŖŹĒMn2+£¬ŌņMnO2ÓėSO2·¢ÉśŃõ»Æ»¹Ō·“Ó¦£¬½ž³öŅŗ»¹ŗ¬ÓŠÉŁĮæµÄFe2+”¢Al3+µČĘäĖū½šŹōĄė×Ó£¬Fe2+¾ßÓŠ»¹ŌŠŌ£¬æÉŅŌ±»MnO2ŌŚĖįŠŌĢõ¼žĻĀŃõ»Æ³ÉFe3+£¬ŌŚŃõ»ÆŗóµÄŅŗĢåÖŠ¼ÓČėŹÆ»Ņ½¬£¬ŌÓÖŹÖŠŗ¬ÓŠFe2+”¢Al3+”¢Ca2+”¢Pb2+ĖÄÖÖŃōĄė×Ó£¬ÓɳĮµķµÄpH·¶Ī§ÖŖ£¬Fe2+µÄ³ĮµķÓėMn2+Ąė×ӵijĮµķĖłŠčµÄpH½Ó½ü£¬¶ųFe3+ŌņĻą²īŗÜŌ¶£¬¹ŹæÉŅŌ½«Fe2+Ńõ»Æ³ÉFe3+¶ų³żŌÓ£®“ÓĪüø½ĀŹµÄĶ¼æÉŅŌ擳ö£¬Ca2+”¢Pb2+µÄĪüø½ĀŹ½Ļøߣ¬¹ŹÖ»ŅŖµ÷½ŚpHÖµŌŚ4.7”«8.3¼ä£¬Fe3+”¢Al3+ŃōĄė×ÓĶعżµ÷pHÖµ£¬×Ŗ»ÆĪŖĒāŃõ»ÆĢś”¢ĒāŃõ»ÆĀĮ³Įµķ£¬Ķ¬Ź±Éś³ÉĪ¢ČܵÄĮņĖįøĘ£¬¹żĀĖ£¬ĀĖŌüÖ÷ŅŖÓŠĒāŃõ»ÆĢś”¢ĒāŃõ»ÆĀĮ”¢ĮņĖįøĘ£¬ÓÉÓŚÖĘČ”µÄMnSO4•H2Oŗ¬ÓŠ½į¾§Ė®£¬¹Ź²Ł×÷a²ÉÓĆÕō·¢ÅØĖõ½į¾§µÄ·½·Ø£¬µĆµ½MnSO4•H2O£¬
£Ø1£©“ÓĮ÷³ĢĶ¼æ“£¬½ž³ö¹ż³ĢŹĒČķĆĢæ󽬣ØMnO2£©ÓėSO2µÄ·“Ó¦£»
£Ø2£©ŌÓÖŹĄė×ÓÖŠÖ»ÓŠFe2+¾ßÓŠ»¹ŌŠŌ£¬æÉŅŌ±»MnO2ŌŚĖįŠŌĢõ¼žĻĀŃõ»Æ³ÉFe3+£»
£Ø3£©“Ó±ķæÉŅŌ擳ö£¬Ö»ŅŖµ÷½ŚpHÖµŌŚ4.7”«8.3¼ä£¬“óÓŚ4.7æÉŅŌ½«Fe3+ŗĶAl3+³żČ„£¬Š”ÓŚ8.3ŹĒ·ĄÖ¹Mn2+Ņ²³Įµķ£»
£Ø4£©½įŗĻ°ė¾¶£¬·ÖĪöÓŅĶ¼ÖŖ£¬Ķ¼ÖŠĄė×Ó“ÓÉĻÖĮĻĀ£¬°ė¾¶ÓŠ¼õŠ”Ē÷ŹĘ£¬¶ŌÓ¦µÄĪüø½ĀŹ¼õŠ”£®Ėę×ÅŹ±¼äµÄµŻŌö£¬ĖłÓŠĄė×ÓµÄĪüø½ĀŹ¾łŌö“ó£»ĮķFe3+ŗĶAl3+Ąė×ÓĖł“ųµēŗÉŹż“ó£¬ĘäĪüø½ĀŹµĶ£¬“ÓĪüø½ĀŹµÄĶ¼æÉŅŌ擳ö£¬Ca2+”¢Pb2+µÄĪüø½ĀŹ½Ļøߣ¬
£Ø5£©2.00”Į10-2 mol•L-1Na2SO4ČÜŅŗÖŠc£ØSO42-£©=2.00”Į10-2 mol•L-1£¬øł¾ŻKsp£ØCaSO4£©=c£ØCa2+£©•c£ØSO42-£©£¬æÉĒóµĆc£ØCa2+£©£¬½ų¶ųČ·¶ØcµÄÖµ£®
½ā“š ½ā£ŗøßĪĀ±ŗÉÕŗ¬Įņ·ĻŌü²śÉśµÄSO2·ĻĘų£¬ČķĆĢæ󽬵ÄÖ÷ŅŖ³É·ÖŹĒMnO2£¬ĶØČėSO2½ž³öŅŗµÄpH£¼2£¬ĘäÖŠµÄ½šŹōĄė×ÓÖ÷ŅŖŹĒMn2+£¬ŌņMnO2ÓėSO2·¢ÉśŃõ»Æ»¹Ō·“Ó¦£¬½ž³öŅŗ»¹ŗ¬ÓŠÉŁĮæµÄFe2+”¢Al3+µČĘäĖū½šŹōĄė×Ó£¬Fe2+¾ßÓŠ»¹ŌŠŌ£¬æÉŅŌ±»MnO2ŌŚĖįŠŌĢõ¼žĻĀŃõ»Æ³ÉFe3+£¬ŌŚŃõ»ÆŗóµÄŅŗĢåÖŠ¼ÓČėŹÆ»Ņ½¬£¬ŌÓÖŹÖŠŗ¬ÓŠFe2+”¢Al3+”¢Ca2+”¢Pb2+ĖÄÖÖŃōĄė×Ó£¬ÓɳĮµķµÄpH·¶Ī§ÖŖ£¬Fe2+µÄ³ĮµķÓėMn2+Ąė×ӵijĮµķĖłŠčµÄpH½Ó½ü£¬¶ųFe3+ŌņĻą²īŗÜŌ¶£¬¹ŹæÉŅŌ½«Fe2+Ńõ»Æ³ÉFe3+¶ų³żŌÓ£®“ÓĪüø½ĀŹµÄĶ¼æÉŅŌ擳ö£¬Ca2+”¢Pb2+µÄĪüø½ĀŹ½Ļøߣ¬¹ŹÖ»ŅŖµ÷½ŚpHÖµŌŚ4.7”«8.3¼ä£¬Fe3+”¢Al3+ŃōĄė×ÓĶعżµ÷pHÖµ£¬×Ŗ»ÆĪŖĒāŃõ»ÆĢś”¢ĒāŃõ»ÆĀĮ³Įµķ£¬Ķ¬Ź±Éś³ÉĪ¢ČܵÄĮņĖįøĘ£¬¹żĀĖ£¬ĀĖŌüÖ÷ŅŖÓŠĒāŃõ»ÆĢś”¢ĒāŃõ»ÆĀĮ”¢ĮņĖįøĘ£¬ÓÉÓŚÖĘČ”µÄMnSO4•H2Oŗ¬ÓŠ½į¾§Ė®£¬¹Ź²Ł×÷a²ÉÓĆÕō·¢ÅØĖõ½į¾§µÄ·½·Ø£¬µĆµ½MnSO4•H2O£¬
£Ø1£©µĶĘ·Ī»ČķĆĢæ󽬵ÄÖ÷ŅŖ³É·ÖŹĒMnO2£¬ĶØČėSO2½ž³öŅŗµÄpH£¼2£¬ĘäÖŠµÄ½šŹōĄė×ÓÖ÷ŅŖŹĒMn2+£¬ŌņMnO2ÓėSO2·¢ÉśŃõ»Æ»¹Ō·“Ó¦£¬·“Ó¦µÄ»Æѧ·½³ĢŹ½ĪŖSO2+MnO2=MnSO4£¬¹Ź“š°øĪŖ£ŗSO2+MnO2=MnSO4£»
£Ø2£©ŌÓÖŹĄė×ÓÖŠÖ»ÓŠFe2+¾ßÓŠ»¹ŌŠŌ£¬æÉŅŌ±»MnO2ŌŚĖįŠŌĢõ¼žĻĀŃõ»Æ³ÉFe3+£¬·“Ó¦µÄĄė×Ó·½³ĢŹ½ĪŖ2Fe2++MnO2+4H+=2Fe3++Mn2++2H2O£¬
¹Ź“š°øĪŖ£ŗ2Fe2++MnO2+4H+=2Fe3++Mn2++2H2O£»
£Ø3£©µ÷½ŚpHÖµÓƵ½µÄŅĒĘ÷ŹĒpH¼Ę£¬ŌÓÖŹÖŠŗ¬ÓŠFe3+”¢Al3+ŃōĄė×Ó£¬“ÓĶ¼æɱķŅŌ擳ö£¬“óÓŚ4.7æÉŅŌ½«Fe3+ŗĶAl3+³żČ„£¬Š”ÓŚ8.3ŹĒ·ĄÖ¹Mn2+Ņ²³Įµķ£¬ĖłŅŌÖ»ŅŖµ÷½ŚpHÖµŌŚ4.7”«8.3¼ä¼“æÉ£®
¹Ź“š°øĪŖ£ŗpH¼Ę£»4.7”ÜpH£¼8.3£»
£Ø4£©Ķ¼ÖŠĄė×Ó“ÓÉĻÖĮĻĀ£¬°ė¾¶ÓŠ¼õŠ”Ē÷ŹĘ£¬¶ŌÓ¦µÄĪüø½ĀŹ¼õŠ”£®Ėę×ÅŹ±¼äµÄµŻŌö£¬ĖłÓŠĄė×ÓµÄĪüø½ĀŹ¾łŌö“ó£»ĮķFe3+ŗĶAl3+Ąė×ÓĖł“ųµēŗÉŹż“ó£¬ĘäĪüø½ĀŹµĶ£¬ŌÓÖŹÖŠŗ¬ÓŠFe2+”¢Al3+”¢Ca2+”¢Pb2+ĖÄÖÖŃōĄė×Ó£¬ÓɳĮµķµÄpH·¶Ī§ÖŖ£¬Fe2+µÄ³ĮµķÓėMn2+Ąė×ӵijĮµķĖłŠčµÄpH½Ó½ü£¬¶ųFe3+ŌņĻą²īŗÜŌ¶£¬¹ŹæÉŅŌ½«Fe2+Ńõ»Æ³ÉFe3+¶ų³żŌÓ£®“ÓĪüø½ĀŹµÄĶ¼æÉŅŌ擳ö£¬Ca2+”¢Pb2+µÄĪüø½ĀŹ½Ļøߣ¬
¹Ź“š°øĪŖ£ŗĪüø½Ź±¼ä”¢½šŹōĄė×Ó°ė¾¶”¢½šŹōĄė×ÓµēŗÉ£»Pb2+”¢Ca2+£»
£Ø5£©c mol•L-1CaCl2ČÜŅŗÓė2.00”Į10-2 mol•L-1Na2SO4ČÜŅŗµČĢå»ż»ģŗĻ£¬»ģŗĻŗóNa2SO4µÄÅضČĪŖ1.00”Į10-2 mol•L-1£¬øł¾ŻKsp£ØCaSO4£©=c£ØCa2+£©•c£ØSO42-£©£¬æÉÖŖ»ģŗĻČÜŅŗÖŠc£ØCa2+£©=$\frac{Ksp£ØCaS{O}_{4}£©}{c£ØS{{O}_{4}}^{2-}£©}$=$\frac{9.10”Į1{0}^{-6}}{1.00”Į1{0}^{-2}}$ mol•L-1=9.10”Į10-4 mol•L-1£¬ĖłŅŌ»ģŗĻĒ°c=2”Į9.10”Į10-4 mol•L-1=1.82”Į10 -3mol•L-1£¬
¹Ź“š°øĪŖ£ŗ1.82”Į10 -3mol•L-1£®
µćĘĄ ±¾ĢāŅŌÖʱøĮņĖįĆĢµÄÉś²śĮ÷³ĢĪŖÖŖŹ¶ŌŲĢ壬漲é»Æѧ·“Ó¦µÄŹéŠ“£¬¼°³żŌÓÖŠµÄĪŹĢā£¬ĢāÄæÄѶČÖŠµČ£¬±¾Ģā×¢Ņā°ŃĪÕŹż¾Ż“¦ĄķÄÜĮ¦ŗĶĶ¼Ļó·ÖĪöÄÜĮ¦£®



| Äź¼¶ | øßÖŠæĪ³Ģ | Äź¼¶ | ³õÖŠæĪ³Ģ |
| øßŅ» | øßŅ»Ćā·ŃæĪ³ĢĶĘ¼ö£” | ³õŅ» | ³õŅ»Ćā·ŃæĪ³ĢĶĘ¼ö£” |
| ø߶ž | ø߶žĆā·ŃæĪ³ĢĶĘ¼ö£” | ³õ¶ž | ³õ¶žĆā·ŃæĪ³ĢĶĘ¼ö£” |
| øßČż | øßČżĆā·ŃæĪ³ĢĶĘ¼ö£” | ³õČż | ³õČżĆā·ŃæĪ³ĢĶĘ¼ö£” |
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗĢīæÕĢā
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ½ā“šĢā
 ĄūÓĆ·ĻĀĮ²£ØÖ÷ŅŖ³É·ÖĪŖAl”¢ÉŁĮæµÄFe”¢SiµČ£©¼ČæÉÖĘȔӊ»śŗĻ³É“߻ƼĮAlBr3ÓÖæÉÖĘČ”¾»Ė®¼ĮĮņĖįĀĮ¾§Ģå[A12£ØSO4£©3•18H2O]£®
ĄūÓĆ·ĻĀĮ²£ØÖ÷ŅŖ³É·ÖĪŖAl”¢ÉŁĮæµÄFe”¢SiµČ£©¼ČæÉÖĘȔӊ»śŗĻ³É“߻ƼĮAlBr3ÓÖæÉÖĘČ”¾»Ė®¼ĮĮņĖįĀĮ¾§Ģå[A12£ØSO4£©3•18H2O]£®²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗĢīæÕĢā
| Ź±¼ä£Ømin£© | 0 | 1 | 2 | 3 | 4 | 5 | 6 | 7 | 8 |
| n£ØA£© | 2.00 | 1.90 | 1.82 | 1.76 | 1.64 | 1.54 | 1.50 | 1.50 | 1.50 |
| n£ØB£© | 1.00 | 0.95 | 0.91 | 0.88 | 0.82 | 0.77 | 0.75 | 0.75 | 0.75 |
| n£ØC£© | 0 | 0.10 | 0.18 | 0.24 | 0.36 | 0.46 | 0.50 | 0.50 | 0.50 |

²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ½ā“šĢā

| ĪļÖŹ | ČŪµć/”ę | ·Šµć/”ę |
| PCl3 | -112 | 75.5 |
| POCl3 | 2 | 105.3 |
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗŃ”ŌńĢā
| A£® | X”¢Y”¢ZŠĪ³ÉµÄ»ÆŗĻĪļÖŠ²»æÉÄܼČÓŠĄė×Ó¼ü | |
| B£® | XŗĶZ”¢MŗĶY”¢ZŗĶW¾łæÉŠĪ³ÉŌ×ÓøöŹż±ČĪŖ1£ŗ1µÄ»ÆŗĻĪļ | |
| C£® | Y”¢Z”¢W”¢MŠĪ³ÉµÄ¼ņµ„Ąė×Ó°ė¾¶“󊔹ŲĻµĪŖY£¾Z£¾M£¾W | |
| D£® | WÓėClŠĪ³É»ÆŗĻĪļµÄČŪµćµĶÓŚMÓėClŠĪ³É»ÆŗĻĪļµÄČŪµć |
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ½ā“šĢā

²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗŃ”ŌńĢā
| A£® | Ė®µēĄėµÄc£Ø H+£©=1”Įl0-13 mol/LµÄČÜŅŗÖŠ£ŗK+”¢Na+”¢SiO32-”¢SO42- | |
| B£® | ÄÜŹ¹ŹÆČļ³ŹĄ¶É«µÄČÜŅŗÖŠ£ŗNa+”¢Fe3+”¢SO42-”¢Cl- | |
| C£® | $\frac{{K}_{W}}{c£ØO{H}^{-}£©}$=l”Įl0-13mol/LµÄČÜŅŗÖŠ£ŗBa2+”¢ClO-”¢Cl-”¢NO3- | |
| D£® | ÄÜÓėĀĮ·“Ó¦·Å³öH2µÄČÜŅŗÖŠ£ŗFe2+”¢K+”¢SO42-”¢Cl- |
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗŃ”ŌńĢā
| A£® | Na+”¢Mg2+”¢Br-”¢Ba2+ | B£® | Na+”¢SO32-”¢SO42-”¢K+ | ||
| C£® | K+”¢MnO4-”¢NO3-”¢Na+ | D£® | K+”¢Ca2+”¢SO32-”¢Cl- |
²éæ““š°øŗĶ½āĪö>>
°Ł¶ČÖĀŠÅ - Į·Ļ°²įĮŠ±ķ - ŹŌĢāĮŠ±ķ
ŗž±±Ź”»„ĮŖĶųĪ„·ØŗĶ²»Į¼ŠÅĻ¢¾Ł±ØĘ½ĢØ | ĶųÉĻÓŠŗ¦ŠÅĻ¢¾Ł±Ø×ØĒų | µēŠÅÕ©Ę¾Ł±Ø×ØĒų | É꥜Ź·ŠéĪŽÖ÷ŅåÓŠŗ¦ŠÅĻ¢¾Ł±Ø×ØĒų | ÉęĘóĒÖČؾŁ±Ø×ØĒų
Ī„·ØŗĶ²»Į¼ŠÅĻ¢¾Ł±Øµē»°£ŗ027-86699610 ¾Ł±ØÓŹĻä£ŗ58377363@163.com