
【题目】下列各组物质互为同系物的是 ( )
A. 硬脂酸和软脂酸 B. 乙酸和油酸
C. 丙酸丙酯和硬脂酸丙三酯 D. C6H5—CH2OH和C6H5—OH
科目:高中化学 来源: 题型:
【题目】镁-次氯酸盐电池的工作原理如图,该电池反应为:
Mg+ClO-+H20=Mg(0H)2+Cl-。下列有关说法正确的是

A.电池工作时,正极a附近的pH将不断增大
B.电池工作时,C溶液中的溶质是MgCl2
C.负极反应式:ClO- +2e- +H20 = Cl- +20H-
D.b电极发生还原反应,每转移0.2mol电子,理论上生成0.1 mol Cl-
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】聚乙炔能够导电,下列关于聚乙炔![]() 和聚合物A
和聚合物A![]() 的说法中正确的是
的说法中正确的是
A.两种聚合物的单体互为同系物
B.聚合物A不属于单双键交错的结构
C.聚合物A的相对分子质量是聚乙炔的两倍
D.1 mol两种聚合物的单体分别与Br2发生加成反应,最多消耗Br2的物质的量之比为2∶1
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某些有机化合物的模型如图所示。
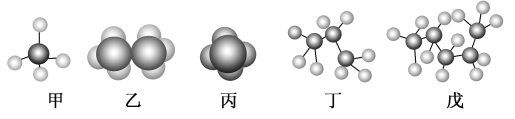
回答下列问题:
(1)属于比例模型的是________(填“甲”、“乙”、“丙”、“丁”或“戊”,下同)。
(2)表示同一种有机化合物的是____________。
(3)存在同分异构体的是___________,写出其同分异构体的结构简式________________________。
(4)含碳量最低的是________,含氢量最低的分子中氢元素的质量分数是________(保留一位小数)。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】中国计量科学研究院研制的NIM5铯原子喷泉钟,2000 万年不差一秒,日前成为国际计量局认可的基准钟之一,参与国际标准时间修正。关于Cs元素,下列说法错误的是
A. 137Cs和133Cs互为同位素 B. 单质Cs与水反应非常缓慢
C. 137Cs比133Cs多4个中子 D. 137Cs最外层只有1个电子
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】为探究FeCl3溶液中的离子平衡和离子反应,某小组同学进行了如下实验。
(1)配制50 mL 1.0 mol·L1的FeCl3溶液,测其pH约为0.7,即c(H+) = 0.2 mol·L1。
① 用化学用语解释FeCl3溶液呈酸性的原因: 。
② 下列实验方案中,能使FeCl3溶液pH升高的是 (填字母序号)。
a. 加水稀释 b. 加入FeCl3固体
c. 滴加浓KSCN溶液 d. 加入NaHCO3固体
(2)小组同学利用上述FeCl3溶液探究其与足量锌粉的反应。实验操作及现象如下:
操作 | 现象 |
向反应瓶中加入6.5 g锌粉,然后加入50 mL 1.0 mol·L1的FeCl3溶液,搅拌 | 溶液温度迅速上升,稍后出现红褐色沉淀,同时出现少量气泡;反应一段时间后静置,上层溶液为浅绿色,反应瓶底部有黑色固体 |
收集检验反应过程中产生的气体 | 集气管口靠近火焰,有爆鸣声 |
已知:Zn的性质与Al相似,能发生反应:Zn + 2NaOH = Na2ZnO2 + H2 ↑
① 结合实验现象和平衡移动原理解释出现红褐色沉淀的原因: 。
② 用离子方程式解释反应后溶液为浅绿色的原因: 。
③ 分离出黑色固体,经下列实验证实了其中含有的主要物质。
i. 黑色固体可以被磁铁吸引;
ii. 向黑色固体中加入足量的NaOH溶液,产生气泡;
iii. 将ii中剩余固体用蒸馏水洗涤后,加入稀盐酸,产生大量气泡;
iv. 向iii反应后的溶液中滴加KSCN溶液,无变化。
a. 黑色固体中一定含有的物质是 。
b. 小组同学认为上述实验无法确定黑色固体中是否含有Fe3O4,理由是 。
(3)为进一步探究上述1.0 mol·L1 FeCl3溶液中Fe3+和H+氧化性的相对强弱,继续实验并观察到反应开始时现象如下:
操作 | 现象 |
将5 mL 1.0 mol·L1的FeCl3溶液与0.65 g锌粉混合 | 溶液温度迅速上升,开始时几乎没有气泡 |
将 与0.65 g锌粉混合 | 溶液中立即产生大量气泡 |
小组同学得出结论:在1.0 mol·L1 FeCl3溶液中,Fe3+的氧化性比H+更强。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】X、Y、Z、W四种化合物均由1~18号元素组成,其中X含有四种元素,X、Y、Z的焰色反应均为黄色,W为无色无味气体。这四种化合物具有下列转化关系(部分反应物、产物及反应条件已略去)。请回答:

(1)W的分子式是___________。
(2)X与Y在溶液中反应的离子方程式是__________________。
(3)X含有的四种元素之间(二种、三种或四种)可组成多种化合物,选用其中某些化合物,利用下图装置快速制取少量的O2,并演示Na在O2中的燃烧实验。

①关闭装置中的止水夹a后,开启活塞b,漏斗中液体不断地往下滴,直至全部流入试管。试判断装置是否漏气______ (填“漏气”、“不漏气”或“无法确定”) ,判断理由是______。
②写出A装置中反应的化学方程式并标出电子得失情况:__________。
③C装置中观察到的现象是___________。
④D装置中盛放的试剂是__________,其作用是____________。
(4)向Z溶液中通入氯气,可制得某种生产和生活中常用的漂白、消毒的物质,同时有X生成,该反应的化学方程式是____________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列说法中正确的是
A.食盐水在电流作用下电离成钠离子和氯离子
B.强电解质的水溶液的导电能力一定比弱电解质的水溶液的导电能力强
C.电解质溶液中已电离出的离子和未电离的分子可以共存
D.电解质溶液的导电过程,与金属导体相同,都是物理过程
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com