
Ϊ������·���ѩ�����dz�ʹ��һ����ѩ��������Ҫ�ɷֵĻ�ѧʽΪXY2��X��Y��Ϊ���ڱ�ǰ20��Ԫ�أ��������Ӻ������ӵĵ��Ӳ�ṹ��ͬ����1 mol XY2����54 mol���ӡ�
(1)����ѩ���Ļ�ѧʽ��____________���������л�ѧ��������______________������ʽ��________________________________________��
(2)Ԫ��D��Eԭ�ӵ�����������������Ӳ�����2����D��Y���ڣ���D�����ӽṹʾ��ͼ��________��D��E���γ�һ�ֽṹ������CO2����ԭ�ӷ��ӣ���ÿ��ԭ�Ӿ��ﵽ��8e���ȶ��ṹ���÷��ӵĽṹʽΪ________������ʽΪ______________����ѧ������Ϊ________(����Ӽ��������Ǽ��Թ��ۼ������Թ��ۼ���)��
(3)W����Dͬ����Ķ�����Ԫ�أ�Z�ǵ������ڽ�������ǿ��Ԫ�أ�Z�ĵ�����W�ij��������з�Ӧʱ�����ֲ��������ʱ����________���仯ѧ������Ϊ________������ʱ����________���仯ѧ������Ϊ___________________________________________________________��

| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
ij�����ˮ��Һ�п��ܺ������������е������֣�K����NH4����Cl�� ��Ca2����CO32���� SO42������ÿ��ȡ100 mL��Һ�ֱ��������ʵ�飺
| ʵ���� | ʵ�鲽�� | ʵ������ |
| ����AgNO3��Һ | �г������� | |
| ��������NaOH��Һ����� | �ռ�����0.896L����״���� | |
| ����������BaCl2 ��Һ | �õ�����6.27g����������������ϴ�ӡ������ʣ��2.33 g |
����˵����ȷ���� ( )
A��һ�������ڵ����ӣ�Ca2����Cl��
B��c(K��) = 0.2 mol/L
C��c(K��) + c(NH4��) = c(CO32��) + c(SO42��)
D��һ�����ڵ����ӣ�K+��NH4����CO32����SO42��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
���жԻ�����M��N��������ȷ����

A��M�ķ���ʽΪC12H9O3
B��1mol M���������6molH2�����ӳɷ�Ӧ
C��M��N�����Լ���ϣ���ˮ��NaOH��Һ����
D��M��N�����Լ���ϣ�FeCl3��Һ��ϡH2SO4����
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
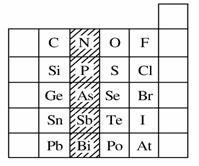
��ͼ��Ԫ�����ڱ���һ���֣�����ͼ����Ӱ����Ԫ�ص�˵���У���ȷ����
A��NԪ��Ϊ��һ����Ԫ��
B��PH3���ȶ��Ա�H2Sǿ
C��������Ԫ�ص�����������Ӧ��ˮ���ﻯѧʽ��ΪH3RO4
D��H3AsO4�����Ա�H3PO4��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
���ֶ�����Ԫ�������ڱ��е�λ������ͼ������ֻ��MΪ����Ԫ�ء�����˵������ȷ����
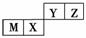 A��ԭ�Ӱ뾶Z<M
A��ԭ�Ӱ뾶Z<M
B��Y������������Ӧˮ��������Ա�X����
C��X �������̬�⻯������ȶ��Ա�Z��С
D��Zλ��Ԫ�����ڱ��е�2���ڡ��ڢ�A��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����ʵ��������ܴﵽĿ�ĵ���(����)
A����ȥMgCl2������Һ�е�Fe3�������Ƚ��裬����MgCO3�����ˣ�������������
B���Ʊ����ὺ�壺�������ˮ��Һ����εμ�ϡ��������Һ��ǿ����
C������Fe2(SO4)3��Һ���Ƿ���FeSO4���μ��������Ը��������Һ������
D��ʹʢ������������þ�������Թ��еij����ܽ⣺����һ�������Ȼ����Һ
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
������ʵ����ʵ���ó��Ľ��ۻ�����Ľ�����ȷ����(����)
| ʵ����ʵ | ���ۻ���� | |
| A | ��40 g NaOH����1 L����ˮ�� | ����Һ�����ʵ���������Ϊ3.84%�������ʵ���Ũ��Ϊ1 mol��L��1 |
| B | ��ʢ��Ũ������Թ��зֱ����AlƬ��CuƬ��ǰ��û�����������߷�Ӧ���ң�������������ɫ���� | ��ԭ��Al��Cu |
| C | �������Һ�м���ϡH2SO4�����ȼ����ӣ���ȴ���ټ�������Cu(OH)2�����ȣ�û�к�ɫ�������� | ����û��ˮ��������� |
| D | ��������FeCl3��MgCl2��Һ�м�������Mg(OH)2��ĩ������һ��ʱ������ | ��ȥMgCl2��Һ������FeCl3 |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Na2CO3��10H2O��NaHCO3��һ��������ɵĻ����ΪR����ȡm g R����ˮ�����Ƴ�200 mL��Һ����ʵ���ø���Һ�е�c(Na��)��0.50 mol��L��1������2m g��R�������������ٸı�ʱ���õ��Ĺ�������Ϊ(����)
A��10.60 g�� B��7.95 g
C��5.30 g�� D��2.65 g
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
�����İ��ˡ���һ����Ҫ�����ǣ���������˶�Ա�����˷ܼ���ij���˷ܼ��Ľṹ��ʽ��ͼ��ʾ���йظ����ʵ�˵����ȷ���ǣ�������
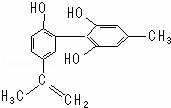
| �� | A�� | ��FeCl3��Һ����ɫ����Ϊ�������뱽������ͬϵ�� |
| �� | B�� | ����KMnO4��H+����Һ���۲���ɫ��ȥ����֤���ṹ�д���̼̼˫�� |
| �� | C�� | 1 mol��������Ũ��ˮ��H2��Ӧ�������Br2��H2�ֱ�Ϊ4 mol��7 mol |
| �� | D�� | �÷����е�����ԭ�ӿ��ܹ�ƽ�� |
�鿴�𰸺ͽ���>>
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com