
【题目】某校学习小组探究不同条件对电解FeCl2溶液产物的影响。所用实验装置如下图所示,其中电极为石墨电极。

(查阅文献)i. Fe2+、Fe3+在溶液中通过与Cl-结合分别形成FeCl42-、FeCl63-,可降低正电荷。
ii. 电解过程中,外界条件(如电解液pH、离子浓度、电压、电极材料等)会影响离子的放电能力。
(实验记录)
序号 | 实验条件 | 实验现象 | |
阴极 | 阳极 | ||
I | pH=0 1 mol·L-1 FeCl2溶液 电压1.5 V | 电极上产生无色气体。 | ①湿润淀粉碘化钾试纸始终未见变蓝。 ②取阳极附近溶液于试管中,滴加KSCN溶液,溶液变红。 |
II | pH=4.9 1 mol·L-1 FeCl2溶液 电压1.5 V | ①未观察到气泡产生,电极表面有银灰色金属光泽的固体析出。 ②电解结束后,将电极浸泡在盐酸中,观察到有大量气泡产生。 | ①湿润淀粉碘化钾试纸始终未见变蓝。 ②阳极附近出现红褐色浑浊。 取阳极附近浊液于试管中,先用盐酸酸化,再滴加KSCN溶液,溶液变红。 |
(1)结合阴极实验现象的分析
①实验I中阴极的电极反应式为________。
②用化学用语表示实验II中产生阴极现象的原因:________。
③对比实验I、II的阴极现象,可以获得的结论是________。
(2)结合阳极实验现象的分析
①甲同学认为实验I中Cl-没有放电,得出此结论依据的实验现象是________。阳极附近溶液滴加KSCN溶液变红,依据此现象分析,阳极反应可能是Fe2+ - e- === Fe3+、________。
②对比实验I、II的阳极现象,解释产生差异的原因:________。
(实验讨论)
(3)有同学提出,改变条件有可能在阳极看到“湿润淀粉碘化钾试纸变蓝”的现象,可能改变的条件是________,对应的实验方案是________。
【答案】2H+ + 2e- == H2↑ Fe2+ + 2e- == Fe和Fe + 2H+ == Fe2+ + H2↑ 其他条件相同时,pH=0,pH较小,c(H+)较大]时,阴极H+优先于1 mol·L-1 Fe2+放电产生H2,而pH=4.9,pH较大,c(H+)较小时,阴极1 mol·L-1Fe2+优(由pH=0变为pH=4.9,c(H+)减小,H+放电能力减弱,Fe2+放电能力增强) 湿润淀粉碘化钾试纸始终未见变蓝 FeCl42- - e- === Fe3+ + 4Cl-(或写为:FeCl42- + 2Cl- - e- === FeCl63-) 随着溶液pH的越低,c(H+)升高,抑制水解平衡Fe3+ + 3H2O![]() Fe(OH)3 + 3H+正向移动,难以生成Fe(OH)3或随着溶液pH的增大,c(H+)减小,有利于水解平衡Fe3+ + 3H2O
Fe(OH)3 + 3H+正向移动,难以生成Fe(OH)3或随着溶液pH的增大,c(H+)减小,有利于水解平衡Fe3+ + 3H2O![]() Fe(OH)3 + 3H+正向移动,生成Fe(OH)3 可改变条件1:改变c(Cl-);可改变条件2:改变电压 保持其他条件不变,用2 mol/L FeCl2溶液和n(n>0)mol/L NaCl溶液等体积混合的溶液作为电解液[c(Fe2+)= 1 mol/L,c(Cl-)>2 mol/L],观察阳极“湿润淀粉碘化钾试纸”上的现;保持其他条件不变,增大电压(或改变电压),观察阳极“湿润淀粉碘化钾试纸”上的现象
Fe(OH)3 + 3H+正向移动,生成Fe(OH)3 可改变条件1:改变c(Cl-);可改变条件2:改变电压 保持其他条件不变,用2 mol/L FeCl2溶液和n(n>0)mol/L NaCl溶液等体积混合的溶液作为电解液[c(Fe2+)= 1 mol/L,c(Cl-)>2 mol/L],观察阳极“湿润淀粉碘化钾试纸”上的现;保持其他条件不变,增大电压(或改变电压),观察阳极“湿润淀粉碘化钾试纸”上的现象
【解析】
(1)①根据电解的原理,阳离子应在阴极上放电,阳离子是Fe2+、H+,根据I中阴极现象:电极上产生无色气体,即阴极电极反应式为2H++2e-=H2↑;
②阴极未观察到气泡产生,电极表面有银灰色金属光泽的固体析出,即产生铁单质,电极反应式为Fe2++2e-=Fe,电解结束后将电极浸泡在盐酸中,观察到有大量气泡产生,发生Fe+2H+=Fe2++H2↑;
③对比实验I和II,不同的是H+浓度,得出结论是:其他条件相同时,pH=0,pH较小,c(H+)较大]时,阴极H+优先于1 mol·L-1 Fe2+放电产生H2,而pH=4.9,pH较大,c(H+)较小时,阴极1 mol·L-1Fe2+优(由pH=0变为pH=4.9,c(H+)减小,H+放电能力减弱,Fe2+放电能力增强) ;
(2)①Cl-放电,产生Cl2,氯气能将I-氧化成I2,淀粉碘化钾试纸将会变蓝,但实验I中,试纸并未变蓝,即Cl-没有放电;根据查阅文献i,阳极反应可能是Fe2+-e-=Fe3+,FeCl42--e-=Fe3++4Cl-,FeCl42-+Cl--e-=FeCl63-;
②两者现象差异是实验II中,阳极附近出现红褐色浑浊,即实验II阳极附近产生Fe(OH)3,产生差异的原因是随着溶液pH的越低,c(H+)升高,抑制水解平衡Fe3+ + 3H2O![]() Fe(OH)3 + 3H+正向移动,难以生成Fe(OH)3或随着溶液pH的增大,c(H+)减小,有利于水解平衡Fe3+ + 3H2O
Fe(OH)3 + 3H+正向移动,难以生成Fe(OH)3或随着溶液pH的增大,c(H+)减小,有利于水解平衡Fe3+ + 3H2O![]() Fe(OH)3 + 3H+正向移动,生成Fe(OH)3;
Fe(OH)3 + 3H+正向移动,生成Fe(OH)3;
(3)根据查阅文献ii,影响离子放电能力的外界因素有电解液的pH、离子浓度、电压、电极材料等,根据题意,改变条件有可能在阳极看到“湿润淀粉碘化钾试纸变蓝”,说明Cl-放电,可以是改变c(Cl-),设计方案是保持其他条件不变,用2 mol·L-1 FeCl2溶液和n(n>0)mol·L-1 NaCl溶液等体积混合的溶液作为电解液 NaCl溶液等体积混合的溶液作为电解液[cFe2+)= 1 mol/L,c(Cl-)>2 mol/L],观察阳极"湿润淀粉碘化钾试纸"上的现象;或者改变电压,设计方案是保持其他条件不变,增大电压(或改变电压),观察阳极"湿润淀粉碘化钾试纸"上的现象。


科目:高中化学 来源: 题型:
【题目】下列各组离子中,能大量共存且形成无色透明溶液的是
A.Mg2+、H+、C1-、OH-B.Na+、Ba2+、C1-、NO3-
C.Na+、H+、Cl-、CO32-D.K+、Cu2+、NO3-、SO42-
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】为探究某固体化合物X(仅含两种元素)的组成和性质,设计并完成如下实验,请回答:
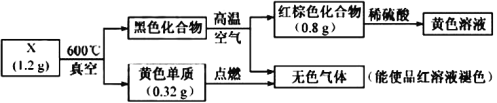
(1)X中的非金属元素是_________。
(2)黑色化合物高温空气红棕色化合物的化学方程式是___________________。
(3)设计实验方案检验黄色溶液中的金属阳离子_________________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列有关氧化还原反应的叙述中正确的是( )
A. 有单质参加或有单质生成的反应一定是氧化还原反应
B. 氧化还原反应的本质是元素化合价的升降
C. 金属单质在化学反应中一定作还原剂
D. 失电子的反应物在反应中作还原剂,反应中被还原
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】苯甲醛在医药、染料、香料等行业中都有着广泛的应用。实验室通过下图所示的流程由Mn2O3氧化甲苯制备苯甲醛,试回答下列问题。

(1)Mn2O3氧化甲苯的反应需要不断搅拌,搅拌的作用是________。
(2)甲苯经氧化后得到的混合物通过结晶、过滤进行分离,该过程中需将混合物冷却,其目的是______。
(3)实验过程中,可循环使用的物质有__________。
(4)实验中分离甲苯和苯甲醛采用的操作Ⅰ是___,其原理是_____。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列有关有机化合物(a)![]() (b)
(b)![]() (c)
(c)![]() 的说法正确的是
的说法正确的是
A. (a)(b)(c)均能与溴水发生化学反应
B. (b)二氯代物有两种
C. (a)(b)(c)互为同分异构体
D. (a)中所有原子可能共平面
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列说法正确的是( )
A.含有两种元素的物质一定是混合物
B.石墨在一定条件下转变为金刚石是物理变化
C.有单质参加的反应不一定是氧化还原反应
D.碳元素只能形成金刚石和石墨两种同素异形体
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列反应必须加入氧化剂才能实现的是( )
A. KMnO4→K2MnO4 B. CH4→CO2 C. SO2→SO3 2- D. H2O2→O2
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com