
| A. | Mg、Al、B | B. | N、O、S | C. | Li、Be、Mg | D. | B、F、Cl |
分析 A和B同周期,B和C同主族,设A元素的最外层电子数为x,则B、C最外层电子数为x+1或x-1,若B、C元素的最外层电子数为x+1,则x+2(x+1)=17,解得x=5,符合题意;若B、C元素的最外层电子数为x-1,则有x+2(x-1)=17,解得x=$\frac{19}{3}$,不符合题意,即A处于ⅤA族,B、C处于ⅥA族.三种元素质子数总和为31,平均质子数=$\frac{31}{3}$=10.3,一定有元素处于第二周期,故三元素处于短周期,可以确定B、C为O元素、S元素,进而计算A的质子数,确定A、B、C元素.
解答 解:A和B同周期,B和C同主族,设A元素的最外层电子数为x,则B、C最外层电子数为x+1或x-1,若B、C元素的最外层电子数为x+1,则x+2(x+1)=17,解得x=5,符合题意;若B、C元素的最外层电子数为x-1,则有x+2(x-1)=17,解得x=$\frac{19}{3}$,不符合题意,即A处于ⅤA族,B、C处于ⅥA族.三种元素质子数总和为31,平均质子数=$\frac{31}{3}$=10.3,一定有元素处于第二周期,故三元素处于短周期,可以确定B、C为O元素、S元素,故A的质子数为31-8-16=7,则A为N元素,由于A与B同周期,故B为O元素、C为S元素,故选B.
点评 本题考查原子结构与位置关系,难度中等,关键是根据三种元素位置关系结合质子数总和为31、最外层电子数之和为17,确定元素所在的周期和主族,注意掌握短周期元素的特点.


 名校课堂系列答案
名校课堂系列答案科目:高中化学 来源: 题型:选择题
| A. | 滴加KI-淀粉溶液变为蓝色 | |
| B. | 该溶液中Cu2+、NH4+、SO42-、Cl- 可以大量共存 | |
| C. | 与硝酸酸化的AgNO3溶液反应有沉淀生成并放出气体 | |
| D. | 向该溶液中通入过量Cl2,反应的离子方程式:2Fe2++4Br-+3Cl2═2Fe3++2Br2+6Cl- |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 第1列中的碱金属和第17列元素的单质熔、沸点变化趋势相同 | |
| B. | 元素周期表中从ⅢB族到ⅡB族十个纵列的元素都是金属元素 | |
| C. | 在整个18列元素中,第14列元素形成的化合物种类最多 | |
| D. | 在整个18列元素中,第3列元素种类最多 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
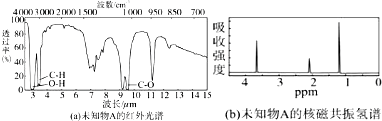
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
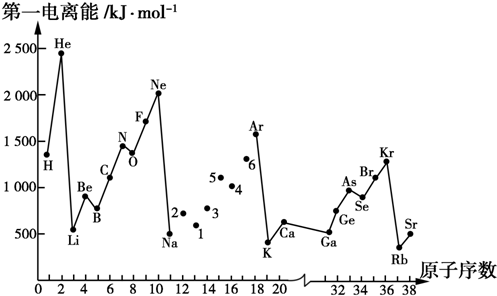
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
 将等物质的量浓度的CuSO4和NaCl等体积混合后,用石墨电极进行电解,电解过程中,溶液pH随时间t变化的曲线如图,则下列说法正确的是( )
将等物质的量浓度的CuSO4和NaCl等体积混合后,用石墨电极进行电解,电解过程中,溶液pH随时间t变化的曲线如图,则下列说法正确的是( )| A. | 阳极产物一定是Cl2,阴极产物一定是Cu | |
| B. | BC段表示在阴极上是H+放电产生了H2 | |
| C. | 整个过程中阳极先产生Cl2,后产生O2 | |
| D. | CD段表示的电解过程中水的电离被促进 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
| 元素 | A | B | C | D |
| 性质或结构信息 | 工业上通过分离液态空气获得其单质,单质能助燃 | 气态氢化物显碱性 | +3价阳离子的核外电子排布与氖原子相同 | 第三周期原子半径最小 |
 ,C单质与NaOH溶液反应的离子方程式为2Al+2H2O+2OH-=2AlO2-+3H2↑.
,C单质与NaOH溶液反应的离子方程式为2Al+2H2O+2OH-=2AlO2-+3H2↑.查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com