
��һ���ܱ������з������·�Ӧ��2SO2��g��+O2��g��![]() 2SO3��g������Ӧ������ijһʱ��SO2��SO3��O2�����ʵ���Ũ�ȷֱ�Ϊ0.2 mol��L-1��0.2 mol��L-1��0.1 mol��L-1������Ӧ�ﵽƽ��ʱ�����ܵ������ǣ� ��
2SO3��g������Ӧ������ijһʱ��SO2��SO3��O2�����ʵ���Ũ�ȷֱ�Ϊ0.2 mol��L-1��0.2 mol��L-1��0.1 mol��L-1������Ӧ�ﵽƽ��ʱ�����ܵ������ǣ� ��
A.c��SO3��=0.4 mol��L-1 B.c��SO2��+c��SO3��=0.15 mol��L-1
C.c��SO2��=0.25 mol��L-1 D.c��SO2��+c��SO3��=0.4 mol��L-1
 53���ò�ϵ�д�
53���ò�ϵ�д�
| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ��Ķ�����
| ���� |
| �� |
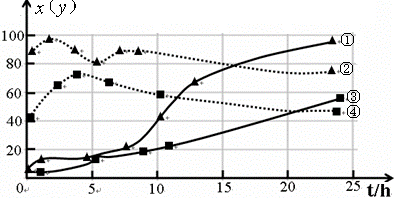
| ʵ����� | �¶ȡ� | ��ʼCCl4Ũ�ȣ�mol?L-1�� | ��ʼH2Ũ�ȣ�mol?L-1�� | CCl4��ת���� |
| 1 | 110 | 0.8 | 1.2 | a |
| 2 | 110 | 1 | 1 | 50% |
| 3 | 120 | 1 | 2 | x |
| 4 | 120 | 1 | 4 |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
��һ���ܱ������з������·�Ӧ��2SO2(g)+O2(g)![]() 2SO3(g)����Ӧ������ijһʱ�̲��SO2��O2��SO3��Ũ�ȷֱ�Ϊ��0.2 mol��L��1��0.2 mol��L��1��0.2 mol��L��1������Ӧ�ﵽƽ��ʱ�����ܳ��ֵ�������
2SO3(g)����Ӧ������ijһʱ�̲��SO2��O2��SO3��Ũ�ȷֱ�Ϊ��0.2 mol��L��1��0.2 mol��L��1��0.2 mol��L��1������Ӧ�ﵽƽ��ʱ�����ܳ��ֵ�������
A��c(SO3)=0.4 mol��L��1
B��c(SO2)=c(SO3)=0.15 mol��L��1
C��c(SO2)=0.25 mol��L��1
D��c(SO2)+c(SO3)=0.4 mol��L��1
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ��2013�츣��ʡ�߶���ѧ����ĩ���Ի�ѧ�Ծ� ���ͣ�ѡ����
��һ���ܱ������з������·�Ӧ��2SO2 (g)+O2(g)  2SO3(g������Ӧ������ijһʱ�̲��SO2��O2��SO3��Ũ�ȷֱ�Ϊ0.2
mol��L-1��0.1 mol��L-1��0.2 mol��L-1������Ӧ�ﵽƽ��ʱ�����ܳ��ֵ�������
�� ��
2SO3(g������Ӧ������ijһʱ�̲��SO2��O2��SO3��Ũ�ȷֱ�Ϊ0.2
mol��L-1��0.1 mol��L-1��0.2 mol��L-1������Ӧ�ﵽƽ��ʱ�����ܳ��ֵ�������
�� ��
A��C(SO3) = 0.4 mol��L-1 B��C(SO3) + C(SO2) = 0.15 mol��L-1
C��C(O2) = 0.3 mol��L-1 D��C(SO3) + C(SO2) = 0.4 mol��L-1
�鿴�𰸺ͽ���>>
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com