
为比较Fe3+和Cu2+对H2O2分解的催化效果强弱,甲乙两组同学分别设计了如图一、图二所示的实验.
(1)图一可通过观察 (现象)定性比较得出结论.有同学提出将CuSO4改为CuCl2或将FeCl3改为浓度相当的Fe2(SO4)3更为合理,其理由是: .
(2)图二所示实验中需测量的数据是 .
| 实验装置综合;催化剂的作用.. | |
| 分析: | (1)产生气泡的快慢可以定性确定双氧水的分解速率大小,比较Fe3+和Cu2+对H2O2分解的催化效果,要让选择的试剂Fe3+和Cu2+中的阴离子种类相同才有意义; (2)根据乙图装置来选择气密性的检查方法;该反应是通过反应速率分析的,结合v= |
| 解答: | 解:(1)可以通过观察产生气泡的快慢来定性比较比较Fe3+和Cu2+对H2O2分解的催化效果,将CuSO4改为CuCl2更为合理,把氯化铁改为硫酸铁,这样Fe3+和Cu2+中的阴离子种类相同,可以排除因阴离子的不同可能带来的影响, 故答案为:应产生气泡快慢(或反应完成的先后或试管壁的冷热程度);控制阴离子相同,排除阴离子的干扰; (2)结合乙图装置,该气密性的检查方法为:关闭分液漏斗活塞,将注射器活塞拉出一定距离,一段时间后松开活塞,观察活塞是否回到原位,则气密性良好,然后结合v= 故答案为:一定时间内收集到的气体体积(或收集一定体积的气体所需要的时间). |
| 点评: | 本题考查实验装置的综合应用,为高频考点,把握反应速率测定原理及影响反应速率的因素为解答的关键,侧重分析与实验能力的考查,题目难度不大. |


 黄冈创优卷系列答案
黄冈创优卷系列答案科目:高中化学 来源: 题型:
下列关于甲、乙、丙、丁四种仪器装置的有关用法,其中不合理的是

A.甲装置:可用来证明硫的非金属性比硅强
B.乙装置:橡皮管的作用是能使水顺利流下
C.丙装置:用图示的方法能检查此装置的气密性
D.丁装置:可在瓶中先装入某种液体收集NO气体
查看答案和解析>>
科目:高中化学 来源: 题型:
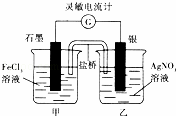
控制适合的条件,将反应Fe3++Ag⇌Fe2++Ag+设计成如图所示的原电池(盐桥装有琼脂﹣硝酸钾溶液;灵敏电流计的0刻度居中,左右均有刻度).已知接通后观察到电流计指针向右偏转.下列判断正确的是( )
|
| A. | 盐桥中的K+移向乙烧杯 |
|
| B. | 一段时间后,电流计指针反向偏转,越过0刻度,向左边偏转 |
|
| C. | 在外电路中,电子从石墨电极流向银电极 |
|
| D. | 电流计指针居中后,往甲烧杯中加入一定量的铁粉,电流计指针将向左偏转 |
查看答案和解析>>
科目:高中化学 来源: 题型:
下列化学反应的速率,一定是前者大于后者的( )
|
| A. | 反应A+B |
|
| B. | 相同温度下,与同浓度盐酸反应的锌粉和铁粉产生氢气的速率 |
|
| C. | 相同温度下,颗粒大小相同的生铁分别在水和饱和食盐水中的腐蚀生锈 |
|
| D. | 一定温度下,相同氢离子浓度、相同体积的盐酸与硫酸分别与大小相同的锌片反应,产生气泡的快慢 |
查看答案和解析>>
科目:高中化学 来源: 题型:
在1L恒容密闭容器中充入1mol Z发生反应:2Z(g)═2X(g)+Y(g),反应过程持续升高温度,测得混合体系中Z的体积分数与温度的关系如图所示.下列推断正确的是( )

|
| A. | 升高温度,平衡常数减小 |
|
| B. | Z在a、c两点的反应速率相等 |
|
| C. | b点时,Z的转化率最小 |
|
| D. | 平衡时充入惰性气体时,平衡向逆反应方向移动 |
查看答案和解析>>
科目:高中化学 来源: 题型:
下列关于乙醇的说法不正确的是( )
A.可用纤维素的水解产物制取 B. 可由乙烯通过加成反应制取
C.与乙醛互为同分异构体 D. 可以用于制取乙酸乙酯
查看答案和解析>>
科目:高中化学 来源: 题型:
下表中对应关系正确的是( )
| A | CH3CH3+Cl2CH3CH2Cl+HCl CH2=CH2+HCl→CH3CH2Cl | 均为取代反应 |
| B | 由油脂得到甘油; 由淀粉得到葡萄糖 | 均发生了水解反应 |
| C | Cl2+2Br‾═2Cl‾+Br2; Zn+Cu2+═Zn2++Cu | 均为单质被还原的置换反应 |
| D | 2Na2O2+2H2O+4NaOH+O2↑;Cl2+H2O═HCl+HClO | 均为水作还原剂的氧化还原反应 |
|
| A. | A | B. | B | C. | C | D. | D |
查看答案和解析>>
科目:高中化学 来源: 题型:
焦亚硫酸钠(Na2S2O5)是常用的食品抗氧化剂之一.某研究小组进行如下实验:
实验一 焦亚硫酸钠的制取
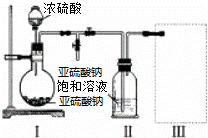
采用如图装置(实验前已除尽装置内的空气)制取Na2S2O5.装置Ⅱ中有Na2S2O5晶体析出,发生的反应为:Na2SO3+SO2═Na2S2O5
(1)装置Ⅰ中产生气体的化学方程式为 .
(2)要从装置Ⅱ中获得已析出的晶体,可采取的分离方法是 .
(3)装置Ⅲ用于处理尾气,可选用的最合理装置(夹时仪器已略去)为 (填序号)

实验二 焦亚硫酸钠的性质
Na2S2O5溶于水即生成NaHSO3.
(4)证明NaHSO3溶液中HSO3﹣的电离程度大于水解程度,可采用的实验方法是 .
a.测定溶液的pH b.加入Ba(OH)2溶液 c.加入盐酸
d.加入品红溶液 e.用蓝色石蕊试纸检测
(5)检验Na2S2O5晶体在空气中已被氧化的实验方案是 .
实验三 葡萄酒中抗氧化剂残留量的测定
(6)葡萄酒常用Na2S2O5作抗氧化剂.测定某葡萄酒中抗氧化剂的残留量(以游离SO2计算)的方案如下:

(已知:滴定时反应的化学方程式为SO2+I2+2H2O═H2SO4+2HI)
①按上述方案实验,消耗标准I2溶液25.00mL,该次实验测得样品中抗氧化剂的残留量(以游离SO2计算)为 g•L﹣1.
②在上述实验过程中,若有部分HI被空气氧化,则测定结果 (填“偏高”“偏低”或“不变”).
查看答案和解析>>
科目:高中化学 来源: 题型:
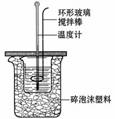
关于中和热测定实验的下列说法不正确的是( )
A.烧杯间填满碎泡沫塑料是减少实验过程中的热量损失
B.使用环形玻璃棒既可以搅拌又避免损坏温度计
C.向盛装酸的烧杯中加碱时要小心缓慢
D.测定酸后的温度计要用蒸馏水清洗干燥后再测碱的温度
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com