
某溶液中可能有下列阴离子中的一种或几种:SO42﹣、CO32﹣、Cl﹣、OH﹣.
(1)当溶液中有大量H+存在时,则不可能有 存在,发生反应的离子方程式 ;
(2)当溶液中有大量Ba2+存在时,则不可能有 ﹣ 存在,发生反应的离子方程式 ;
(3)检验某溶液中是否存在SO42﹣的试剂为 .
考点: 离子共存问题.
分析: (1)氢离子与碳酸根离子反应生成二氧化碳气体,氢离子与氢氧根离子反应生成水;
(2)钡离子与硫酸根离子、碳酸根离子反应生成难溶物碳酸钡、硫酸钡;
(3)先用稀盐酸除去干扰离子,然后用氯化钡溶液具有硫酸根离子.
解答: 解:(1)当溶液中有大量H+存在时,OH﹣、CO32﹣能够与氢离子发生反应,在溶液中不能大量共存,反应的离子方程式为:2H++CO32﹣=H2O+CO2↑(或H++CO32﹣=HCO3﹣)、OH﹣+H+=H2O,
故答案为:OH﹣、CO32﹣;2H++CO32﹣=H2O+CO2↑(或H++CO32﹣=HCO3﹣)、OH﹣+H+=H2O;
(2)当溶液中有大量Ba2+存在时,SO42﹣、CO32﹣能够与Ba2+发生反应生成难溶物,在溶液中不能大量共存,发生反应为:SO42﹣+Ba2+=BaSO4↓、CO32﹣+Ba2+=BaCO3↓,
故答案为:SO42﹣、CO32﹣;SO42﹣+Ba2+=BaSO4↓、CO32﹣+Ba2+=BaCO3↓;
(3)检验 SO42﹣时要避免SO32﹣的影响,就不要加入稀硝酸,因为稀硝酸能把SO32﹣ 氧化为SO42﹣,从而干扰SO42﹣ 的检验;要先加入过量稀盐酸,以除去 SO32﹣、CO32﹣ 等离子的影响,同时,当加入稀盐酸时没有沉淀,可排除Cl﹣的影响.当然,若溶液中不含SO32﹣离子,则加入稀硝酸也可.检验SO42﹣可用BaCl2溶液,看有没有白色沉淀产生;综上分析可知,检验某溶液中是否含有SO42﹣的操作方法是:首先在试液中加入盐酸酸化,再加入BaCl2溶液,若有BaSO4白色沉淀产生,则证明有SO42﹣,即:选用试剂为:稀盐酸和BaCl2,
故答案为:稀盐酸和BaCl2.
点评: 本题考查了离子共存、离子方程式的书写,题目难度中等,注意掌握离子反应发生条件,明确离子方程式的书写原则及离子共存的判断方法,试题培养了学生的分析、理解能力及灵活应用基础知识的能力.


 中考解读考点精练系列答案
中考解读考点精练系列答案科目:高中化学 来源: 题型:
某实验小组用工业上废弃固体(主要成分Cu2S和Fe2O3)混合物制取粗铜和Fe2(SO4)3晶体,设计的操作流程如图:

(1)除酒精灯和铁架台或三脚架外,①中所需的容器和夹持仪器分别为 ,①和⑥中都用到的仪器为 ;
(2)试剂x的化学式为H2O2;x与溶液B反应的离子方程式为 ;
(3)某同学取少量的溶液B向其中加入过量的某种强氧化剂,再滴加KSCN溶液,发现溶液变红色,放置一段时间后,溶液褪色,该同学猜测溶液褪色的原因是溶液中的SCN﹣ 被过量的氧化剂氧化所致,现给出以下试剂:1.0mol•L﹣1硫酸、1.0mol•L﹣1 NaOH溶液、0.1mol•L﹣1 Fe2(SO4)3溶液、20%KSCN溶液、蒸馏水.请你设计合理实验验证乙同学的猜测是否合理.简要说明实验步骤和现象 .
查看答案和解析>>
科目:高中化学 来源: 题型:
为确定某溶液的离子组成,分别进行如下实验:
①测定溶液的pH,溶液显强碱性.
②取少量溶液加入稀盐酸至溶液呈酸性,产生无刺激性、能使澄清石灰水变浑浊的气体.
③在上述溶液中再滴加Ba(NO3)2溶液,产生白色沉淀.
④取上层清液继续滴加Ba(NO3)2溶液至无沉淀时,再滴加AgNO3溶液,产生白色沉淀.
根据实验以下推测正确的是()
A. 一定有SO32﹣离子
B. 一定有CO32﹣离子
C. 一定有Cl﹣离子存在
D. 不能确定HCO3﹣离子是否存在
查看答案和解析>>
科目:高中化学 来源: 题型:
关于物质的分类正确组合是()
分类
组合 酸 碱 盐 氧化物
A H2SO4 Na2CO3 NaHCO3 SiO2
B HCl NaOH NaCl Na2O
C CO2 NaOH MgCl2 SO3
D HNO3 KOH CaO CaCO3
A. A B. B C. C D. D
查看答案和解析>>
科目:高中化学 来源: 题型:
关于氢氧化铁胶体和氯化镁溶液的说法中正确的是()
A. 可用丁达尔现象区分氢氧化铁胶体和氯化镁溶液两种分散系
B. 两者的分散质微粒均能透过半透膜和滤纸
C. 将氢氧化铁固体和氯化镁固体分别溶于水中即可得到氢氧化铁胶体和氯化镁溶液
D. 两种分散系中的分散质微粒直径均介于1~100nm之间
查看答案和解析>>
科目:高中化学 来源: 题型:
下列关于实验现象的描述不正确的是()
A. 把铜片和铁片紧靠在一起浸入稀硫酸中,铜片表面出现气泡
B. 用锌片做阳极,铁片做阴极,电解氯化锌溶液,铁片表面出现一层锌
C. 把铜片插入三氯化铁溶液中,在铜片表面出现一层铁
D. 把锌粒放入盛有盐酸的试管中,加入几滴氯化铜溶液,气泡放出速率加快
查看答案和解析>>
科目:高中化学 来源: 题型:
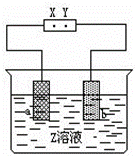
如图中X、Y分别是直流电源的两极,通电后发现a极板质量增加,b极板处有无色无臭气体放出,如图中符合这一情况的是()
A极板 B极板 X电极 Z溶液
A 锌 石墨 负极 CuSO4
B 石墨 石墨 负极 NaOH
C 银 铁 正极 AgNO3
D 铜 石墨 负极 CuCl2
A. A B. B C. C D. D
查看答案和解析>>
科目:高中化学 来源: 题型:
已知KNO3晶体溶解于水时要吸收热量,从溶液中析出KNO3晶体时会放出热量.若有室温下KNO3饱和溶液20mL,向其中加入1g KNO3晶体,充分搅拌后,下列判断正确的是( )
A. 溶液质量增加 B. 溶液的温度降低
C. 晶体不再溶解 D. 溶液的温度和质量都不变
查看答案和解析>>
科目:高中化学 来源: 题型:
氢气(H2)、一氧化碳(CO)、辛烷(C8H18)、甲烷(CH4)的热化学方程式分别为:H2(g)+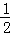 O2(g)=H2O(l);△H=﹣285.8kJ/molCO(g)+
O2(g)=H2O(l);△H=﹣285.8kJ/molCO(g)+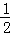 O2(g)=CO2(g);△H=﹣283.0kJ/molC8H18(l)+
O2(g)=CO2(g);△H=﹣283.0kJ/molC8H18(l)+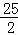 O2(g)=8CO2(g)+9H2O(l);△H=﹣5518kJ/molCH4(g)+2O2(g)=CO2(g)+2H2O(l);△H=﹣890.3kJ/mol
O2(g)=8CO2(g)+9H2O(l);△H=﹣5518kJ/molCH4(g)+2O2(g)=CO2(g)+2H2O(l);△H=﹣890.3kJ/mol
相同质量的H2、CO、C8H18、CH4完全燃烧时,放出热量最少的是()
A. H2(g) B. CO(g) C. C8H18(l) D. CH4(g)
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com