
【题目】常温下,下列各组离子一定能在指定溶液中大量共存的是
A. 能使pH试纸显蓝色的溶液中:Na+、ClO-、Fe3+、SO42-
B. 含有大量Al3+的溶液中:K+、Mg2+、NO3-、HCO3-
C. ![]() =1×10-13mol·L-1的溶液中:NH4+、Ca2+、Cl-、NO3-
=1×10-13mol·L-1的溶液中:NH4+、Ca2+、Cl-、NO3-
D. 常温下由水电离出的c(H+)=10-13 mol·L-1的溶液中:Na+、Ba2+、HCO3-、Cl-
【答案】C
【解析】能使pH试纸显蓝色的溶液显碱性,Fe3+与OH—发生反应,不能大量共存,A错误;含有Al3+的溶液水解显酸性,含有HCO3-的溶液水解显碱性,二者混合相互促进水解,生成沉淀和气体,不能大量共存,B错误;根据KW=c(H+)×c(OH—)可知,![]() =1×10-13mol·L-1的溶液c(OH—)= 1×10-13mol·L-1,c(H+)=0.1 mol·L-1的溶液显酸性,H+、NH4+、Ca2+、Cl-、NO3-离子间均能大量共存,C正确;常温下由水电离出的c(H+)=10-13 mol·L-1的溶液可以为酸溶液,也可以为碱溶液,HCO3-与H+、OH—均能发生反应,不能大量共存,D错误;正确选项C。
=1×10-13mol·L-1的溶液c(OH—)= 1×10-13mol·L-1,c(H+)=0.1 mol·L-1的溶液显酸性,H+、NH4+、Ca2+、Cl-、NO3-离子间均能大量共存,C正确;常温下由水电离出的c(H+)=10-13 mol·L-1的溶液可以为酸溶液,也可以为碱溶液,HCO3-与H+、OH—均能发生反应,不能大量共存,D错误;正确选项C。


 状元坊全程突破导练测系列答案
状元坊全程突破导练测系列答案 直通贵州名校周测月考直通名校系列答案
直通贵州名校周测月考直通名校系列答案科目:高中化学 来源: 题型:
【题目】在2 L的恒容密闭容器中充入A(g)和B(g),发生反应A(g)+B(g)![]() 2C(g)+D(s) △H=a kJ·mol-1,实验内容和结果分别如表和图所示,下列说法不正确的是
2C(g)+D(s) △H=a kJ·mol-1,实验内容和结果分别如表和图所示,下列说法不正确的是
实验序号 | 温度 | 起始物质的量 | 热量变化 | |
A | B | |||
I | 600℃ | 1mol | 3mol | 96kJ |
II | 800℃ | 1.5mol | 0.5mol | —— |
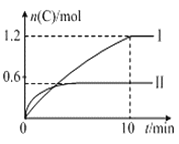
A. 实验Ⅰ中,10 min内平均速率v(B)=0.03 mol·L-1·min-1
B. 上述方程式中a=160
C. 600 ℃时,该反应的平衡常数是1.5
D. 向实验Ⅱ的平衡体系中再充入0.5 mol A和1.5 mol B,A的转化率增大
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】已知X、Y、Z、E、F五种常见物质含有同一元素M,在一定条件下它们有如下转化关系,Z是NO,下列推断不合理的是:

A. X可能是一种氢化物
B. 若Y为单质,Y生成Z属于化合反应
C. E可能是一种有色气体
D. F中M元素的化合价可能为+5
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】如图是中学化学中常用于混合物的分离和提纯的装置。
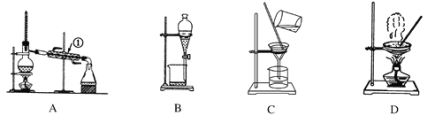
利用以上装置,可以按以下实验方案从海洋动物柄海鞘中提取具有抗肿瘤活性的天然产物。(已知甲苯和甲醇均为有机溶剂,有机物大多能互溶)

(1)装置A中仪器①的作用是________,使用装置A的操作是_____(填“a”、“b”、“c”或“d”,下同)。
(2)使用装置B的操作是______,为使其中液体顺利滴下,除打开下端活塞外,还应进行的具体操作是___________________。
(3)使用装置C的操作是_______,若所得沉淀不溶于水且需要洗涤,则洗涤的具体操作是________________________________________________________________________________。
(4)使用装置D的操作是_______。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】近日,中国科学院深圳先进技术研究院研发出一种高性能的钙离子电池:以溶有六氟磷酸钙Ca(PF6)2的碳酸酯类溶剂为电解液,放电时合金Ca7Sn6发生去合金化反应,阴离子(PF6)从石墨烯中脱嵌,进入电解质溶液。放电时其工作原理如下图,下列说法错误的是(已知:比能量为单位质量的电极放出电能的大小)
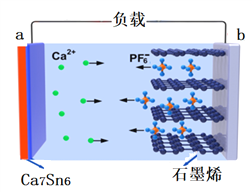
A. 电池放电时,化学能转化为电能和热能
B. 放电时,a电极的电极反应方程式为:Ca7Sn6 —14e- =7Ca2+ + 6Sn
C. 充电时,b电极接电源的正极
D. 与锂离子电池相比较钙离子电池具有材料储量丰富、比能量高的优点
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】以氧化铝为原料,通过碳热还原法可合成氮化铝(AlN);通过电解法可制取铝。电解铝时阳极产生的CO2可通过二氧化碳甲烷化再利用。
请回答:
(1)已知:2Al2O3(s)===4Al(g)+3O2(g) ΔH1=3 351 kJ·mol-1
2C(s)+O2(g)===2CO(g) ΔH2=-221 kJ·mol-1
2Al(g)+N2(g)===2AlN(s) ΔH3=-318 kJ·mol-1
碳热还原Al2O3合成AlN的总热化学方程式是________________________,
该反应自发进行的条件________。
(2)在常压、Ru/TiO2催化下,CO2和H2混合气体(体积比1∶4,总物质的量a mol)进行反应,测得CO2转化率、CH4和CO选择性随温度变化情况分别如图1和图2所示(选择性:转化的CO2中生成CH4或CO的百分比)。
反应Ⅰ CO2(g)+4H2(g)![]() CH4(g)+2H2O(g) ΔH4
CH4(g)+2H2O(g) ΔH4
反应Ⅱ CO2(g)+H2(g)![]() CO(g)+H2O(g) ΔH5
CO(g)+H2O(g) ΔH5
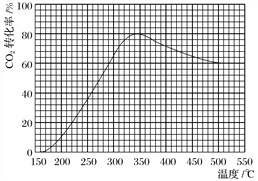
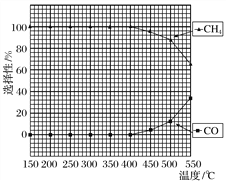
图1 图2
①下列说法不正确的是________。
A.ΔH4小于零
B.温度可影响产物的选择性
C.CO2平衡转化率随温度升高先增大后减少
D.其他条件不变,将CO2和H2的初始体积比改变为1∶3,可提高CO2平衡转化率
②350 ℃时,反应Ⅰ在t1时刻达到平衡,平衡时容器体积为V L,该温度下反应Ⅰ的平衡常数为________(用a、V表示)。
③350 ℃下CH4物质的量随时间的变化曲线如图3所示。画出400 ℃下0~t1时刻CH4物质的量随时间的变化曲线。__________________________
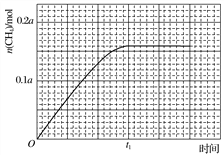
图3
(3)据文献报道,CO2可以在碱性水溶液中电解生成甲烷,生成甲烷的电极反应式是______。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com