
【题目】次磷酸钴[Co(H2PO2)2]广泛应用于化学电镀,工业上利用电渗析法制取次磷酸钴的原理图如图所示。
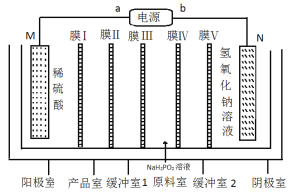
已知:①该装置的电极材料分别为金属钴和不锈钢。
②Co(H2PO2)2溶液在强碱性条件下通过自身催化发生氧化还原反应,实现化学镀钴。
下列说法中正确的是( )
A.膜Ⅱ、膜Ⅲ均为阴离子交换膜
B.M电极反应为Co-2e-+2H2PO2-=Co(H2PO2)2
C.a为电源的负极
D.Co(H2PO2)2溶液化学镀钴过程中反应可能为Co2++H2PO2-+3OH=Co+HPO3-+2H2O
 口算心算速算应用题系列答案
口算心算速算应用题系列答案 同步拓展阅读系列答案
同步拓展阅读系列答案科目:高中化学 来源: 题型:
【题目】局部麻醉药普鲁卡因E(结构简式为![]() )的三条合成路线如下图所示(部分反应试剂和条件已省略):
)的三条合成路线如下图所示(部分反应试剂和条件已省略):
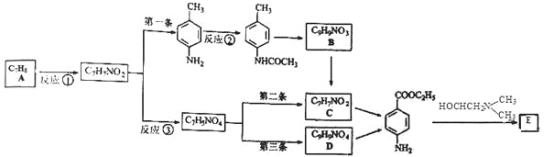
完成下列填空:
(1).比A多一个碳原子,且一溴代物只有3种的A的同系物的名称是___________。
(2).写出反应试剂和反应条件。反应①______;③______
(3).设计反应②的目的是____________。
(4).B的结构简式为_____;C的名称是____。
(5).写出一种满足下列条件的D的同分异构体的结构简式____。
①芳香族化合物 ②能发生水解反应 ③有3种不同环境的氢原子
1 mol该物质与NaOH溶液共热最多消耗_____mol NaOH。
(6).普鲁卡因的三条合成路线中,第一条合成路线与第二条、第三条相比不太理想,理由是_________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】有机物X、Y的转化如下,下列说法不正确的是
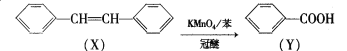
A. X转化为Y的反应属于氧化反应
B. ![]() 与Y互为同分异构体
与Y互为同分异构体
C. Y分子苯环上的二氯代物有5种
D. X、Y分子的所有原子可能共平面
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】用NA表示阿伏加德罗常数的值。下列说法正确的是( )
A. 28g CO和N2的混合气体质子数为14 NA
B. 标况下,22.4 L CCl4含有Cl原子数为4NA
C. 标准状况下22.4L 氯气与水完全反应生成HCl的数目为NA
D. 1 mol·L-1 K2CO3溶液中含有钾离子数目为2NA
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】为验证氯元素的非金属性比硫元素的非金属性强,某化学实验小组设计了如图实验,请回答下列问题:
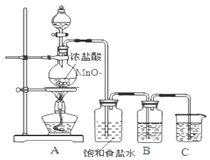
(1)装置B中盛放的试剂是___(填选项),实验现象为___,化学反应方程式是___。
A.Na2S溶液 B.Na2SO3溶液 C.Na2SO4溶液
(2)装置C中盛放烧碱稀溶液,目的是___。反应的离子方程式是___。
(3)能证明氯元素比硫元素非金属性强的依据为___。(填序号)
①氯原子比硫原子更容易获得电子形成离子
②次氯酸的氧化性比稀硫酸强
③比Cl-还原性强
④比H2S稳定
(4)若B瓶中盛放KI溶液和CCl4试剂,实验后,振荡、静置,会出现分层,下层呈紫红色的实验现象,若B瓶中通入标准状况下44.8L氯气全部参加反应,则转移的电子数目是___。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】(1)3.1 g Na2X含有Na+ 0.1 mol,则Na2X的摩尔质量为________,X的相对原子质量为________。
(2)同温同压下,同体积的甲烷和氢气分子数之比为_______,原子个数之比为_____,质量之比为_________,电子数之比为________。
(3)用等体积的0.1 mol·L-1的BaCl2溶液,可使相同体积的Fe2(SO4)3、Na2SO4、Al2(SO4)3三种溶液中的SO42-都恰好完全沉淀,则三种硫酸盐的物质的量浓度之比为_____。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列说法正确的是
A. 氢氧燃料电池放电时化学能全部转化为电能
B. 反应4Fe(s)+3O2(g)![]() 2Fe2O3(s)常温下可自发进行,该反应为吸热反应
2Fe2O3(s)常温下可自发进行,该反应为吸热反应
C. 3 mol H2与1 mol N2混合反应生成NH3,转移电子的数目小于6×6.02×1023
D. 在酶催化淀粉水解反应中,温度越高淀粉水解速率越快
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】已知某气体反应的平衡常数可表示为K=![]() ,该反应在不同温度下的平衡常数:400℃,K=32;500℃,K=44。请回答下列问题:
,该反应在不同温度下的平衡常数:400℃,K=32;500℃,K=44。请回答下列问题:
(1)写出上述反应的化学方程式____。
(2)已知在密闭容器中,测得某时刻各组分的浓度如下:
物质 | CH3OH(g) | CH3OCH3(g) | H2O(g) |
浓度/(molL-1) | 0.54 | 0.68 | 0.68 |
①此时温度400℃,则某时刻υ正____υ逆(填<、>或=,下同)。
②若以温度为横坐标,以该温度下平衡态甲醇物质的量n为纵坐标,此时反应点在图象的位置是图中___点,比较图中B、D两点所对应的正反应速率υB_____υD,理由是____。

(3)一定条件下要提高反应物的转化率,可以采用的措施是___。
a.升高温度 b.加入催化剂 c.压缩容器的体积 d.增加水蒸气的浓度 e.及时分离出产物
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】25℃时,醋酸溶液中存在电离平衡:CH3COOH![]() CH3COO-+ H+,下列说法正确的是
CH3COO-+ H+,下列说法正确的是
A.向体系中加入少量CH3COONa固体,平衡向左移动,c(CH3COO-)下降
B.向体系中加水稀释,平衡向右移动,溶液中所有离子的浓度都减小
C.加入少量NaOH固体(忽略溶解热效应),平衡向右移动,水的电离程度也随之增大
D.升高体系温度(忽略醋酸挥发),溶液中H+数目增多,平衡一定向左移动
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com