
| A. | 一定有SO2、NH3和NO | B. | 一定有NO和HCl | ||
| C. | 可能有Cl2和O2 | D. | 一定没有Cl2、NO2、NH3和O2 |
分析 根据气体的颜色判断可排除Cl2和NO2气体,将此无色混合气体通过品红溶液后,品红溶液褪色说明含SO2,把剩余气体排入空气中,很快变为红棕色,说明含有气体NO,一氧化氮和氧气发生反应,所以原混合气体中一定无氧气,该无色混合气体遇浓盐酸未看到明显现象,证明原气体中无NH3存在.
解答 解:根据气体的颜色判断可排除Cl2和NO2气体,将此无色混合气体通过品红溶液后,品红溶液褪色说明含SO2,把剩余气体排入空气中,很快变为红棕色,说明含有气体NO,一氧化氮和氧气发生反应,所以原混合气体中一定无氧气,该无色混合气体遇浓盐酸未看到明显现象,证明原气体中无NH3存在,原混合气体成分一定没有Cl2、NO2、NH3和O2,故选D.
点评 本题考查常见气体的检验,题目难度不大,注意常见气体的性质以及检验方法,特别是有颜色的气体要熟练掌握.


 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案科目:高中化学 来源: 题型:解答题
 前四周期元素X、Y、Z、Q、R、W的原子序数依次增大.X基态原子的2p轨道为半充满状态;Y基态原子的L层有2个未成对电子;Z基态原子的最外层电子排布为3s23p2;Q、R、W都属于金属元素,Q、W基态原子核外均没有未成对电子,R基态原子的d轨道上有3个空轨道.
前四周期元素X、Y、Z、Q、R、W的原子序数依次增大.X基态原子的2p轨道为半充满状态;Y基态原子的L层有2个未成对电子;Z基态原子的最外层电子排布为3s23p2;Q、R、W都属于金属元素,Q、W基态原子核外均没有未成对电子,R基态原子的d轨道上有3个空轨道.查看答案和解析>>
科目:高中化学 来源: 题型:选择题
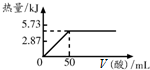 已知H+(aq)+OH-(aq)=H2O(l)△H=-57.3kJ/mol,向50mL 2mol/L的NaOH溶液中加入1mol/L的某种酸恰好完全反应,测得加入酸的体积与反应放出热量的关系如下图所示(不考虑热量的散失),则该酸可能是( )
已知H+(aq)+OH-(aq)=H2O(l)△H=-57.3kJ/mol,向50mL 2mol/L的NaOH溶液中加入1mol/L的某种酸恰好完全反应,测得加入酸的体积与反应放出热量的关系如下图所示(不考虑热量的散失),则该酸可能是( )| A. | 醋酸(CH3COOH) | B. | 盐酸 | C. | 草酸(HOOC-COOH) | D. | 硫酸 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 配制银氨溶液时的总反应:Ag++3NH3•H20═[Ag(NH3)2]OH+NH4++2H20 | |
| B. | 向1 mL 0.l mol/L硝酸亚铁溶液加入1 mL 0.1 mol/L的HI溶液:3 Fe2++N03-+4H+═3 Fe3++NO+2H2O | |
| C. | 向10 mL 0.lmol/L NH4Al(SO4)2溶液中加入0.1 mol/L Ba(OH)2溶液至恰好只有一种沉淀时:NH4++Al3++5OH-+2 SO42-+2Ba2+═AlO2-+NH3•H2O+2H2O+2BaSO4L | |
| D. | 向高锰酸钾酸性溶液中滴加H202溶液,高锰酸钾溶液紫红色褪去:2MnO4-+7H2O2+6H+═2Mn2++6O2+lOH2O |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 25.4ρ | B. | 12.7ρ | C. | 6.97ρ | D. | 6.35ρ |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 需要配置480mL该溶液,应选用500mL容量瓶 | |
| B. | 固体NaOH须放到烧杯中称量 | |
| C. | 把称好的固体加水溶解后马上转移到容量瓶中 | |
| D. | 定容时俯视刻度线,所配NaOH溶液浓度会偏大 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
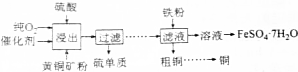
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | CH3F | B. | CCl4 | C. | COCl2 | D. | CH2ClCOOH. |
查看答案和解析>>
科目:高中化学 来源: 题型:填空题
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com