
| A. | 浓硫酸 | B. | 浓硝酸 | C. | 稀硝酸 | D. | 盐酸 |
分析 常温下将铁放入下列过量的溶液中,其中浓硫酸、浓硝酸会发生钝化现象,在金属表面形成一薄层氧化物薄膜阻止反应进行,铁是变价金属遇到强氧化剂会生成三价铁离子,遇到弱氧化剂会生成二价铁离子,据此分析选项.
解答 解:A.常温下将铁放入浓硫酸中发生钝化,反应不能继续进行,故A错误;
B.常温下将铁放入浓硝酸中发生钝化,反应不能继续进行,故B错误;
C.过量稀硝酸具有强氧化性能氧化铁为三价铁离子,在溶液中能大量生成Fe3+,故C正确;
D.铁放入盐酸发生反应生成氯化亚铁和氢气,不能得到三价铁,故D错误;
故选C.
点评 本题考查了铁的性质分析,主要是浓硫酸、浓硝酸中的钝化现象、稀酸溶液在产物的判断,注意溶液都是过量反应,题目难度不大.


 小题狂做系列答案
小题狂做系列答案科目:高中化学 来源: 题型:选择题
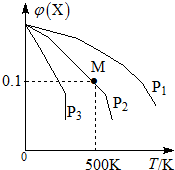 某可逆反应为2X(g)?3Y(g)+Z(g),混合气体中X的物质的量分数与温度关系如图所示:下列推断正确的是( )
某可逆反应为2X(g)?3Y(g)+Z(g),混合气体中X的物质的量分数与温度关系如图所示:下列推断正确的是( )| A. | 升高温度,该反应平衡常数K减小 | |
| B. | 压强大小有P3>P2>P1 | |
| C. | 平衡后加入高效催化剂使气体相对分子质量增大 | |
| D. | 在该条件下M点X平衡转化率为$\frac{9}{11}$ |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | “熬胆矾铁釜,久之亦化为铜”,该过程发生了置换反应 | |
| B. | 某古剑“以剂钢为刃,铁为茎干,…,”“剂钢”指的是铁的合金 | |
| C. | 《梦溪笔谈》载:“高奴县出脂水,燃之如麻,但烟甚浓”,所述“脂水”属于石油 | |
| D. | 《肘后备急方》载:“青蒿一握,以水二升渍,绞取汁”,如此提取青蒿素纯属萃取 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
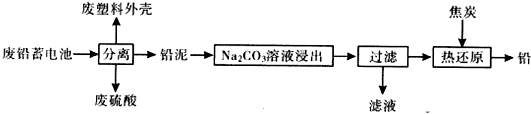
| 物质 | Ksp(25℃) | 颜色 |
| PbSO4 | 1.8×10-8 | 白色 |
| PbCO3 | 1.5×10-13 | 白色 |
| PbCrO4 | 1.8×10-14 | 黄色 |
| BaCrO4 | 1.2×10-10 | 黄色 |
| Pb(OH)2 | 1.4×10-20 | 白色 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
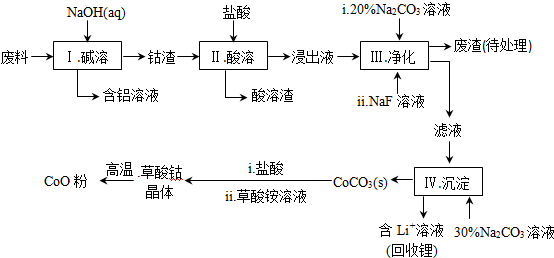
| Fe3+ | Co2+ | Co3+ | Al3+ | |
| pH(开始沉淀) | 1.9 | 7.15 | -0.23 | 3.4 |
| pH(完全沉淀) | 3.2 | 9.15 | 1.09 | 4.7 |
 LixC+Li1-xCoO2,LixC中Li的化合价为0价,该锂离子电池充电时阳极的电极反应式为LiCoO2-xe-=Li1-xCoO2+xLi+.
LixC+Li1-xCoO2,LixC中Li的化合价为0价,该锂离子电池充电时阳极的电极反应式为LiCoO2-xe-=Li1-xCoO2+xLi+.查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 除去铁粉中的铜粉,加入足量浓硫酸加热反应后进行过滤 | |
| B. | 不用任何其他试剂就可以鉴别NaOH溶液和Al2(SO4)3溶液 | |
| C. | 制备Fe(OH)3胶体时,通常是将Fe(OH)3固体溶于沸水中 | |
| D. | 某溶液中加入盐酸能产生使澄清石灰水变浑浊的气体,则该溶液中一定含有CO32- |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
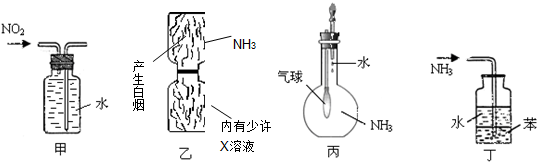
| A. | 图甲:收集NO2气体 | B. | 图乙:验证X溶液为浓硫酸 | ||
| C. | 图丙:验证氨气在水中的溶解性 | D. | 图丁:用于吸收尾气NH3 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com