
(8分)下图为某同学设计的一个原电池。
若电解质溶液为H2SO4:
①Fe是______极,其电极反应为_________________,该反应是__________(填“氧化”或“还原”)反应;
②Cu是______极,其电极反应为___________________,该电极上反应现象是________________;
若电解质溶液为CuSO4:
③Cu电极上电极反应为________________,其反应现象是________________。
科目:高中化学 来源: 题型:阅读理解
 长期存放的亚硫酸钠可能会被空气中的氧气氧化.某化学兴趣小组通过实验来定性、定量测定亚硫酸钠试剂的被氧化的程度,设计如下方案:
长期存放的亚硫酸钠可能会被空气中的氧气氧化.某化学兴趣小组通过实验来定性、定量测定亚硫酸钠试剂的被氧化的程度,设计如下方案:| 126b |
| 233a |
| 126b |
| 233a |
查看答案和解析>>
科目:高中化学 来源: 题型:
称取![]()
![]() 精盐
精盐
(1)判断BaCl2已过量的方法是____________________________________________________。
(2)第④步中,相关的离子方程式是_____________________________________________。
(3)若先用盐酸调pH再过滤,将对实验结果产生影响,其原因是_____________________。
(4)为检验精盐纯度,需配制150 mL 0.2 mol·L-1 NaCl(精盐)溶液,下图是该同学转移溶液的示意图,图中的错误是_________________________________________________。

查看答案和解析>>
科目:高中化学 来源: 题型:

A.电源中a为负极,b为正极 B.电解池中的电解液不能用NaCl溶液
C.A、B两端都必须使用铁作电极 D.阳极的电极反应式为:Fe-2e-====Fe2+
查看答案和解析>>
科目:高中化学 来源: 题型:

A.关闭K2、打开K1,试管内两极都有气泡产生
B.关闭K2、打开K1,一段时间后,发现左侧试管收集到的气体比右侧略多,则a为负极,b为正极
C.关闭K2、打开K1,一段时间后,用拇指堵住试管移出烧杯,向试管内滴入酚酞,发现左侧试管内溶液变红色,则a为负极,b为正极
D.关闭K2、打开K1,一段时间后,再关闭K1、打开K2,电流计指针不会偏转
查看答案和解析>>
科目:高中化学 来源:同步题 题型:实验题
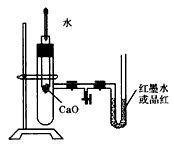
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com