
【题目】现有容积均为2 L的甲、乙恒容密闭容器,向甲中充入1.5 mol CO2和3 mol H2,乙中充入2 mol CO2、3 mol H2,一定条件下仅发生反应:CO2(g)+3H2(g) ![]() CH3OH(g)+H2O(g),实验测得反应体系中CO2的平衡转化率与温度的关系曲线如图所示。下列说法正确的是
CH3OH(g)+H2O(g),实验测得反应体系中CO2的平衡转化率与温度的关系曲线如图所示。下列说法正确的是

A.该反应的ΔH>0
B.曲线Ⅱ表示甲容器中CO2的平衡转化率与温度的关系
C.500 K时,该反应的化学平衡常数为200
D.700 K时,若在上述密闭容器中充入0.9 mol CO2、1.2 mol H2、0.1 mol CH3OH、0.1mol H2O,则达到平衡时,H2的体积分数大于![]()
【答案】CD
【解析】
A.随着温度升高,CO2平衡转化率降低,表明温度升高不利于反应正向进行,所以反应为放热反应,该反应的ΔH<0,故A错误;
B.相同温度下,平衡常数不变,曲线Ⅰ中CO2的平衡转化率高,甲和乙相比,相同条件下乙中二氧化碳的浓度大,曲线Ⅰ表示甲容器中CO2的平衡转化率与温度的关系,故B错误;
C.如图所示,曲线Ⅰ代表甲容器的反应,500 K时,CO2的平衡转化率为60%,根据反应CO2(g)+3H2(g)CH3OH(g)+H2O(g),则平衡时n(CO2)= 1.5 mol×(1-60%)=0.6mol,n(H2)=3mol -3×1.5 mol×60%=0.3 mol,n(CH3OH)= n(H2O)=0.9mol,该反应的化学平衡常数为K=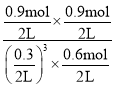 =200,故C正确;
=200,故C正确;
D.如图所示,曲线Ⅱ代表乙容器的反应,700 K时,乙容器中CO2的平衡转化率为20%,根据反应CO2(g)+3H2(g)CH3OH(g)+H2O(g),则平衡时n(CO2)=2mol×(1-20%)=1.6mol,n(H2)=3mol -3×2 mol×20%=1.8 mol,n(CH3OH)= n(H2O)=0.4mol,此时H2的体积分数=![]() =
=![]() ,若在上述密闭容器中充入0.9 mol CO2、1.2 mol H2、0.1 mol CH3OH、0.1mol H2O,此时密闭容器中n(CO2)=2.5mol,n(H2)=3mol,n(CH3OH)= n(H2O)=0.5mol,与原平衡初始相比,氢气的物质的量不变,其他组分增加,相当于增大了密闭容器的压强,平衡正向移动,则达到平衡时,H2的体积分数大于
,若在上述密闭容器中充入0.9 mol CO2、1.2 mol H2、0.1 mol CH3OH、0.1mol H2O,此时密闭容器中n(CO2)=2.5mol,n(H2)=3mol,n(CH3OH)= n(H2O)=0.5mol,与原平衡初始相比,氢气的物质的量不变,其他组分增加,相当于增大了密闭容器的压强,平衡正向移动,则达到平衡时,H2的体积分数大于![]() ,故D正确;
,故D正确;
答案选CD。


科目:高中化学 来源: 题型:
【题目】在恒容密闭容器中加入浓度均为0.2 mol·L1的CO和H2O, T℃发生如下反应:CO(g)+H2O(g)![]() CO2(g)+H2(g)。下列说法能充分说明该反应已经达到化学平衡状态的是
CO2(g)+H2(g)。下列说法能充分说明该反应已经达到化学平衡状态的是
A.单位时间内消耗1 mol CO同时生成1 mol CO2
B.混合气体的密度不再变化
C.CO、H2O、CO2和H2 的浓度不再变化
D.混合气体的平均摩尔质量不再变化
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】常温下,向20.00mL0.1mol·L-1氨水中滴入0.1mol·L-1盐酸,溶液中由水电离出的c(H+)的负对数[-1gc水(H+)]与所加盐酸体积的关系如图所示,下列说法不正确的是( )
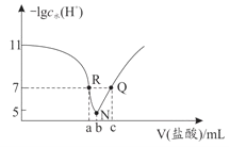
A.常温下,Kb(NH3·H2O)约为1×10-5
B.b=20.00
C.R、Q两点对应溶液均呈中性
D.R到N、N到Q所加盐酸体积不相等
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】正溴丁烷是稀有元素萃取的溶剂及有机合成的中间体,其制备如图(夹持装置略):
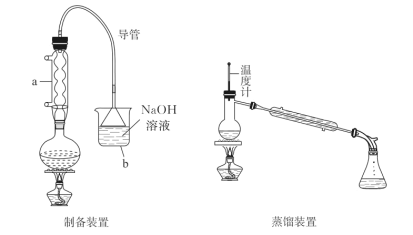
已知:i.NaBr+H2SO4(浓)=HBr↑+NaHSO4
ii.CH3CH2CH2CH2OH十HBr→CH3CH2CH2CH2Br+H2O
iii.2HBr+H2SO4![]() Br2+SO2+2H2O
Br2+SO2+2H2O
iv.正溴丁烷密度:1.27g·mL-1;浓硫酸密度:1.84g·mL-1
请回答下列问题:
(1)正溴丁烷粗产品的制备:
①仪器a的名称是__,向圆底烧瓶中添加药品顺序正确的是__(填正确选项字母)。
A.浓H2SO4→适量水→正丁醇→溴化钠粉末
B.适量水→浓H2SO4→正丁醇→溴化钠粉末
C.适量水→正丁醇→浓H2SO4→溴化钠粉末
D.适量水→正丁醇→溴化钠粉末→浓H2SO4
②装置b中装入NaOH溶液,目的是__。
③加热回流,在此期间要不断地摇动反应装置,其原因为__;冷却后改为蒸馏装置,蒸出其正溴丁烷的粗品。
(2)正溴丁烷的提纯:
①把正溴丁烷粗品倒入分液漏斗中,加入适量水洗涤,分出有机层;
②在另一干燥的分液漏斗中,加入浓硫酸洗去有机层中少量的未反应的正丁醇及副产物,从__(选填“上口”或“下口”)分出有机层;
③有机层依次用适量的水、浓硫酸、水、饱和NaHCO3溶液、水洗涤,用无水CaCl2干燥。以上三次用水洗涤简化为一次用水洗涤是否合理,并说明理由__。
(3)①若洗涤后产物有红色,说明含有溴单质,应加入适量的饱和NaHSO3溶液洗涤,将溴单质全部除去,其反应的离子方程式为__。
②若投入正丁醇11.84g,得到产物12.50g。则正丁醇的转化率为__(保留两位小数)。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】已知A、B、C、D、E都是周期表中前四周期的元素,它们的核电荷数依次增大。其中A原子核外有三个未成对电子;A与B可形成离子化合物B3A2;C元素是地壳中含量最高的金属元素;D原子核外的M层中有两对成对电子;E原子核外最外层只有1个电子,其余各层电子均充满。请根据以上信息,回答下列问题(答题时,A、B、C、D、E用所对应的元素符号表示):
(1)B的轨道排布式是_____________________________________,A、B、C、D的第一电离能由小到大的顺序为___________________________________________。
(2)B的氯化物的熔点远高于C的氯化物的熔点,理由是________________________;
(3)A的最高价含氧酸根离子中,其中心原子采取____________杂化,D的低价氧化物分子的空间构型是___________________________。
(4)A、E形成某种化合物的晶胞结构如图所示,则其化学式为________________;(每个球均表示1个原子) 若相邻A原子和E原子间的距离为a nm,阿伏伽德罗常数为NA,则该晶体的密度为_____________g/cm3(用含a、NA的符号表示)。

查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列实验操作、现象和结论均正确,且存在对应关系的是
选项 | 实验操作 | 实验现象 | 结论 |
A | 将NaOH溶液逐滴滴加到AlC13溶液中至过量 | 先产生白色胶状沉淀,后沉淀溶解 | Al(OH)3是两性氢氧化物 |
B | NaHCO3溶液与NaAlO溶液混合 | 生成白色沉淀 | 结合H+的能力:CO32->AlO2- |
C | 向盛有Na2SiO3,溶液的试管中滴加1滴酚酞,然后逐滴加入稀盐酸至过量 | 试管中红色逐渐褪去,出现白色凝胶 | 非金属性:Cl>Si |
D |
| 白色固体先变为淡黄色,后变为黄色 | 溶度积常数:Ksp(AgCl)>Ksp(AgBr)>Ksp(AgI) |
A.AB.BC.CD.D
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列现象与氢键有关的是( )
①![]() 的熔、沸点比
的熔、沸点比![]() 的高
的高
②乙醇能与水以任意比混溶,而乙硫醇(![]() )微溶于水
)微溶于水
③冰的密度比液态水的密度小
④邻羟基苯甲酸的熔、沸点比对羟基苯甲酸的低
⑤![]() 比
比![]() 稳定
稳定
⑥接近沸点的水蒸气的相对分子质量测量值大于实际值
A.①②③④⑥B.①②③④⑤C.②③④⑤D.①②③④⑤⑥
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】氮氧化物(主要为NO和NO2)是大气污染物,如何有效地消除氮氧化物的污染是目前科学家们研究的热点问题。
(1)用尿素[CO(NH2)2]吸收氮氧化物是一种可行的方法。
①尿素在高温条件下与NO2反应转化成无毒气体,该反应的化学方程式为___。用尿素溶液也可吸收氮氧化物,研究表明,当混合气体中![]() =1时,总氮还原率最高,随着,
=1时,总氮还原率最高,随着,![]() 比值增大,总氮还原率降低的主要原因是___。
比值增大,总氮还原率降低的主要原因是___。
②在一个体积为1L的恒容密闭容器中充入1molCO2和1molNH3,在恒定温度下使其发生反应2NH3(g)+CO2(g)![]() NH2CONH2(s)+H2O(g) △H<0并达到平衡,混合气体中氨气的体积分数随时间的变化如图所示。
NH2CONH2(s)+H2O(g) △H<0并达到平衡,混合气体中氨气的体积分数随时间的变化如图所示。
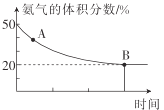
则A点时v正(CO2)___(填“>”“<”或“=”)B点时v正(CO2),原因是___。B点时,NH3的转化率为___。
③下列有关反应2NH3(g)+CO2(g)![]() CO(NH2)2(s)+H2O(g)的说法正确的是___。
CO(NH2)2(s)+H2O(g)的说法正确的是___。
A.分离出少量的尿素,NH3的转化率将增大
B.反应达到平衡时,降低反应体系的温度,CO2的浓度减小
C.NH3的转化率始终等于CO2的转化率
D.加入有效的催化剂能够提高尿素的产率
(2)已知O3氧化氮氧化物的主要反应的热化学方程式如下:
2NO(g)+O2(g)=2NO2(g) △H1=akJ·mol-1
NO(g)+O3(g)=NO2(g)+O2(g) △H2=bkJ·mol-1
6NO2(g)+O3(g)=3N2O5(g) △H3=ckJ·mol-1
则反应4NO2(g)+O2(g)=2N2O5(g)△H=___(用含a、b、c的代数式表示)kJ·mol-1。
(3)氮氧化物也可用碱液吸收。若NO和NO2的混合气体被NaOH溶液完全吸收,只生成一种盐,则该盐的化学式为___;已知常温下Ka(HNO2)=5×10-4,则反应HNO2(aq)+NaOH(aq)![]() NaNO2(aq)+H2O(l)的平衡常数K=___。
NaNO2(aq)+H2O(l)的平衡常数K=___。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com