
| A.NaCl | B.干冰 | C.晶体硅 | D.石英 |
科目:高中化学 来源:不详 题型:单选题
| A.含有共价键的化合物一定是共价化合物 |
| B.共价化合物中一定含有共价键 |
| C.含有离子键的化合物一定是离子化合物 |
| D.双原子单质分子中的共价键一定是非极性键 |
查看答案和解析>>
科目:高中化学 来源:不详 题型:填空题
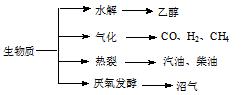
 CH3OH(g) △H= -90.8kJ·mol-1。
CH3OH(g) △H= -90.8kJ·mol-1。| 容器 | 甲 | 乙 | 丙 |
| 反应物投入量 | 1molCO 、2molH2 | 1mol CH3OH | 2molCO、4molH2 |
| CH3OH的浓度(mol/L) | c1 | c2 | c3 |
| 反应的能量变化 | 放出Q1 kJ | 吸收Q2 kJ | 放出Q3 kJ |
| 平衡常数 | K1 | K2 | K3 |
| 反应物转化率 | α1 | α 2 | α3 |
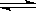 CH3OCH3(g)+CO2(g)
CH3OCH3(g)+CO2(g)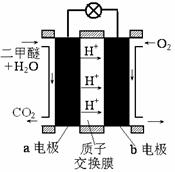
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
| A.氢键比范德华力强,所以它属于化学键 | |
| B.分子间形成的氢键使物质的熔点和沸点升高 | C.沸点HI>HBr>HCl>HF |
| D.H2O是一种稳定的化合物,这是由于H2O之间形成氢键所致 |
查看答案和解析>>
科目:高中化学 来源:不详 题型:填空题
查看答案和解析>>
科目:高中化学 来源:不详 题型:填空题
| 分子或离子 | PbCl2 | XeF4 | SnCl62- | PF3Cl2 | Hg Cl42- Cl42- | ClO4-- |
| 空间 构型 | | | | | | |
查看答案和解析>>
科目:高中化学 来源:不详 题型:填空题
| 元素 | A | B | C |
| 结构信息 | 基态原子核外有两个电子层,最外层有3个未成对的电子 | 基态原子的M层有1对成对的p电子 | 基态原子核外电子排布为[Ar]3s104sx,有+1、+ 2两种常见化合价 2两种常见化合价 |
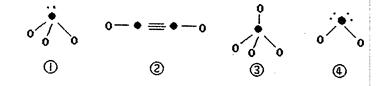
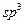 杂化形成化学键是 (填写序号);在②的分子中有 个
杂化形成化学键是 (填写序号);在②的分子中有 个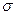 键和 个
键和 个 键。
键。查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com