
”¾ĢāÄæ”æ“Óijŗ¬ÓŠFeCl2”¢FeCl3”¢CuCl2µÄ¹¤Ņµ·ĻŅŗÖŠ»ŲŹÕĶ²¢ÖʱøĀČ»ÆĢś¾§ĢåµÄĮ÷³ĢČēĻĀ£ŗ
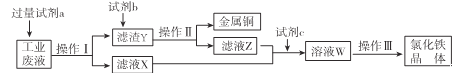
ŅŃÖŖ£ŗFeCl3ŌŚ¼ÓČČĒéæöĻĀÓėĖ®·“Ӧɜ³ÉFe£ØOH£©3”£
»Ų“šĻĀĮŠĪŹĢā£ŗ
£Ø1£©ŹŌ¼ĮaŹĒ ____________£¬¹żĮæµÄŌŅņ______________________”£
£Ø2£©²Ł×÷¢ņŹĒ___________£¬ÓƵ½µÄ²£Į§ŅĒĘ÷___________________________”£
£Ø3£©ČōŹŌ¼ĮCŹĒCl2£¬Ōņ·“Ó¦µÄĄė×Ó·½³ĢŹ½£ŗ __________________________”£
£Ø4£©ĀĖŅŗX”¢ZÖŠ¶¼ÓŠĶ¬Ņ»ÖÖČÜÖŹ£¬ĒėÉč¼ĘŹµŃéŃéÖ¤øĆČÜÖŹµÄĄė×Ó£ŗ___________”£
£Ø5£©²Ł×÷¢óÓ¦øĆŹĒ£Ø______£©
A Õō·¢ BÕōĮó C ·ÖŅŗ D ½į¾§
”¾“š°ø”æ Fe Ź¹ĀČ»ÆĢś/ĀČ»ÆĶĶźČ«·“Ó¦ ¹żĀĖ ÉÕ± Ā©¶· ²£Į§°ō 2Fe2++Cl2=2Fe2+ + 2Cl- Č”Ī“ÖŖŅŗÉŁĮæ,µĪ¼ÓKSCNČÜŅŗ,ĪŽĆ÷ĻŌĻÖĻó£»ŌŁµĪ¼ÓĀČĖ®ŗó,ČÜŅŗ±äĪŖŃŖŗģÉ«.Ö¤Ć÷ŗ¬ÓŠFe2+£¬ĮķČ”Ī“ÖŖŅŗÉŁĮæ,µĪ¼ÓĻ”ĻõĖįĖį»ÆµÄAgNO3ČÜŅŗ,²śÉś°×É«³Įµķ.Ö¤Ć÷ŗ¬ÓŠCl-. D
”¾½āĪö”æÓÉĢāæÉÖŖ£¬±¾Į÷³ĢÖʱøĀČ»ÆĢś¾§Ģ壬¹żĮæµÄaæÉŅŌ±»ŹŌ¼ĮbČܽā£¬ĒŅČܽāŗóæÉŅŌŗĶĀĖŅŗXŗĻ²¢ŗóÖʱøĀČ»ÆĢś£¬ĖłŅŌaŹĒĢś”¢bŹĒŃĪĖį”¢cŹĒĀČĘų£»
£Ø1£©æÉĶĘÖŖaĪŖFe£¬¼ÓČė¹żĮæµÄŹŌ¼ĮFeµÄÄæµÄŹĒŹ¹ĀČ»ÆĢśŗĶĀČ»ÆĶ³ä·Ö·“Ó¦£»
£Ø2£©²Ł×÷IIŹĒµĆµ½½šŹōĶŗĶĀĖŅŗ£¬ĖłŅŌ²Ł×÷IIÓ¦ŹĒ¹żĀĖ£¬ÓƵ½µÄ²£Į§ŅĒĘ÷ŹĒÉÕ±”¢Ā©¶·”¢²£Į§°ō£»
£Ø3£©¾¹ż²Ł×÷IµĆµ½µÄĀĖŅŗXŹĒFeCl2ČÜŅŗ£¬ĀĖŅŗZŹĒĀČ»ÆŃĒĢśŗĶŃĪĖį»ģŗĻČÜŅŗ£¬ĶØČėĀČĘų·¢ÉśµÄĄė×Ó·“Ó¦ŹĒ2Fe2++Cl2=2Fe3++2Cl-£»
£Ø4£©“Ó£Ø3£©µÄ·ÖĪöæÉÖŖŗ¬ÓŠµÄĶ¬Ņ»ČÜÖŹĪŖFeCl2£¬¼ģŃéøĆĄė×ӵķ½·ØŹĒ£ŗČ”Ī“ÖŖŅŗÉŁĮæ,µĪ¼ÓKSCNČÜŅŗ,ĪŽĆ÷ĻŌĻÖĻó£»ŌŁµĪ¼ÓĀČĖ®ŗó,ČÜŅŗ±äĪŖŃŖŗģÉ«.Ö¤Ć÷ŗ¬ÓŠFe2+£¬ĮķČ”Ī“ÖŖŅŗÉŁĮæ,µĪ¼ÓĻ”ĻõĖįĖį»ÆµÄAgNO3ČÜŅŗ,²śÉś°×É«³Įµķ.Ö¤Ć÷ŗ¬ÓŠCl-£»
£Ø5£©²Ł×÷IIIŹĒĪŖĮĖ“ÓČÜŅŗÖŠ»ńµĆ¾§Ģ壬ӦŌŚČ·±£ČÜŅŗÖŠ“ęŌŚŃĪĖįµÄĢõ¼žĻĀ£¬Õō·¢ÅØĖõ”¢ĄäČ“½į¾§£¬Ó¦²ÉÓĆ½į¾§µÄ·½Ź½µĆµ½ĀČ»ÆĢś¾§Ģ壬“š°øŃ”D”£


 ŌĶĮæģ³µĻµĮŠ“š°ø
ŌĶĮæģ³µĻµĮŠ“š°ø
| Äź¼¶ | øßÖŠæĪ³Ģ | Äź¼¶ | ³õÖŠæĪ³Ģ |
| øßŅ» | øßŅ»Ćā·ŃæĪ³ĢĶĘ¼ö£” | ³õŅ» | ³õŅ»Ćā·ŃæĪ³ĢĶĘ¼ö£” |
| ø߶ž | ø߶žĆā·ŃæĪ³ĢĶĘ¼ö£” | ³õ¶ž | ³õ¶žĆā·ŃæĪ³ĢĶĘ¼ö£” |
| øßČż | øßČżĆā·ŃæĪ³ĢĶĘ¼ö£” | ³õČż | ³õČżĆā·ŃæĪ³ĢĶĘ¼ö£” |
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ
”¾ĢāÄæ”æ²čŅ¶ÖŠĢśŌŖĖŲµÄ¼ģŃéæɾ¹żŅŌĻĀĖÄøö²½ÖčĶź³É£¬ø÷²½ÖčÖŠŃ”ÓƵďµŃéÓĆĘ·²»Äܶ¼ÓƵ½µÄŹĒ£Ø £© 
A.½«²čŅ¶×ĘÉÕ»Ņ»Æ£¬Ń”ÓĆ¢Ł”¢¢ŚŗĶ¢į
B.ÓĆÅØĻõĖįČܽā²čŅ¶»Ņ²¢¼ÓÕōĮóĖ®Ļ”ŹĶ£¬Ń”ÓĆ¢Ü”¢¢ŽŗĶ¢ß
C.¹żĀĖµĆµ½µÄĀĖŅŗ£¬Ń”ÓĆ¢Ü”¢¢ŻŗĶ¢ß
D.¼ģŃéĀĖŅŗÖŠµÄFe3+ £¬ Ń”ÓĆ¢Ū”¢¢ąŗĶ¢ā
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ
”¾ĢāÄæ”æÓŠŅ»°üNaHCO3ŗĶKHCO3µÄ»ģŗĻĪļѳʷ£®Ä³ŃŠ¾æŠŌѧĻ°Š”×é¶ŌĘä½ųŠŠĮĖČēĻĀĢ½¾æ£¬Ēė°“ŅŖĒóĶź³ÉĻĀĮŠĢ½¾æ±Øøę£®
£Ø1£©”¾Ģ½¾æÄæµÄ”æŹµŃé²ā¶Øѳʷ֊NaHCO3ŗĶKHCO3ĪļÖŹµÄĮæÖ®±Č£® ”¾Ģ½¾æĖ¼Ā·”æÉč¼ĘŹµŃé²āĮæÓŠ¹Ų·“Ó¦ĪļŗĶÉś³ÉĪļµÄĮ棬²¢Ķعż¼ĘĖćČ·¶Øѳʷ֊NaHCO3ŗĶKHCO3ĪļÖŹµÄĮæÖ®±Č£®
”¾ŹµŃéĢ½¾æ”æŹµŃé×°ÖĆČēĶ¼¼×ĖłŹ¾£®½«Ņ»¶ØÖŹĮæµÄ»ģŗĻĪļѳʷ¼ÓČė׶ŠĪĘæÖŠ£¬ÓĆÕėĶ²a×¢ČėŅ»¶ØĢå»żµÄĻ”ĮņĖį³ä·Ö·“Ó¦£¬ŌŁÓĆÕėĶ²bŹÕ¼ÆÉś³ÉĘųĢåµÄĢå»ż£ØŗöĀŌÕėĶ²¹Ü±Ś¼äµÄĦ²Į£©£®
Čē¹ūĶł×¶ŠĪĘæ֊עČėµÄĻ”ĮņĖįµÄĢå»żĪŖV1mL£¬³ä·Ö·“Ó¦ŗó£¬ÕėĶ²bÖŠĘųĢåµÄ¶ĮŹżĪŖV2mL£¬Ōņ·“Ó¦ÖŠÉś³ÉµÄCO2ĘųĢåĢå»żĪŖmL£®Š“³ö׶ŠĪĘæÖŠ·“Ó¦µÄĄė×Ó·½³ĢŹ½ £®
”¾½į¹ū“¦Ąķ”æ׶ŠĪĘæÖŠ·ÅÓŠ»ģŗĻ¾łŌȵÄNaHCO3ŗĶKHCO3µÄѳʷ3.6g£¬Ļņ׶ŠĪĘæÖŠµĪČėŅ»¶ØĮæµÄĻ”ĮņĖį£¬Éś³ÉµÄĘųĢåĢå»ż£ØŅŃ»»Ėć³É±ź×¼×“æö£©Óė¼ÓČėµÄĻ”ĮņĖįµÄĢå»ż¹ŲĻµČēĶ¼ŅŅĖłŹ¾£ŗ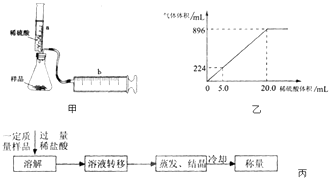
ŹµŃéĖłÓĆĻ”ĮņĖįÖŠČÜÖŹµÄĪļÖŹµÄĮæÅØ¶ČŹĒmol/L£®
£Ø2£©ŃłĘ·ÖŠNaHCO3ŗĶKHCO3ĪļÖŹµÄĮæÖ®±ČĪŖ £® ”¾ĶŲÕ¹Ģ½¾æ”æijĶ¬Ń§Éč¼ĘĮĖĮķŅ»ÖÖ·½°ø£¬Ęä²Ł×÷Į÷³ĢČēĶ¼±ū£ŗŌŚ×ŖŅĘČÜŅŗŹ±£¬Čē¹ūČÜŅŗ×ŖŅĘ²»ĶźČ«£¬Ōņ²āµĆµÄ»ģŗĻĪļÖŠNaHCO3ŗĶKHCO3ĪļÖŹµÄĮæÖ®±Č£ØŃ”Ģī”°Ę«“ó”±”¢”°Ę«Š””±»ņ”°²»±ä”±£©£®
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ
”¾ĢāÄæ”æ8.34g FeSO47H2OѳʷŌŚøō¾ųæÕĘųĢõ¼žĻĀŹÜČČĶŃĖ®¹ż³ĢµÄČČÖŲĒśĻߣØѳʷ֏ĮæĖęĪĀ¶Č±ä»ÆµÄĒśĻߣ©ČēĶ¼ĖłŹ¾£®ĻĀĮŠĖµ·ØÖŠÕżČ·µÄŹĒ£Ø £© 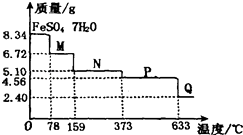
A.ĪĀ¶ČĪŖ78”ꏱ¹ĢĢåĪļÖŹMµÄ»ÆѧŹ½ĪŖFeSO4?5H2O
B.ĪĀ¶ČĪŖl59”ꏱ¹ĢĢåĪļÖŹNµÄ»ÆѧŹ½ĪŖFeSO4?3H2O
C.ŌŚøō¾ųæÕĘųĢõ¼žĻĀÓÉNµĆµ½PµÄ»Æѧ·½³ĢŹ½ĪŖFeSO4 ![]() ?FeO+SO3”ü
?FeO+SO3ӟ
D.Č”ŹŹĮæ380”ꏱĖłµĆµÄѳʷP£¬øō¾ųæÕĘų¼ÓČČÖĮ650”ę£¬µĆµ½Ņ»ÖÖ¹ĢĢåĪļÖŹQ£¬Ķ¬Ź±ÓŠĮ½ÖÖĪŽÉ«ĘųĢåÉś³É£¬QµÄ»ÆѧŹ½ĪŖFe2O3
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ
”¾ĢāÄæ”æĶ¬Ņ»ÖÜĘŚČżÖÖ·Ē½šŹōŌŖĖŲX”¢Y”¢Z£¬Ęä×īøß¼ŪŃõ»ÆĪļµÄĖ®»ÆĪļµÄĖįŠŌÓÉĒæµ½ČõµÄĖ³ŠņŹĒ£ŗHXO4>H2YO4>H3ZO4”£ĻĀĮŠĖµ·ØÕżČ·µÄŹĒ£Ø £©
A£®ŌŖĖŲµÄ·Ē½šŹōŠŌ£ŗX<Y<Z
B£®ĘųĢ¬Ēā»ÆĪļµÄĪČ¶ØŠŌ£ŗHX>H2Y>ZH3
C£®ŅõĄė×ӵĻ¹ŌŠŌ£ŗX->Y2->Z3-
D£®X”¢Y”¢ZŅĄ“ĪĪ»ÓŚ¢õA×唢¢öA×唢¢÷A×唣
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ
”¾ĢāÄæ”æĘū³µĪ²ĘųÖŠ£¬²śÉśNOµÄ·“Ó¦ĪŖ£ŗN2£Øg£©+O2£Øg£©2NO£Øg£©£¬Ņ»¶ØĢõ¼žĻĀ£¬µČĪļÖŹµÄĮæµÄN2£Øg£©ŗĶO2£Øg£©ŌŚŗćČŻĆܱÕČŻĘ÷ÖŠ·“Ó¦£¬ČēĶ¼ĒśĻßa±ķŹ¾øĆ·“Ó¦ŌŚĪĀ¶ČTĻĀN2µÄÅضČĖꏱ¼äµÄ±ä»Æ£¬ĒśĻßb±ķŹ¾øĆ·“Ó¦ŌŚÄ³Ņ»ĘšŹ¼Ģõ¼žøı䏱N2µÄÅضČĖꏱ¼äµÄ±ä»Æ£®ĻĀĮŠŠšŹöÕżČ·µÄŹĒ£Ø £© 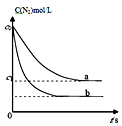
A.ČōĒśĻßb¶ŌÓ¦µÄĢõ¼žøıäŹĒĪĀ¶Č£¬æÉÅŠ¶ĻøĆ·“Ó¦µÄ”÷H£¼0
B.ĪĀ¶ČTĻĀ£¬Ėę×Å·“Ó¦µÄ½ųŠŠ£¬»ģŗĻĘųĢåµÄĆÜ¶Č¼õŠ”
C.ĒśĻßb¶ŌÓ¦µÄĢõ¼žøıäæÉÄÜŹĒ¼ÓČėĮĖ“߻ƼĮ
D.ĪĀ¶ČTĻĀ£¬øĆ·“Ó¦µÄĘ½ŗā³£ŹżK= ![]()
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ
”¾ĢāÄæ”æĻņ50mL NaOHČÜŅŗÖŠÖš½„ĶØČėŅ»¶ØĮæµÄCO2£Ø¼ŁÉčČÜŅŗĢå»ż²»±ä£©£¬ĖęŗóČ”“ĖČÜŅŗ10mL£¬½«ĘäĻ”ŹĶÖĮ100mL£¬²¢Ļņ“ĖĻ”ŹĶŗóµÄČÜŅŗÖŠÖšµĪ¼ÓČė0.1molL©1µÄŃĪĖį£¬²śÉśCO2ĘųĢåµÄĢå»ż£Ø±ź×¼×“æöĻĀ£©ÓėĖł¼ÓČėµÄŃĪĖįµÄĢå»ż¹ŲĻµČēĶ¼ĖłŹ¾£® 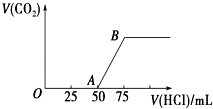
£Ø1£©Š“³öOA¶ĪĖł·¢Éś·“Ó¦µÄĄė×Ó·½³ĢŹ½£ŗ £®
£Ø2£©NaOHŌŚĪüŹÕCO2ŗó£¬ĖłµĆČÜŅŗµÄČÜÖŹĪŖ £¬ ĘäĪļÖŹµÄĮæÅضČÖ®±ČĪŖ £®
£Ø3£©²śÉśµÄCO2Ģå»ż£Ø±ź×¼×“æöĻĀ£©ĪŖ £®
£Ø4£©ŌNaOHČÜŅŗµÄĪļÖŹµÄĮæÅضČĪŖ £®
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ
”¾ĢāÄæ”æĻĀĮŠŹĀŹµ²»ÄÜÓĆŌµē³ŲĄķĀŪ½āŹĶµÄŹĒ£Ø £©
A”¢ĀĮʬ²»ÓĆĢŲŹā·½·Ø±£“ę
B”¢ÉśĢś±Č“æĢśŅ×ÉśŠā
C”¢ÖĘĒāĘųŹ±ÓĆ“ÖŠæ¶ų²»ÓĆ“æŠæ
D”¢¹¤³ĢŹ©¹¤¶ÓŌŚĢśÖĘĖ®¹ÜĶāĖ¢Ņ»²ć”°Ņų·Ū”±
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ
”¾ĢāÄæ”æĒėŌ¤²āÓŠ»śĪļ±ūĻ©Ėį£ØCH2=CH-COOH£©µÄ·¢ÉśµÄ·“Ó¦ĄąŠĶæÉÄÜÓŠ£Ø””””£©
¢Ł¼Ó³É·“Ó¦¢ŚĖ®½ā·“Ó¦¢Ūõ„»Æ·“Ó¦¢ÜÖŠŗĶ·“Ó¦¢ŻŃõ»Æ·“Ó¦.
A. Ö»ÓŠ¢Ł¢ŪB. Ö»ÓŠ¢Ł¢Ū¢ÜC. ¢Ł¢Ś¢Ū¢Ü¢ŻD. Ö»ÓŠ¢Ł¢Ū¢Ü¢Ż
²éæ““š°øŗĶ½āĪö>>
°Ł¶ČÖĀŠÅ - Į·Ļ°²įĮŠ±ķ - ŹŌĢāĮŠ±ķ
ŗž±±Ź”»„ĮŖĶųĪ„·ØŗĶ²»Į¼ŠÅĻ¢¾Ł±ØĘ½ĢØ | ĶųÉĻÓŠŗ¦ŠÅĻ¢¾Ł±Ø×ØĒų | µēŠÅÕ©Ę¾Ł±Ø×ØĒų | É꥜Ź·ŠéĪŽÖ÷ŅåÓŠŗ¦ŠÅĻ¢¾Ł±Ø×ØĒų | ÉęĘóĒÖČؾŁ±Ø×ØĒų
Ī„·ØŗĶ²»Į¼ŠÅĻ¢¾Ł±Øµē»°£ŗ027-86699610 ¾Ł±ØÓŹĻä£ŗ58377363@163.com