
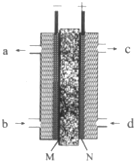
 甲醇是燃料电池的常见原料,现已熔融的K2CO3为电解质,以甲醇为燃料,空气为氧化剂,以具有催化作用和导电性能的稀土金属材料为电极.如图是甲醇燃料电池模型,试回答下列问题:
甲醇是燃料电池的常见原料,现已熔融的K2CO3为电解质,以甲醇为燃料,空气为氧化剂,以具有催化作用和导电性能的稀土金属材料为电极.如图是甲醇燃料电池模型,试回答下列问题:| 16g |
| 32g/mol |


科目:高中化学 来源: 题型:
 (一)常温下,在27.5g水中溶解12.5g CuSO4?5H2O,恰好达到饱和,该溶液密度为1.21g/cm3,求:
(一)常温下,在27.5g水中溶解12.5g CuSO4?5H2O,恰好达到饱和,该溶液密度为1.21g/cm3,求:查看答案和解析>>
科目:高中化学 来源: 题型:
查看答案和解析>>
科目:高中化学 来源: 题型:
查看答案和解析>>
科目:高中化学 来源: 题型:
| t(s) | 200 | 400 | 800 |
| c(A)(mol?L-1) | 1.45 | 1.28 | 1.00 |
| c(B)(mol?L-1) | 0.38 | 0.72 | 1.28 |
| c(C)(mol?L-1) | 0.095 | 0.18 | 0.32 |
查看答案和解析>>
科目:高中化学 来源: 题型:
 如图是几种烷烃的球棍模型,试回答下列问题:
如图是几种烷烃的球棍模型,试回答下列问题:查看答案和解析>>
科目:高中化学 来源: 题型:
| A、最外层电子数:O>N>C |
| B、碱性:Al(OH)3>Mg(OH)2>NaOH |
| C、F、Cl、Br三种原子的核外电子层数依次增多 |
| D、P、S、Cl三种元素的最高价氧化物对应水化物酸性依次增强 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、标准状况下,1mol任何物质的体积约为22.4L |
| B、1mol气体的体积约为22.4L |
| C、1mol氖气和1mol氧气体积相同 |
| D、标准状况下,1mol 空气的体积约为22.4L |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com