
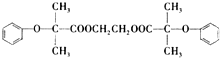 )可由下列路线合成:
)可由下列路线合成: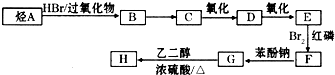
| HBr/过氧化物 |
| Br2/红磷 |

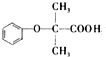 ,E在溴、红磷条件下反应得到F,F与苯酚钠反应得到G,结合反应信息Ⅱ可知F为
,E在溴、红磷条件下反应得到F,F与苯酚钠反应得到G,结合反应信息Ⅱ可知F为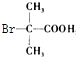 ,E为(CH3)2CHCOOH,逆推可得D为(CH3)2CHCHO,C为(CH3)2CHCH2OH,B为(CH3)2CHCH2Br、A为(CH3)2C=CH2,据此解答.
,E为(CH3)2CHCOOH,逆推可得D为(CH3)2CHCHO,C为(CH3)2CHCH2OH,B为(CH3)2CHCH2Br、A为(CH3)2C=CH2,据此解答. ,E在溴、红磷条件下反应得到F,F与苯酚钠反应得到G,结合反应信息Ⅱ可知F为
,E在溴、红磷条件下反应得到F,F与苯酚钠反应得到G,结合反应信息Ⅱ可知F为 ,E为(CH3)2CHCOOH,逆推可得D为(CH3)2CHCHO,C为(CH3)2CHCH2OH,B为(CH3)2CHCH2Br、A为(CH3)2C=CH2,
,E为(CH3)2CHCOOH,逆推可得D为(CH3)2CHCHO,C为(CH3)2CHCH2OH,B为(CH3)2CHCH2Br、A为(CH3)2C=CH2, ,
, ,其同分异构体符合下列条件:①能使FeCl3溶液显紫色,说明含有酚羟基;②苯环上只有2个取代基,③1mol该物质最多可消耗3mol NaOH,可以确定另外取代基为-OOCCH2CH2CH3或-OOCCH(CH3)2,各有邻、间、对三种位置,故符合条件的同分异构体共有6种,其中核磁共振氢谱为5组峰的为
,其同分异构体符合下列条件:①能使FeCl3溶液显紫色,说明含有酚羟基;②苯环上只有2个取代基,③1mol该物质最多可消耗3mol NaOH,可以确定另外取代基为-OOCCH2CH2CH3或-OOCCH(CH3)2,各有邻、间、对三种位置,故符合条件的同分异构体共有6种,其中核磁共振氢谱为5组峰的为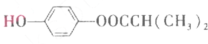 ,
,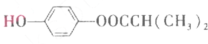 ;
; ,
, .
.


 培优好卷单元加期末卷系列答案
培优好卷单元加期末卷系列答案 一线名师权威作业本系列答案
一线名师权威作业本系列答案科目:高中化学 来源: 题型:
 甲烷分子中4个氢原子被苯基取代,如图所示,对该分子描述正确的是( )
甲烷分子中4个氢原子被苯基取代,如图所示,对该分子描述正确的是( )| A、该物质属于芳香烃,是苯的同系物 |
| B、所有的碳原子可能在同一平面 |
| C、此物质属于高分子化合物 |
| D、此分子的一氯取代物有3种 |
查看答案和解析>>
科目:高中化学 来源: 题型:
查看答案和解析>>
科目:高中化学 来源: 题型:
查看答案和解析>>
科目:高中化学 来源: 题型:
查看答案和解析>>
科目:高中化学 来源: 题型:

查看答案和解析>>
科目:高中化学 来源: 题型:
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、在0.1mol?L-1 CH3COONa溶液中,c(OH-)=c(CH3COOH)+c(H+) |
| B、0.1mol?L-1的KAl(SO4)2溶液中:c(SO42-)>c(Al3+)>c(OH-)>c(H+) |
| C、pH相等的NaOH、CH3COONa和NaHCO3三种溶液,则有:c(NaOH)<c(CH3COONa)<c(NaHCO3) |
| D、等体积、等物质的量浓度的NaX和弱碱HX混合后的溶液,若溶液呈酸性,则有c(Na+)>c(HX)>c(X-)>c(H+)>c(OH-) |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com