
下列说法正确的是
A. 镁着火不能用CO2灭火
B. 钠只有在加热条件下才能与氯气反应
C. 浓硫酸有氧化性,稀硫酸没有氧化性
D. SO2能使酸性高锰酸钾溶液褪色,说明SO2具有漂白性
科目:高中化学 来源:2016-2017学年江西省南昌市高二上学期期末考试化学试卷(解析版) 题型:选择题
公元前一世纪,我国已使用天然气,天然气的主要成分为甲烷。下列关于甲烷的叙述中,错误的是
A. 通常情况下,甲烷跟强酸、强碱、强氧化剂不起反应
B. 甲烷化学性质比较稳定,不能被任何氧化剂氧化
C. 甲烷跟氧气反应无论生成CH3Cl、CH2Cl、CHCl3还是CCl4,都属于取代反应
D. 甲烷的四种取代物都难溶于水
查看答案和解析>>
科目:高中化学 来源:2017届江苏省、溧水高级中学)等六校高三2月联考化学试卷(解析版) 题型:选择题
下列反应的离子方程式书写不正确的是
A. 用氨水吸收过量的二氧化硫:NH3·H2O+SO2=HSO3-+NH4+
B. 用过氧化氢从酸化的海带灰浸出液中提取碘:2I-+H2O2+2H+ = I2+2H2O
C. 向NH4Al(SO4)2溶液中滴入Ba(OH) 2溶液恰好使SO42-完全沉淀:2Ba2+ + Al3+ + 2SO42- + 4OH- = AlO2- + 2BaSO4↓+ 2H2O
D. 向含0.1mol·L-1 Na2CO3和0.2mol·L-1 NaOH的混合溶液中加入等体积的0.15mol·L-1的硫酸:CO32-+3H++2OH- = 2H2O+HCO3-
查看答案和解析>>
科目:高中化学 来源:2017届浙江省台州市高三上学期期末质量评估考试化学试卷(解析版) 题型:选择题
下列说法正确的是
A. HCl、HBr、HI的分子间作用力依次增大,热稳定性也依次增强
B. N2和Cl2两种分子中,每个原子的最外层都具有8电子稳定结构
C. 在O2、CO2和SiO2中,都存在共价键,它们均由分子构成
D. KOH和MgCl2都是离子晶体,均在共价键和离子键
查看答案和解析>>
科目:高中化学 来源:2017届浙江省台州市高三上学期期末质量评估考试化学试卷(解析版) 题型:选择题
下列离子方程式正确的是
A. 澄清石灰水中加盐酸:2H++Ca(OH)2=Ca2++2H2O
B. 向NaHCO3溶液中加入NaOH溶液:HCO3-+OH-=CO32-+H2O
C. 氯气溶于水:Cl2+H2O 2H++ClO-+Cl-
2H++ClO-+Cl-
D. 向Ba(OH)2溶液中滴加稀硫酸:Ba2++OH-+H++SO42-=BaSO4↓+H2O
查看答案和解析>>
科目:高中化学 来源:2017届江苏省高三下学期开学考试化学试卷(解析版) 题型:简答题
化合物H是合成植物生长调节剂赤霉酸的重要中间体,其合成路线如下:
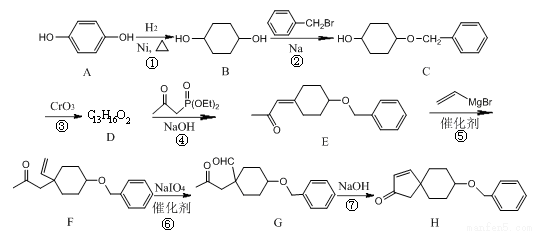
(1)化合物E的含氧官能团为______和______(填官能团的名称)。
(2)反应②的类型为__________。
(3)写出一种满足下列条件的C的同分异构体的结构简式____________。
I.分子含有1个苯环;
II.能发生银镜反应和水解反应;
III.分子有4种不同化学环境的氢。
(4)化合物C被氧化生成化合物D,D的结构简式为_______________。
(5)根据已有知识并结合相关信息,写出以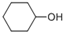 为有机原料制备
为有机原料制备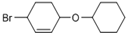 的合成路线流程图(无机试剂任用,可选择适当有机溶剂,合成路线流程图示例见本题题干)___________________。
的合成路线流程图(无机试剂任用,可选择适当有机溶剂,合成路线流程图示例见本题题干)___________________。
查看答案和解析>>
科目:高中化学 来源:2017届福建省漳州市八校高三2月联考化学试卷(解析版) 题型:实验题
亚氯酸钠(NaClO2)是重要的漂白剂。某小组开展如下实验,按如图装置制取无水NaClO2晶体,回答下列问题:
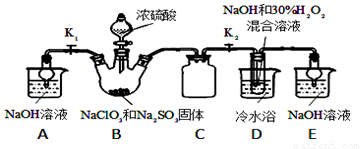
已知:NaClO2饱和溶液在低于38℃时析出NaClO2•3H2O,高于38℃时析出NaClO2,高于60℃时NaClO2分解成NaClO3和NaCl.
(1)装置C的作用是_________________;
(2)已知装置B中的产物有ClO2气体,则B中反应的方程式为_________________;装置D中反应生成NaClO2的化学方程式为_________________________;
(3)从装置D反应后的溶液中获得无水NaClO2晶体的操作步骤为:①减压,55℃蒸发结晶;②____________;③用38℃~60℃热水________;④在_____________条件下干燥得到成品.
(4)如果撤去D中的冷水浴,可能导致产品中混有的杂质是_________和____________;
(5)测定样品中NaClO2的纯度.测定时进行如下实验:
准确称一定质量的样品,加入适量蒸馏水和过量的KI晶体,在酸性条件下发生如下反应:ClO2-+4I-+4H+═2H2O+2I2+Cl-,将所得混合液稀释成100mL待测溶液.取25.00mL待测溶液,加入淀粉溶液做指示剂,用c mol•L-1 Na2S2O3标准液滴定至终点,测得消耗标准溶液体积的平均值为V mL(已知:I2+2S2O32-═2I-+S4O62-).请计算所称取的样品中NaClO2的物质的量为__________.
查看答案和解析>>
科目:高中化学 来源:2017届山东省菏泽市高三上学期期末学分认定考试B卷化学试卷(解析版) 题型:实验题
化学是一门以实验为基础的自然科学,是研究物质的性质的重要途径。某化学兴趣小组为探究SO2的性质,按下图所示装置进行实验。

已知:Na2SO3+H2SO4(浓)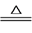 Na2SO4+SO2↑+H2O,请回答下列问题:
Na2SO4+SO2↑+H2O,请回答下列问题:
(1) 装置A中盛放浓硫酸的仪器名称是__________________。
(2) 实验过程中,C中的现象是____________,说明SO2具有_________性。
(3) 实验过程中,观察到装置B中出现了明显的白色沉淀。为探究该白色沉淀的成分,该小组同学进行了如下实验:
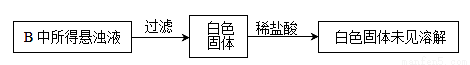
根据实验事实判断该白色沉淀的成分是_______________(填化学式),产生该白色沉淀的原因可能是_____________(填字母编号)。
a.BaSO3既不溶于水也不溶于酸
b.BaCl2溶液中可能溶解有氧气
c.BaCl2溶液中可能混有NaOH
d.由A制得的SO2气体中可能混有氧气
(4)如果将装置A中的浓H2SO4换作浓HNO3,对此实验是否有影响并说明理由_________________
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com