
【题目】一定温度下,浓度均为0.1mol/L的下列溶液中,含H+离子浓度最小的是( )
A.CH3COOH B.H2SO4 C.HNO3 D.HCl
 阅读快车系列答案
阅读快车系列答案科目:高中化学 来源: 题型:
【题目】鉴别淀粉、蛋白质、葡萄糖水溶液,依次可分别使用的试剂和对应的现象正确的是
A. 碘水,变蓝色;浓硝酸,变黄色;新制Cu(OH)2,砖红色沉淀
B. 浓硝酸,变黄色;新制Cu(OH)2,砖红色沉淀;碘水,变蓝色
C. 新制Cu(OH)2,砖红色沉淀;碘水,变蓝色;浓硝酸,变黄色
D. 碘水,变蓝色;新制Cu(OH)2,砖红色沉淀;浓硝酸,变黄色
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】3月调研)[化学——选修3:物质结构与性质]氮化硼( BN)是一种重要的功能陶瓷材料。以天然硼砂(主要成分Na2B4O7)为起始物,经过一系列反应可以得到BN和火箭高能燃料及有机合成催化剂BF3的过程如下:

(1)写出由B203制备BF3的化学方程式 ,BF3中B原子的杂化轨道类型为____,BF3分子空间构型为____。
(2)在硼、氧、氟、氮中第一电离能由大到小的顺序是(用元素符号表示)____。
(3)已知:硼酸的电离方程式为H3B03 +H20 ![]() [B(OH)4] - +H+,试依据上述反应写出[ Al( OH)4] -的结构式____,并推测1mol NH4BF4(氟硼酸铵)中含有____个配位键。
[B(OH)4] - +H+,试依据上述反应写出[ Al( OH)4] -的结构式____,并推测1mol NH4BF4(氟硼酸铵)中含有____个配位键。
(4)由12个硼原子构成如图1的结构单元,硼晶体的熔点为1873℃,则硼晶体的1个结构单元中含有____ 个B-B键。

(5)氮化硼(BN)晶体有多种相结构。六方相氮化硼(晶体结构如图2)是通常存在的稳定相可作高温润滑剂。立方相氮化硼(晶体结构如图3)是超硬材料,有优异的耐磨性。
①关于这两种晶体的说法,不正确的是____(填字母)。
a.两种晶体均为分子晶体
b.两种晶体中的B-N键均为共价键
c.六方相氮化硼层间作用力小,所以质地软
d.立方相氮化硼含有σ键和π键,所以硬度大
②六方相氮化硼晶体内B-N键数与硼原子数之比为__ __,其结构与石墨相似却不导电,原因是____。
③立方相氮化硼晶体中,每个硼原子连接____个六元环。该晶体的天然矿物在青藏高原地下约300 km的古地壳中被发现。根据这一矿物形成事实,推断实验室由六方相氮化硼合成立方相氮化硼需要的条件应是 。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列有关物质的性质或应用的说法正确的是
A.晶体硅具有半导体性质,可用于生成光导纤维
B.用Na2O2漂白过的织物、麦秆日久又渐渐变成黄色
C.K2FeO4具有强氧化性,可用于自来水的杀菌消毒、
D.浓硫酸具有较强酸性,常用作淀粉水解的催化剂
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】用足量的一氧化碳还原14.5g铁的氧化物的混合物。将生成的气体通入足量的澄清石灰水中,生成沉淀25g,则该混合物的组合可能的是
A.Fe2O3、Fe3O4、FeO
B.FeO、Fe3O4
C.Fe3O4、Fe2O3
D.Fe3O4、Fe5O7
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】苯和液溴的取代反应的实验装置如图所示,其中A为具支试管改制成的反应容器,在其下端开了一小孔,塞好石棉绒,再加入少量铁屑。填写下列空白:

(1)写出A中反应的化学方程式__________________________________________。
(2)试管C中苯的作用是:________________。反应开始后,观察D和E两试管,看到的现象为:D________________;E________________。
(3)B中的NaOH溶液的作用是_____________________________________________,可观察到的现象是________________。
(4)在上述整套装置中,具有防倒吸的装置有________(填字母序号)。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】已知A的产量通常用来衡量一个国家的石油化工发展水平,B、D是饮食中两种常见的有机物,F是一种有香味的物质,F中碳原子数是D的两倍。现以A为主要原料合成F和高分子化合物E,其合成路线如图所示。
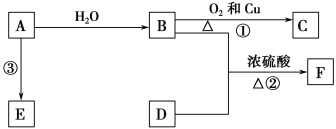
(1)A的结构式为____________,B中决定其性质的重要官能团的名称为____________。
(2)写出反应的化学方程式并判断反应类型。
①______________________________________,反应类型:____________。
③________________________,反应类型:____________。
(3)实验室怎样鉴别B和D?_________________________________________________。
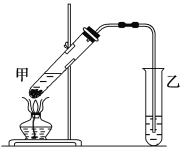
(4)该装置图中有一个明显的错误是_______________________________________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】【化学——选修2:化学与技术】
炼锌厂产生的工业废渣—锌渣(除了含Zn外,还含有Fe、Al、Cd和SiO2等杂质),利用锌渣制取并回收ZnSO4·7H2O和金属镉是一个有益的尝试,其流程如下:

已知:Fe3+、Al3+、Zn2+、Cd2+、Fe2+以氢氧化物完全沉淀时的pH分别为:3.2,4.7,6.5,9.4,9.7;锌的金属活动性比镉强。
试回答下列问题:
(1)“浸出”时用到的“试剂X”为___________(填名称)。
(2)写出“氧化”过程的离子方程式____________。
(3)“调pH”过程可以选用_____________。(从以下选项选择,填序号)
A.H2SO4 B.ZnO C.NaOH D.ZnCO3
“滤渣2”的主要成分是___________(填化学式,下同)。
(4)“试剂Y”是_______________;写出除去Cd2+的化学方程式_______________。
(5)“操作1”的方法是_______________;在“操作1”时,必须采取的实验措施是___________。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com