
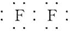 ��
������ �ס��ҡ����������졢��Ϊ������Ԫ���γɵ��������ӣ����ǵĵ���������Ϊ18��
��1����Ϊ˫�˵��ʷ��ӣ�����ˮ�����û���Ӧ�����ΪF2��
��2����Ϊ����Ԫ���γɵ�˫�����ӣ��������ӵ�ˮ��Һ�м���������ˮ���ֻ��ǣ�����ΪHS-����������Ӧ����S��HCl��
��3����Ϊ������Ԫ�صķ��ӣ���ԭ�Ӹ�����Ϊ1��1��ʵ�����п����ñ��Ʊ����������ΪH2O2���ڶ������������������·ֽ�����ˮ��������
��4������18���ӵ�����ΪC2H6��
��5����Ϊ����Ԫ����ɵ���ԭ�ӷ��ӣ������������ȼ�ϣ���ΪN2H4��N2H4��H2O2��Ӧ�����ɶԻ���û��Ӱ����������ʣ�һ���Ǵ�������Ҫ�ɷ֣���һ���ڳ���������ɫҺ�壬�����߷�Ӧ���ɵ�����ˮ��
��� �⣺�ס��ҡ����������졢��Ϊ������Ԫ���γɵ��������ӣ����ǵĵ���������Ϊ18��
��1����Ϊ˫�˵��ʷ��ӣ�����ˮ�����û���Ӧ�����ΪF2������ʽΪ��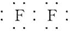 ��
��
�ʴ�Ϊ��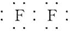 ��
��
��2����Ϊ����Ԫ���γɵ�˫�����ӣ��������ӵ�ˮ��Һ�м���������ˮ���ֻ��ǣ�����ΪHS-����������Ӧ����S��HCl����Ӧ���ӷ���ʽΪ��Cl2+HS-�TS��+2Cl-+H+��
�ʴ�Ϊ��Cl2+HS-�TS��+2Cl-+H+��
��3����Ϊ������Ԫ�صķ��ӣ���ԭ�Ӹ�����Ϊ1��1��ʵ�����п����ñ��Ʊ����������ΪH2O2���ڶ������������������·ֽ�����ˮ����������Ӧ����ʽΪ��2H2O2$\frac{\underline{\;MnO_2\;}}{\;}$2H2O+O2����
�ʴ�Ϊ��2H2O2$\frac{\underline{\;MnO_2\;}}{\;}$2H2O+O2����
��4������18���ӵ�����ΪC2H6��1 g������ȫȼ�շų�52 kJ������������ȫȼ�յĻ�ѧ����ʽΪ2C2H6+7O2$\frac{\underline{\;��ȼ\;}}{\;}$4CO2+6H2O��������ȫȼ�յ��Ȼ�ѧ����ʽΪ��2C2H6��g��+7O2��g���T4CO2��g��+6H2O��l����H=-3 120 kJ•mol-1��
�ʴ�Ϊ��2C2H6��g��+7O2��g���T4CO2��g��+6H2O��l����H=-3 120 kJ•mol-1��
��5����Ϊ����Ԫ����ɵ���ԭ�ӷ��ӣ������������ȼ�ϣ���ΪN2H4�����еĻ�ѧ��Ϊ���ۼ���N2H4��H2O2��Ӧ���ɵ�����ˮ����Ӧ����ʽΪ��N2H4+2H2O2�TN2+4H2O��
�ʴ�Ϊ��N2H4�����ۼ���N2H4+2H2O2�TN2+4H2O��
���� ���⿼��������ƶϣ���������Ԫ�ػ��������ʣ������ѧ����10���ӡ�18���������ǻ���֪ʶ���ۺϿ��飮



| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | �����Ǵ�����Ҵ������ǻ���� | |
| B�� | ������ϩ������������������ܷ����ӳɷ�Ӧ | |
| C�� | ʯ�͵ķ����ú�ĸ������˻�ѧ�仯 | |
| D�� | ��ȥ�������������������ᣬ�ñ���̼������Һϴ�Ӻ��Һ |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | ����NH4+��Cl-��H+��OH-���ӵ���Һ�У�һ���У�c��Cl-����c��NH4+����c��H+����c��OH-�� | |
| B�� | pH=6�Ĵ���������ƵĻ����Һ�У�c��Na+����c��CH3COO-�� | |
| C�� | 0.1mol/L��Na2S��Һ�У�c��OH-��=c��H+��+c��HS-��+2c��H2S�� | |
| D�� | pH=3��һԪ���pH=11��һԪǿ��������Ϻ����Һ�У�c��OH-��=c��H+�� |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | 3�� | B�� | 5�� | C�� | 6�� | D�� | 10�� |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
 �ɼ�дΪ
�ɼ�дΪ ������ij������w�ķ��ӽṹ�ɱ�ʾΪ
������ij������w�ķ��ӽṹ�ɱ�ʾΪ ��
���鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ��ƶ���
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ��ƶ���
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����

| A�� | ���̢��У�FeS��O2��H2SO4��Ӧ�Ļ�ѧ����ʽ��4FeS+3O2+6H2SO4�T2Fe2��SO4��3+6H2O+4S | |
| B�� | ���̢��в����������Դ��������Ⱦ����ѡ������������Һ���� | |
| C�� | ���̢��У���Ҫ���������������ϡ���� | |
| D�� | ���̢��е�ʵ�����������Ũ������ȴ�ᾧ�����ˡ�ϴ�� |
�鿴�𰸺ͽ���>>
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com