
电化学在日常生活中用途广泛,图甲是镁一次氯酸钠燃料电池,电池总反应为:Mg+ClO-+H2O==Cl-+Mg(OH)2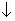 ,图乙是含Cr2O72-的工业废水的处理。下列说法正确的是
,图乙是含Cr2O72-的工业废水的处理。下列说法正确的是

A.图甲中发生的还原反应是Mg2++ClO-+H2O+2e-=Cl-+Mg(OH)2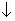
B.图乙中Cr2O72-向惰性电极移动,与该极附近的OH-结合转化成Cr(OH)3除去
C.图乙电解池中,若有0.084 g阳极材料参与反应,则阴极会有336 mL的气体产生
D.若图甲燃料电池消耗3.6 g镁产生的电量用以图乙废水处理,理论上可产生10.7 g氢氧化铁沉淀
科目:高中化学 来源: 题型:
在密闭容器中进行如下反应:X2(g)+Y2(g)  2Z(g),已知X2、Y2、Z的起始浓度分别为0.1mol/L、0.3mol/L、0.2mol/L,在一定条件下,当反应达到平衡时,各物质的浓度有可能是 ( )
2Z(g),已知X2、Y2、Z的起始浓度分别为0.1mol/L、0.3mol/L、0.2mol/L,在一定条件下,当反应达到平衡时,各物质的浓度有可能是 ( )
A. Z为0.3mol/L B. Y2为0.4mol/L C. X2为0.2mol/L D.Z为0.4mol/L
查看答案和解析>>
科目:高中化学 来源: 题型:
在中性含有Na+的溶液中,还可能存在NH4+,Fe2+,Br-,CO32-,I-,SO32-六种离子中的一种或几种,进行如下实验:
(1)原溶液滴加足量氯水后,有气泡生成,溶液呈橙黄色
(2)向橙黄色溶液中加BaCl2溶液无沉淀生成
(3)橙黄色溶液不能使淀粉变蓝
由此推断原溶液中一定不存在的离子是( )
A.NH4+,Br-,CO32- B.NH4+,I-,SO32-
C.Fe2+,I-,CO32- D.Fe2+,I-,SO32-
查看答案和解析>>
科目:高中化学 来源: 题型:
明矾石的主要成分是K2SO4·Al2(SO4)3·2Al2O3·6H2O,还含有杂质Fe2O3。利用明矾石来制取纯净的Al2O3、K2FeO4和H2SO4的工艺流程如图所示。

请回答下列问题:
(1)焙烧炉中发生反应的化学方程式为 ↑,若生成102gAl2O3,转移的电子数目为 .
↑,若生成102gAl2O3,转移的电子数目为 .
(2)生成沉淀I的离子方程式为 ,沉淀II的化学式为 。
(3)溶液经加硫酸调节pH后,过滤,洗涤,可得沉淀I,证明沉淀I已洗涤干净的实验操作和现象是 。
(4)写出Cl2将沉淀Ⅱ氧化为K2FeO4的化学方程式: 。
(5)从滤液中得到K2SO4晶体的方法是 。
(6) K2FeO4也可以铁为电极,通过电解浓的KOH溶液来制取,写出电解法制取K2FeO4的
阳极反应式: .
查看答案和解析>>
科目:高中化学 来源: 题型:
右图所示的甲、乙、丙三种物质均含有相同的某种元素,箭头表示物质间的转化一步就能实现,则甲可能是
①C ②H2O2 ③Na ④Fe ⑤HNO3
A.仅①③④ B.仅①②⑤
C.仅①②③⑤ D.①②③④⑤
查看答案和解析>>
科目:高中化学 来源: 题型:
下列分类,完全正确的是
| A | B | C | D | |
| 强电解质 | H2SO4 | NaCl | HClO | HNO3 |
| 弱电解质 | HF | NH3 | CaCO3 | H2CO3 |
| 非电解质 | Cl2 | CH3COOH | C2H5OH | SO2 |
查看答案和解析>>
科目:高中化学 来源: 题型:
在一洁净锥形瓶中,先用酸式滴定管准确移取25.00mL某未知浓度的盐酸于其中,再用0.20mol·L-1的NaOH溶液(指示剂为酚酞)进行滴定。滴定结果如下:
| 滴定次数 | NaOH起始读数 | NaOH终点读数 |
| 第一次 | 0.10 mL | 18.60 mL |
| 第二次 | 0.30 mL | 18.00 mL |
(1)根据以上表格中数据可以计算出盐酸的物质的量浓度为 mol·L-1
(2)达到滴定终点的标志是
(3)以下操作造成测定结果偏高的原因可能是 。
A.未用标准液润洗碱式滴定管
B.滴定到终点读数时发现滴定管尖嘴处悬挂一滴溶液
C.配制标准溶液的氢氧化钠中混有Na2CO3杂质
D.滴定终点读数时,俯视滴定管的刻度,其它操作均正确
E.盛装未知液的锥形瓶用蒸馏水洗过,未用待测液润洗
查看答案和解析>>
科目:高中化学 来源: 题型:
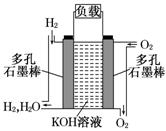 被誉为改变未来世界的十大新科技之一的燃料电池具有无污染、无噪音、高效率的特点。右图为氢氧燃料电池的结构示意图,电解质溶液为KOH溶液,电极材料为疏松多孔石墨棒.当氧气和氢气分别连续不断地从正、负两极通入燃料电池时,便可在闭合回路中不断地产生电流.试回答下列问题:
被誉为改变未来世界的十大新科技之一的燃料电池具有无污染、无噪音、高效率的特点。右图为氢氧燃料电池的结构示意图,电解质溶液为KOH溶液,电极材料为疏松多孔石墨棒.当氧气和氢气分别连续不断地从正、负两极通入燃料电池时,便可在闭合回路中不断地产生电流.试回答下列问题:
(1) 写出氢氧燃料电池工作时正极电极反应方程式:_______
(2) 若将此燃料电池改为以肼( N2H4)和氧气为原料(其他条件不变),工作时(产物为N2 , H2O)负极电极反应式为______
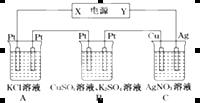
(3) 用上述氢氧燃料电池作直流电源进行电解,装置如下图所示。若通电5 min时,铜电极质量增加2.16 g。试回答:
① 电源中Y电极为直流电源的__________极。(填“正”或“负”)
② 通电5 min后B中pH变化:________,(填“增大”、“减小”或“不变”)。
③ 通电5 min时氢氧燃料电池中,理论上消耗标准状况下_______L氧气。
④ A中KCl溶液体积也是200 mL,通电5 min后,溶液的OH-浓度_______mol·L-1(设电解前后溶液体积无变化且KCl有剩余)。
⑤ 通电5 min时,B中共收集224 mL气体(标况),溶液体积为200 mL,则通电前CuSO4溶液的物质的量浓度为____________(设电解前后溶液体积无变化)。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com