
����Ŀ��ij��ѧ�о���ѧϰС�����ʵ��̽��ͭ�ij�����ѧ���ʣ�����������£��������
����1�������ڱ��У�ͭ������λ�úܽӽ���ͭ���������ã����������������ԣ�������ͭҲ��������
����2������ͭ���б�ۣ�һ������£������������ȶ���С�������۵�������һ��ͭ���ȶ���ҲС�������۵�ͭ��
����3������ͭ�������ԣ��ܱ�H2��CO��ԭ����Ҳ�ܱ�����ij����̬�⻯�ﻹԭ��
ʵ��̽��
��1��I���������1a.���õ���ҩƷ��1molL��1CuSO4��Һ��ϡ������������Լ��Ļ�ѧʽ����Һ��
b.�õ�����������1molL��1CuSO4��Һ250mL��ѡ�õ��������ձ���������ƽ��ҩ�ס�
����������ͷ�ι��⣬���������������ƣ���
c.Ϊ�ﵽʵ��Ŀ�ģ����㲹ȫʵ�����ݺͲ��裺
����CuSO4��Һ�Ʊ�Cu��OH��2��
�� ��
��2���������2ȡһ����I���Ʊ���õ�������ͭ���������������գ����¶ȴﵽ80��100��õ���ɫ�����ĩ������������1000�����ϣ���ɫ��ĩȫ����ɺ�ɫ��ĩ������ͭ��ȡ������ɫ������ͭ��ĩ�ڽྻ�Թ��У����������ϡ���ᣨ�����ᣩ���õ���ɫ��Һ��ͬʱ�۲쵽�Թܵײ����к�ɫ������ڣ���������ʵ������ش����⣮
a.д��������ͭ��ϡ���ᣨ�����ᣩ��Ӧ�����ӷ���ʽ�� ��
b.��ʵ���ɵó��Ľ������ڸ�������һ��ͭ��������ͭ�����ȶ����ȶ�����
��Һ����һ��ͭ��������ͭ�����ȶ����ȶ�����
��3���������3�������װ�ã��г�װ��δ��������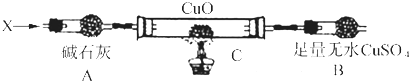
������ij����̬�⻯�X������ͨ�����ȵ�����ͭʱ���۲쵽����ͭ�ɺ�ɫ����˺�ɫ����ˮ����ͭ�����ɫ���������л���һ������Ⱦ�ĵ�������Y����Xͨ�����ȵ�CuOȼ�չ���ȫ��Ӧ������0.01mol X�����Bװ������0.36g�����ռ���0.28g����Y��
a.����A�������� ��
b.X�Ļ�ѧʽΪ ��
���𰸡�
��1��NaOH��Һ��250mL������ƿ����Cu��OH��2�ֱ����ϡ�����ϡNaOH��Һ�У��۲�����
��2��Cu2O+2H+=Cu+Cu2++H2O���ȶ������ȶ�
��3������ܣ�N2H4
���������⣺��1���������1a.Ҫ֤��Cu��OH��2�������ԣ�Ҫ֤��Cu��OH��2�������ԣ�Ӧ�ȼ��������Cu��OH��2 �� ����Ҫ����������ͭ�����Լ��Ӧ��ʵ�飬�ݴ�ѡ���Լ�1molL��1CuSO4��Һ��ϡ���ᡢ����������Һ�����Դ��ǣ�NaOH��Һ��b.��������һ�������һ�����ʵ���Ũ�ȵ���Һ���õ��������ձ���������ƽ��ҩ�ס�����������ͷ�ιܡ�250mL������ƿ�����Դ��ǣ�250mL������ƿ��c.֤��Cu��OH��2�������ԣ�Ӧ�ȼ��������Cu��OH��2 �� ����Ҫ����������ͭ�����Լ��Ӧ��ʵ�飬���Դ��ǣ���Cu��OH��2�ֱ����ϡ�����ϡNaOH��Һ�У��۲�����2���������2 a.������Ϣ����ɫ������ͭ��ĩ�ڽྻ�Թ��У����������ϡ���ᣨ�����ᣩ���õ���ɫ��Һ��ͬʱ�۲쵽�Թܵײ����к�ɫ���壬�����ӷ���ʽΪ��Cu2O+2H+=Cu+Cu2++H2O�����Դ��ǣ�Cu2O+2H+=Cu+Cu2++H2O��b.������Ϣ��������ͭ���壬�����������գ����¶ȴﵽ80��100��õ���ɫ�����ĩ������������1000�����ϣ���ɫ��ĩȫ����ɺ�ɫ��ĩ������ͭ�������ڲ�ͬ�¶��·�Ӧ�����ɿ�ȷ�����ʵ��ȶ��ԣ����Ը���1000��ʱCu2O��CuO�ȶ�������Һ�У�Cu2O+2H+=Cu+Cu2++H2O������Cu2+��Cu+�ȶ������Դ��ǣ��ȶ������ȶ�����3���������3 a.�����ṩ������ȷ��A��B�����Ǹ���ܣ����Դ��ǣ�����ܣ�b.����0.01mol X�����Bװ������0.36g��������0.02mol��ˮ�����ռ�����������Y 0.28g������0.01mol������ԭ���غ����ȷ����̬�⻯��X�к���4����ԭ�Ӻ�2����ԭ�ӣ�X�Ļ�ѧʽΪN2H4 �� ���Դ��ǣ�N2H4 ��


 �Ķ��쳵ϵ�д�
�Ķ��쳵ϵ�д�
| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��������ĿҪ����գ�
��1��Mg2+�Ľṹʾ��ͼΪ��O�ĵ���ʽΪ��H2S�ĽṹʽΪ ��
��2���Ȼ��Ƶĵ���ʽΪ �� ����ˮ��������ĵ��뷽��ʽΪ �� ���Ȼ�����Һ�е���������ʱ������Ӧ�����ӷ���ʽΪ ��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ����NA��ʾ�����ӵ�������ֵ������˵����ȷ����
A. 17gOH-�к��еĵ�����ΪNA
B. 6.5gZn���������ᷴӦʧȥ�ĵ�����Ϊ0.2NA
C. 1L1mol/LCaC12��Һ�к��е�Cl-������ĿΪNA
D. ���³�ѹ�£�11.2LO2�к��е�ԭ����ĿΪNA
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ����«���ṹ����ʽ�����㷺������ʳ����� 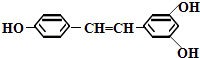 ɣ驡����������������ѣ��У������ܾ��п����ԣ��ܹ���1mol�û�������Ӧ��Br2��H2����������ֱ��ǣ� ��
ɣ驡����������������ѣ��У������ܾ��п����ԣ��ܹ���1mol�û�������Ӧ��Br2��H2����������ֱ��ǣ� ��
A.6mol��7mol
B.5mol��7mol
C.3.5mol��6mol
D.1mol��1mol
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��ij��Һ��ֻ���ܺ���H+��NH4+��Mg2+��Al3+��Fe3+��CO32����SO42����NO3���еļ��֣���������п����������ɫ��ζ�����壻��������NaOH��Һ��������ɫ�������Ҳ����ij����������NaOH�����ʵ���֮��Ĺ�ϵ��ͼ��ʾ��������˵����ȷ���ǣ� �� 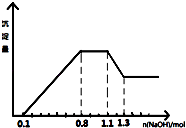
A.��Һ�е�������ֻ��H+��Mg2+��Al3+���ܺ���Fe3+
B.��Һ��һ������CO32����NO3�� �� һ������SO42��
C.��Һ��c��NH4+��=0.3 mol/L
D.c��H+����c��Al3+����c��Mg2+��=1��1��1
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ����NAΪ�����ӵ�������ֵ������˵����ȷ���ǣ� ��
A.��״���£�22.4LCCl4����C��Cl������ĿΪ4NA
B.ȡ50mL 14.0mol/LŨ����������ͭƬ��Ӧ������������ӵ���ĿΪ0.35 NA
C.��ӦNH4N3 ![]() 2N2��+2H2������״����ÿ����22.4LN2 �� ת�Ƶ��ӵ���ĿΪ2 NA
2N2��+2H2������״����ÿ����22.4LN2 �� ת�Ƶ��ӵ���ĿΪ2 NA
D.��⾫��ͭʱ����ת�Ƶĵ�����ΪNA����������������С32g
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��һ����̬������һ����̬ϩ���Ļ����9g�����ܶ�����ͬ�����������ܶȵ�11.25�������������ͨ��������ˮʱ����ˮ����4.2g������������̬���ǣ� ��
A.�������ϩ
B.�������ϩ
C.����ͱ�ϩ
D.����Ͷ�ϩ
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ����15.6gNa2O2��5.4gAlͬʱ����һ������ˮ�У���ַ�Ӧ��õ�200mL��Һ���ٻ���ͨ��HCl����6.72L����״����������Ӧ��������Һ��������ֲ��䣬�� ��
A.��Ӧ�����еõ�6.72L�����壨��״����
B.���յõ�����Һ������ΪNaCl��NaOH
C.���յõ�15.6g�ij���
D.���յõ�����Һ��NaCl�����ʵ���Ũ��Ϊ1.5mol/L
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ����100mL��NaOH��Һ��ͨ��CO2��ַ�Ӧ���ڼ�ѹ�ͽϵ��¶��£�С�ĵؽ���Һ���ɣ��õ���ɫ����M��ͨ���CO2���������״������M�������Ĺ�ϵ��ͼ��ʾ���Իش��������⣺
��1��A��ʱ����ɫ����M�Ļ�ѧʽΪ �� ͨ���CO2�����ΪmL����״���£���ͬ����
��2��C��ʱ����ɫ����M�Ļ�ѧʽΪ �� ͨ���CO2�����ΪmL��
��3��B��ʱM����ɳɷ�Ϊ���û�ѧʽ��ʾ����ͨ���CO2�����ΪmL��
��4����NaOH��Һ�����ʵ���Ũ��Ϊ ��
�鿴�𰸺ͽ���>>
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com