
【题目】碳、氮、硫的化合物在生产生活中广泛存在。请回答:
(1)以CO2与NH3为原料可合成化肥尿素[CO(NH2)2]。已知:
①2NH3(g)+CO2(g)=NH2CO2NH4(s) ΔH=-l59.5kJ·mol-1
②NH2CO2NH4(s)=CO(NH2)2(s)+H2O(l) ΔH=-160.5kJ·mol-1
写出CO2与NH3合成尿素和液态水的热化学反应方程式__。
(2)T温度时在容积为2L的恒容密闭容器中只充入1.00molNO2气体发生反应:2NO(g)+O2(g)![]() 2NO2(g) H<0。不同时刻测得容器中n(NO2)如下表:
2NO2(g) H<0。不同时刻测得容器中n(NO2)如下表:
时间/s | 0 | 1 | 2 | 3 | 4 | 5 |
n(NO2)/mol | 1.00 | 0.80 | 0.65 | 0.55 | 0.50 | 0.50 |
①升高温度K值___(增大、减小),T温度时化学平衡常数K=___mol-1·L
②从0~2s该反应的平均速率v(NO2)=___。
③对可逆反应2NO(g)+O2(g)![]() 2NO2(g) H<0。恒温,恒容密闭容器中,下列说法中,能说明该反应达到化学平衡状态的是___。
2NO2(g) H<0。恒温,恒容密闭容器中,下列说法中,能说明该反应达到化学平衡状态的是___。
A.混合气体的密度不再变化
B.混合气体的压强不再变化
C.氧气的转化率不再变化
D.N2、O2、NO的物质的量之比为1:1:2
(3)常温下,用SO2与NaOH溶液反应可得到NaHSO3、Na2SO3等。
①已知Na2SO3水溶液显碱性,原因是___(写出主要反应的离子方程式),该溶液中,c(Na+)___2c(SO32-)+c(HSO3-)(填“>”“<”或“=”)。
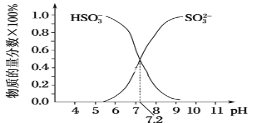
②在某NaHSO3、Na2SO3混合溶液中HSO3-、SO32-物质的量分数随pH变化曲线如图所示(部分),根据图示,则SO32-的第一步水解平衡常数=____。
【答案】2NH3(g)+CO2(g)=CO(NH2)2(s)+H2O(l) △H=-320.0kJ/mol 减小 8 0.0875mol/(L·s) BC SO32-+H2O![]() HSO3-+OH- > 10-6.8
HSO3-+OH- > 10-6.8
【解析】
(1)依据热化学方程式和盖斯定律计算①+②得到CO2与NH3合成尿素和液态水的热化学反应方程式;
(2)①2NO(g)+O2(g)![]() 2NO2(g) H<0,温度升高,平衡逆向移动,则K减小;
2NO2(g) H<0,温度升高,平衡逆向移动,则K减小;  ,根据化学平衡常数K1=
,根据化学平衡常数K1=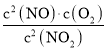 计算K1,进而计算2NO(g)+O2(g)2NO2(g)化学平衡常数K=
计算K1,进而计算2NO(g)+O2(g)2NO2(g)化学平衡常数K=![]() ;
;
②根据v=![]() 计算出前2s内v(NO2);
计算出前2s内v(NO2);
③根据化学平衡状态分析;
(3)①亚硫酸根离子水解导致溶液显示碱性,根据电荷守恒确定离子浓度的关系;
②根据水解平衡常数表达式结合图中数据来计算。
(1)①2NH3(g)+CO2(g)=NH2CO2NH4(s)△H=-l59.5kJmol-1,②NH2CO2NH4(s)=CO(NH2)2(s)+H2O(l)△H=-160.5kJmol-1,依据热化学方程式和盖斯定律计算①+②得到CO2与NH3合成尿素和液态水的热化学反应方程式为2NH3(g)+CO2(g)=CO(NH2)2(s)+H2O(l) △H=-320.0kJ/mol,故答案为:2NH3(g)+CO2(g)=CO(NH2)2(s)+H2O(l) △H=-320.0kJ/mol;
(2)①2NO(g)+O2(g)![]() 2NO2(g) H<0,温度升高,平衡逆向移动,则K减小;
2NO2(g) H<0,温度升高,平衡逆向移动,则K减小;  ,根据化学平衡常数K1=
,根据化学平衡常数K1=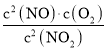 =0.125,所以2NO(g)+O2(g)2NO2(g)化学平衡常数K=
=0.125,所以2NO(g)+O2(g)2NO2(g)化学平衡常数K=![]() =8,故答案为:减小;8;
=8,故答案为:减小;8;
②根据表中数据计算出前2s内v(NO2)=![]() =
=![]() =
=![]() =0.0875mol/(Ls),故答案为:0.0875mol/(L·s);
=0.0875mol/(Ls),故答案为:0.0875mol/(L·s);
③A.该可逆反应在恒容条件下进行,质量反应前后不变,则混合气体的密度始终不变化,错误;
B.该可逆反应在恒容条件下进行,正向进行,体积减小,则压强减小,当混合气体的压强不再变化时,该反应达到化学平衡状态,正确;
C.反应没平衡时,氧气的转化率会变化,当氧气的转化率不变化时,该反应达到化学平衡状态,正确;
D.物质的量之比不能作为判断化学平衡状态依据,错误;
综上,正确的为BC,故答案为:BC;
(3)①亚硫酸根离子水解导致溶液显示碱性,原理是:SO32-+H2OHSO3-+OH-,所以,该溶液中,c(H
②亚硫酸根离子的水解平衡常数K= 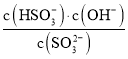 ,当pH=7.2时,SO32-、HSO3-浓度相等,所以K=c(OH-)=10-6.8,故答案为:10-6.8。
,当pH=7.2时,SO32-、HSO3-浓度相等,所以K=c(OH-)=10-6.8,故答案为:10-6.8。


 愉快的寒假南京出版社系列答案
愉快的寒假南京出版社系列答案科目:高中化学 来源: 题型:
【题目】25°C,向20mL 0.1mol·L-1的H2A溶液中滴加0.1mol·L-1的KOH溶液,滴定曲线如图,下列说法不正确的是
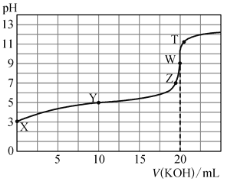
A.H2A的电离方程式:H2AH++HA-,HA-H++A2-
B.X点溶液中:c(HA-)+c(H2A)+c(A2-)=0.1 mol·L-1
C.Z点溶液中存在关系c(K+)=c(HA-)+2c(A2-)
D.W点时,c(K+)>c(OH-)>c(HA-)>c(H2A)>c(A2-)>c(H+)
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】由铜、铁和硫酸铜溶液组成的原电池中,作正极的是_______________,正极的电极反应式为____________________________;作负极的是______________,电子由___________________(填“正”或“负”,下同)极经导线移向________________极,总反应的离子方程式为_________________________。

查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】莫尔盐是硫酸盐的一种复盐,是一种重要的化学试剂,它的水溶液中加入KSCN不显红色,并有如图所示的反应:
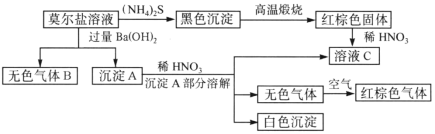
根据以上关系,按要求填空:
(1)可用检验气体B__________________。
(2)莫尔盐的化学式为____________________。
(3)部分沉淀A与稀HNO3反应的离子方程式是_____________________。
(4)古代硫酸的制法是隔绝空气锻烧绿矾(FeSO4·7H2O),将蒸气冷却可制得一种无色粘稠的液体“绿矾油”,剩余的固体为红棕色。(已知SO3的熔点是16.8°C,沸点是44.8°C,再加矾受热分解的产物)

①装置的连接顺序为______________。
②B的作用是验证该反应有水生成,其中的试剂为_________,实验过程中发现F中溶液褪色,D中出现无色粘稠液体,则煅烧绿矾的反应方程式为_____________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】(1)A、B、C、D、E均是短周期元素,其原子序数依次增大,A和B同周期,A原子最外层电子数是内层电子数的二倍,B元素族序数是周期数的三倍,B的阴离子与C的阳离子电子层结构相同,C的单质与B的单质在不同条件下反应,可生成C2B或C2B2,D单质是一种淡黄色固体。请回答:
①C2B2的电子式是___________,D、E可形成化合物DE2中,存在下列哪些静电作用力______。
a.极性键 b.非极性键 c.范德华力 d.氢键 e.离子键
②B、C、E的离子半径由大到小的顺序为_______________(用化学式回答),举一个事实证明E和D非金属性的强弱___________________(用离子反应方程式表示)。
(2)氨和二氧化碳反应可生成尿素CO(NH2)2。尿素在一定条件下会失去氨而缩合,如两分子尿素失去一分子氨形成二聚物:

当尿素三聚时,得到两种产物,其中一种为环状结构,请画出其结构式___________。
(3)已知某元素的原子序数是33,试推测该元素:
①原子的原子结构示意图______________。
②在元素周期表中的位置______________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】如图是镁元素和硫元素的相关信息,由此不能得到的信息是( )

A.镁属于金属元素
B.镁原子核内有12个质子
C.镁离子与硫离子的电子层数相等
D.在化学反应中,1个硫原子容易得到2个电子
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】在2L恒温密闭容器中通入气体X并发生反应:2X(g)![]() Y(g)(正反应放热),X的物质的量n(X)随时间t变化的曲线如图所示(图中的两条曲线分别代表有、无催化剂的情形),下列叙述正确的是( )
Y(g)(正反应放热),X的物质的量n(X)随时间t变化的曲线如图所示(图中的两条曲线分别代表有、无催化剂的情形),下列叙述正确的是( )

A.实线表示使用催化剂的情形
B.b、c两点表明反应在相应的条件下达到了最大限度
C.反应进行到a点时放出的热量多于反应进行到b点时放出的热量
D.反应从开始到a点的平均反应速率可表示为v(Y)=0.01mol·L-1·min-1
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】A是一种常见的单质,B、C为中学化学常见的化合物,A、B、C均含有元素X。它们有如下的转化关系(部分产物及反应条件已略去),下列判断正确的是

A.X元素可能为Al
B.X元素不一定为非金属元素
C.反应①和②互为可逆反应
D.反应①和②一定为氧化还原反应
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】已知 NA是阿伏加德罗常数的值,下列说法正确的是
A.32gS8与 S6(![]() )的混合物中所含共价键数目为NA
)的混合物中所含共价键数目为NA
B.1L0.1mol L-1H2C2O4溶液中含 C2O42- 离子数为0.1NA
C.2molNO与 2molO2在密闭容器中充分反应,转移的电子数为 8NA
D.标准状况下 22.4L氯气与甲烷的混合气体,光照时充分反应生成 HCl分子数为NA
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com