
【题目】钾和钠的化学性质相似。下列说法能最好地解释这个事实的是
A.都是金属元素B.原子半径相差不大
C.最外层电子数相同D.电子层数相同
科目:高中化学 来源: 题型:
【题目】短周期元素A、B的原子序数相差2,则下列叙述正确的是( )
A.A、B可能在同一主族B.A、B一定属于同一周期
C.A、B一定属于不同周期D.A、B一定属于同一主族
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】化合物![]() 是治疗高血压的药物“比索洛尔”的中间体,一种合成
是治疗高血压的药物“比索洛尔”的中间体,一种合成![]() 的路线如下:
的路线如下:

已知以下信息:
①![]() 的核磁共振氢谱为单峰;
的核磁共振氢谱为单峰; ![]() 的核磁共振氢谱为三组峰,峰面积比为
的核磁共振氢谱为三组峰,峰面积比为![]() .
.
②![]() 的苯环上仅有两种不同化学环境的氢;
的苯环上仅有两种不同化学环境的氢; ![]() 可与
可与![]() 或
或![]() 反应.
反应.
回答下列问题:
(1)![]() 的结构简式为______________________.
的结构简式为______________________.
(2)![]() 的化学名称为_______________________.
的化学名称为_______________________.
(3)![]() 与
与![]() 反应生成
反应生成![]() 的化学方程式为______________________________.
的化学方程式为______________________________.
(4)由![]() 生成
生成![]() 的反应类型为_________________________________.
的反应类型为_________________________________.
(5)![]() 的分子式为______________________________________.
的分子式为______________________________________.
(6)![]() 是
是![]() 的同分异构体,可与
的同分异构体,可与![]() 溶液发生显色反应,
溶液发生显色反应, ![]() 的
的![]() 可与
可与![]() 的
的![]() 反应,
反应, ![]() 共有________种;其中核磁共振氢谱为四组峰,峰面积比为
共有________种;其中核磁共振氢谱为四组峰,峰面积比为![]() 的结构简式为________、________.
的结构简式为________、________.
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下表为元素周期表的一部分,其中X、Y、W、Z为知周期元素,T的单质常温下为液体。下列说法错误的是

A. X、Y的单质均存在同素异形体
B. Y、Z的简单氢化物的稳定性依次递增
C. 工业上电解NaW溶液得W2可使用阴离子交换膜
D. R的单质可用于制造半导体材料
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】能通过置换反应得到金属铁的是
A. Na与FeSO4溶液常温混合 B. CO通过灼热的Fe2O3
C. H2通入FeSO4溶液 D. Al和Fe3O4混合加热至高温
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】(1)近年来有人提出了一种利用氯碱工业产品及氯化钠循环治理含二氧化硫废气并回收二氧化硫的方法,该方法的流程如下:
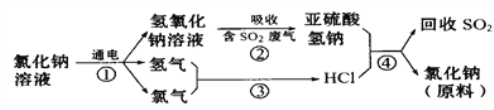
写出反应②的化学方程式______________________________。
(2)亚硫酸氢钠与甲醛经过一定反应,可以合成俗称“吊白块”的物质(该物质对人体有害),其结构简式为HOCH2SO3Na,根据其结构特点,可判断“吊白块”能发生的反应有________。
A.皂化反应 B.加聚反应 C.与金属钠反应 D.氧化反应
(3)近日,中科院大连化物所孙剑、葛庆杰研究员团队发现了二氧化碳高效转化新过程,通过设计一种新型多功能复合催化剂,首次实现了CO2 直接加氢制取高辛烷值汽油(用C5H12表示),试写出该反应的化学方程式____________________________________。
(4)煤的气化和液化属于______________(填“物理”或“化学”)变化。
(5)可燃冰属于新能源,我国是全球第一个成功稳定开采可燃冰的国家某种可燃冰(甲烷水合物)晶体中,平均每46个水分子构成8个分子笼,每个分子笼可容纳1个甲烷分子或1个水分子,若这8个分子笼中有6个容纳的是甲烷分子,另外2个被水分子填充,则这种可燃冰的平均组成可表示为____________
(6)海水中溴含量为65mg·L-1。若1L 海水中有95%的溴元素被氧化为Br2 经热空气吹出,溴单质残留量为3%。最后用SO2 将90%的Br2 还原成Br-,所得溶液体积为50mL,则所得溶液中溴离子浓度为原海水中溴离子浓度的_____________倍(计算结果精确到0.1)。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】在一定温度下的定容密闭容器中,当下列物理量不再变化时,可表明反应:A(g)+B(g)![]() C(g)+D(g) 已达化学平衡状态的是( )
C(g)+D(g) 已达化学平衡状态的是( )
A. 混合气体的压强 B. B的物质的量浓度 C. 混合气体的密度 D. v(A)正 = v(D)正
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】将4 mol A气体和2 mol B气体在体积为2 L的密闭容器中混合,并在一定条件下发生反应:2A(g)+B(g)![]() xC(g),若经2s后测得A的物质的量为2.8 mol,C的物质的量浓度为0.6mol/L。现有下列几种说法:①2s内用物质A表示的平均反应速率为0.3 mol/(L·s);②2s内用物质B表示的平均反应速率为0.6 mol/(L·s);③2s时物质B的转化率为70%;④x=2。其中正确的是( )
xC(g),若经2s后测得A的物质的量为2.8 mol,C的物质的量浓度为0.6mol/L。现有下列几种说法:①2s内用物质A表示的平均反应速率为0.3 mol/(L·s);②2s内用物质B表示的平均反应速率为0.6 mol/(L·s);③2s时物质B的转化率为70%;④x=2。其中正确的是( )
A. ①③ B. ②③ C. ①④ D. ③④
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】关于离子键、共价键的各种叙述中,下列说法中正确的是
A.在离子化合物里,只存在离子键,没有共价键
B.非极性键只存在于双原子的单质分子(如 Cl2)中
C.原子序数为 11 与 9 的元素能够形成离子化合物,该化合物中存在离子键
D.任何物质中都存在化学键
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com